固体A由3种元素组成,为研究其组成,设计如下实验:
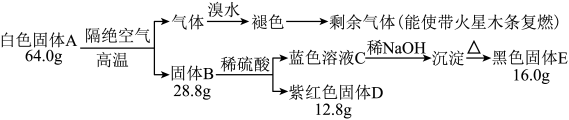
已知:气体通过溴水后,溶液中生成两种强酸。请回答下列问题:
(1)写出固体E的化学式_______ 。
(2)写出固体A在高温下隔绝空气反应的化学方程式_____________________ 。
(3)固体B与CO在高温下反应也可以生成D,试设计实验证明B是否反应完全:____ 。

已知:气体通过溴水后,溶液中生成两种强酸。请回答下列问题:
(1)写出固体E的化学式
(2)写出固体A在高温下隔绝空气反应的化学方程式
(3)固体B与CO在高温下反应也可以生成D,试设计实验证明B是否反应完全:
18-19高二·浙江·期中 查看更多[1]
(已下线)【新东方】高中化学-5018
更新时间:2019-11-15 08:35:17
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】CuCl2常用作催化剂。实验室用废铜屑(含少量CuO、Fe2O3、油污等杂质)制备CuCl2•2H2O的实验流程如图:
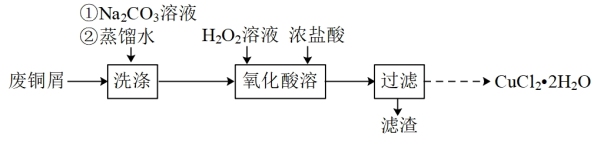
(1)“洗涤”时,Na2CO3溶液的作用是____ 。
(2)“氧化酸溶”在如图所示的装置中进行。
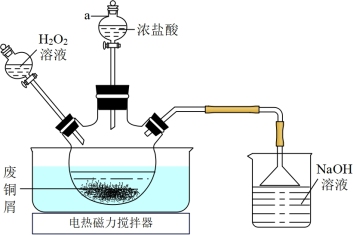
①仪器a的名称为____ 。
②三颈烧瓶中Cu转化为CuCl2的化学方程式为____ 。
(3)以“过滤”后的滤液X为原料制备CuCl2•2H2O晶体。请补充实验方案:向滤液X中____ ,过滤得滤液Y;向滤液Y中____ ,在低温下减压蒸发至____ ,冷却结晶,过滤,将所得固体洗涤、晾干,得到CuCl2•2H2O晶体。(已知该实验中pH=3.2时,Fe3+完全沉淀;pH=4.7时,Cu2+开始沉淀。实验中须用的试剂:CuO粉末,6.0mol·L-1HCl溶液。)
(4)通过下列方法测定CuCl2•2H2O样品的纯度:准确称取0.4800gCuCl2•2H2O样品,加适量水溶解,转移至碘量瓶中,加过量KI溶液,用稀H2SO4酸化,以淀粉溶液为指示剂,用0.1500mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液18.00mL。测定过程中发生下列反应:2Cu2++4I-=2CuI↓+I2;2S2O +I2=S4O
+I2=S4O +2I-。计算样品中CuCl2•2H2O的质量分数
+2I-。计算样品中CuCl2•2H2O的质量分数____ (写出计算过程,计算结果精确到小数点后两位)。

(1)“洗涤”时,Na2CO3溶液的作用是
(2)“氧化酸溶”在如图所示的装置中进行。

①仪器a的名称为
②三颈烧瓶中Cu转化为CuCl2的化学方程式为
(3)以“过滤”后的滤液X为原料制备CuCl2•2H2O晶体。请补充实验方案:向滤液X中
(4)通过下列方法测定CuCl2•2H2O样品的纯度:准确称取0.4800gCuCl2•2H2O样品,加适量水溶解,转移至碘量瓶中,加过量KI溶液,用稀H2SO4酸化,以淀粉溶液为指示剂,用0.1500mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液18.00mL。测定过程中发生下列反应:2Cu2++4I-=2CuI↓+I2;2S2O
 +I2=S4O
+I2=S4O +2I-。计算样品中CuCl2•2H2O的质量分数
+2I-。计算样品中CuCl2•2H2O的质量分数
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】某实验小组以废催化剂(含SiO2、ZnS、CuS及少量的Fe3O4)为原料,回收锌和铜,设计实验流程如图:
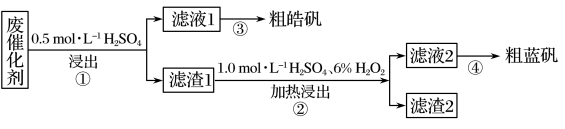
(1)在步骤①中,为提高浸出效率,可以采取的操作是_______ 、_______ (写出两种即可)。
(2) 粗皓矾的化学式为_______ ·7H2O,处理步骤①的污染气体可以用氢氧化钠溶液,利用到的原理为:_______ (用离子方程式表示)。
(3)在“滤液1”中,为检验是否含有Fe2+,可以采用的试剂是_______ ,若存在Fe2+,其现象为_______ 。
(4)已知蓝矾主要成分为:CuSO4·5H2O,步骤②发生主要反应的离子方程式为:_______ 。从“滤液2”中得到蓝矾的操作为:_______ 、_______ 、过滤、洗涤、干燥。

(1)在步骤①中,为提高浸出效率,可以采取的操作是
(2) 粗皓矾的化学式为
(3)在“滤液1”中,为检验是否含有Fe2+,可以采用的试剂是
(4)已知蓝矾主要成分为:CuSO4·5H2O,步骤②发生主要反应的离子方程式为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】实验室用粗铜(含杂质Fe)制备氯化铜。
(1)采用如下图所示的装置进行实验(部分仪器和夹持、加热装置已略去)。
①仪器A的名称是________________ ;
②实验开始前,需要做的操作是____________________ 。
③有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为______ (填“是”或“否”)必需。原因_______________________________________ 。
④实验过程中,装置C内的现象是___________________________________ 。
⑤氢氧化钠溶液的作用是______________________________ ,其中发生反应的主要离子方程式___________________________ 、________________________ 。
(2)若将C中所得固体加稀硫酸溶解。取少量溶液于小试管中,滴加2滴KSCN溶液,无现象。请用必要的文字和离子方程式解释出现这一现象的原因_________________ 。
(1)采用如下图所示的装置进行实验(部分仪器和夹持、加热装置已略去)。

①仪器A的名称是
②实验开始前,需要做的操作是
③有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为
④实验过程中,装置C内的现象是
⑤氢氧化钠溶液的作用是
(2)若将C中所得固体加稀硫酸溶解。取少量溶液于小试管中,滴加2滴KSCN溶液,无现象。请用必要的文字和离子方程式解释出现这一现象的原因
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某同学进行硫酸铜晶体(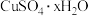 )结晶水含量的测定实验。完成下列填空:
)结晶水含量的测定实验。完成下列填空:
【实验步骤】:
(1)在__________ (填仪器名称)准确称量瓷坩埚的质量。
(2)在瓷坩埚中加入一定量的硫酸铜晶体,并称重。
(3)把盛有硫酸铜晶体的瓷坩埚放在泥三角上慢慢加热,直到蓝色完全变白,然后把坩埚移至_______ (填仪器名称)中冷却到室温,并称重。
(4)重复上述实验进行恒重操作,其目的是_______________ ,直到两次称量结果不超过______ 克。
(5)下面是该学生实验的一次数据,请完成计算:

______ ;(精确到0.01)实验相对误差是_________ (保留小数后一位)。
(6)这次实验中产生误差的原因可能是_______
a. 硫酸铜晶体中含有不挥发性杂质 b. 在加热过程中发现有黑色物质生成
c. 加热时有晶体飞溅出来 d. 加热失水后露置在空气中冷却
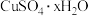 )结晶水含量的测定实验。完成下列填空:
)结晶水含量的测定实验。完成下列填空:【实验步骤】:
(1)在
(2)在瓷坩埚中加入一定量的硫酸铜晶体,并称重。
(3)把盛有硫酸铜晶体的瓷坩埚放在泥三角上慢慢加热,直到蓝色完全变白,然后把坩埚移至
(4)重复上述实验进行恒重操作,其目的是
(5)下面是该学生实验的一次数据,请完成计算:
| 坩埚质量(克) | 坩埚与晶体的质量(克) | 恒重后坩埚与固体质量 |
| 13.721 | 24.692 | 20.631 |

(6)这次实验中产生误差的原因可能是
a. 硫酸铜晶体中含有不挥发性杂质 b. 在加热过程中发现有黑色物质生成
c. 加热时有晶体飞溅出来 d. 加热失水后露置在空气中冷却
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】(1)CuSO4溶液是中学化学及工农业生产中常见的一种试剂。某同学利用CuSO4溶液,进行以下实验探究。
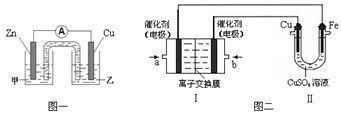
①图一是根据反应Zn+CuSO4=Cu+ZnSO4设计成的锌铜原电池。电解质甲溶液是_____ (填ZnSO4或CuSO4)溶液;Cu极的电极反应式是_______ 。
②图二中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则b处通入的是_______ (填CH4或O2),a处电极上发生的电极反应式是________ 。
(2)将蓝矾(CuSO4·5H2O)、生石灰和水按一定比例混合,即可得到波尔多液(杀菌剂),其有效成分为难溶的碱式硫酸铜[xCuSO4·yCu(OH)2]。为测定某碱式硫酸铜的组成进行了如下实验:取等质量的碱式硫酸铜样品两份,一份滴加稀盐酸至恰好完全溶解,另一份高温灼烧后只得到CuO固体。所得数据显示n(HCl)︰n(CuO)=3︰2,则该碱式硫酸铜的化学式中x︰y=_______ 。
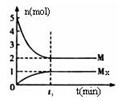
(3)E是非金属性最强的元素,M是E的气态氢化物,在固定体积的密闭容器中,气体M存在如下关系:xM(g) Mx(g),反应物和生成物的物质的量随时间的变化关系如下图。下列说法正确的是
Mx(g),反应物和生成物的物质的量随时间的变化关系如下图。下列说法正确的是___________ 。
A.该反应的化学方程式是2HF (HF)2
(HF)2
B.平衡时混合气体的平均摩尔质量是33.3
C.t1时刻,保持温度不变,再充入1molM,重新达到平衡时,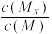 将增大
将增大
D.M的沸点比同主族下一周期元素的气态氢化物沸点低

①图一是根据反应Zn+CuSO4=Cu+ZnSO4设计成的锌铜原电池。电解质甲溶液是
②图二中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则b处通入的是
(2)将蓝矾(CuSO4·5H2O)、生石灰和水按一定比例混合,即可得到波尔多液(杀菌剂),其有效成分为难溶的碱式硫酸铜[xCuSO4·yCu(OH)2]。为测定某碱式硫酸铜的组成进行了如下实验:取等质量的碱式硫酸铜样品两份,一份滴加稀盐酸至恰好完全溶解,另一份高温灼烧后只得到CuO固体。所得数据显示n(HCl)︰n(CuO)=3︰2,则该碱式硫酸铜的化学式中x︰y=
(3)E是非金属性最强的元素,M是E的气态氢化物,在固定体积的密闭容器中,气体M存在如下关系:xM(g)
 Mx(g),反应物和生成物的物质的量随时间的变化关系如下图。下列说法正确的是
Mx(g),反应物和生成物的物质的量随时间的变化关系如下图。下列说法正确的是
A.该反应的化学方程式是2HF
 (HF)2
(HF)2B.平衡时混合气体的平均摩尔质量是33.3
C.t1时刻,保持温度不变,再充入1molM,重新达到平衡时,
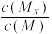 将增大
将增大D.M的沸点比同主族下一周期元素的气态氢化物沸点低
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某白色粉末A在农业上用作杀菌剂,进行下列实验:
①白色粉末A溶解在水中,得到蓝色溶液,分成等量的两份;
②在其中一份蓝色溶液中加入适量的盐溶液B,恰好沉淀完全,过滤,得到白色沉淀和蓝色溶液;在此蓝色溶液中滴加酸化的AgNO3溶液又得到白色沉淀和蓝色溶液;
③在①中的另一份蓝色溶液中加入适量C溶液,恰好沉淀完全,过滤,得到蓝色沉淀和纯净的硫酸钾溶液。
根据实验现象推断:
(1)A______________ B_______________ C_______________ (填化学式)
(2)反应③中的离子方程式为__________________________________________________
①白色粉末A溶解在水中,得到蓝色溶液,分成等量的两份;
②在其中一份蓝色溶液中加入适量的盐溶液B,恰好沉淀完全,过滤,得到白色沉淀和蓝色溶液;在此蓝色溶液中滴加酸化的AgNO3溶液又得到白色沉淀和蓝色溶液;
③在①中的另一份蓝色溶液中加入适量C溶液,恰好沉淀完全,过滤,得到蓝色沉淀和纯净的硫酸钾溶液。
根据实验现象推断:
(1)A
(2)反应③中的离子方程式为
您最近一年使用:0次



