部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共2.88g,经如下处理:
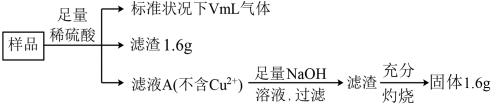
下列说法正确的是

下列说法正确的是
| A.滤液A中的阳离子为Fe2+、Fe3+、H+ | B.V=224 |
| C.样品中CuO的质量为2.0g | D.样品中铁元素的质量为0.56g |
更新时间:2019-10-12 10:56:58
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】将Cu放入0.1 mol•L﹣1FeCl3溶液中,反应一段时间后取出Cu片,溶液中Fe3+与Fe2+的物质的量浓度之比为4:3,则反应后溶液中Cu2+与Fe3+的物质的量之比为
| A.3:2 | B.3:8 | C.4:3 | D.3:4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列离子方程式书写错误的是
A.SO2通入双氧水中: |
B.NaOH浓溶液与饱和NH4Cl溶液: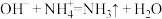 |
C.Pb与Fe2(SO4)3溶液: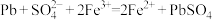 |
D.Ca(HCO3)2与澄清石灰水: |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】取 1LFeCl3溶液腐蚀铜板制作电路板,反应后在此残留液中慢慢加入铁粉,溶液中 Fe2+的浓度变化如图所示(加入固体引起的体积变化忽略不计),下列说法错误的是
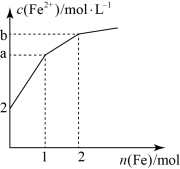
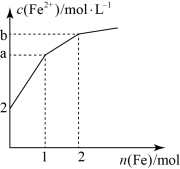
| A.当n(Fe)=0.5mol 时,发生的离子反应为 Fe+2Fe3+=3Fe2+ |
| B.当 n(Fe)=1.5mol 时,溶液中发生的总反应离子方程式为4Fe3++Cu2++3Fe=7Fe2++Cu |
| C.当n(Fe)=1mol 时,溶液中 c(Fe2+)=5 mol·L-1 |
| D.腐蚀之前原溶液中n(Fe3+)=4 mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】根据下列实验现象所得结论正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 | 有气体生成,溶液未呈血红色 | 稀硝酸不能将Fe氧化为Fe3+ |
| B | 向NaAlO2溶液中滴入NaHCO3溶液 | 产生白色沉淀 | AlO2- 结合H+的能力比CO32-强 |
| C | 已知Cu2O+2H+=Cu2++Cu+H2O 将氢气还原氧化铜后所得红色固体 投入足量稀盐酸 | 溶液呈蓝色 | CuO的还原产物不全部是Cu |
| D | 将0.1mol•L-1 MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol•L-1CuSO4溶液 | 先有白色沉淀生成,后变为浅蓝色沉淀 | Cu(OH)2的溶度积比Mg(OH)2的大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】用H2还原mgCuO,当大部分固体变红时停止加热,冷却后称量,知残留固体质量为ng,共用去WgH2,则被还原的CuO的质量为
| A.40Wg | B.5(m-n)g | C.1.25ng | D.mg |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】硫酸铜晶体结晶水含量的测定结果,相对误差为-2.67%,其原因可能是
| A.实验时盛放硫酸铜晶体的容器未完全干燥 | B.加热过程中晶体有少量溅失 |
| C.硫酸铜晶体灼烧后有黑色物质出现 | D.晶体中有受热不反应不挥发的杂质 |
您最近一年使用:0次
【推荐2】固体化合物X由3种元素组成。某学习小组进行了如下实验:
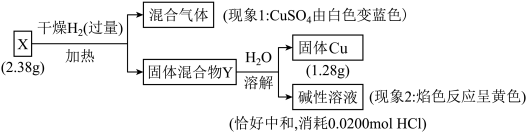
下列推断不正确 的是

下列推断
| A.由现象1得出化合物X含有O元素 |
B.X的化学式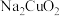 |
C.固体混合物Y的成分可能是 和 和 |
D.若X与浓盐酸反应产生氯气( )气体,则反应中X作氧化剂 )气体,则反应中X作氧化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】现有由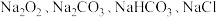 中的某几种组成的混合物,向其中加入足量的盐酸有气体放出,将气体通过足量的
中的某几种组成的混合物,向其中加入足量的盐酸有气体放出,将气体通过足量的 溶液,气体体积有所减少;将上述混合物在空气中加热,有气体放出。下列判断正确的是
溶液,气体体积有所减少;将上述混合物在空气中加热,有气体放出。下列判断正确的是
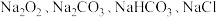 中的某几种组成的混合物,向其中加入足量的盐酸有气体放出,将气体通过足量的
中的某几种组成的混合物,向其中加入足量的盐酸有气体放出,将气体通过足量的 溶液,气体体积有所减少;将上述混合物在空气中加热,有气体放出。下列判断正确的是
溶液,气体体积有所减少;将上述混合物在空气中加热,有气体放出。下列判断正确的是A.混合物中一定不含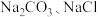 |
B.混合物中一定含有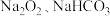 |
C.无法确定混合物中是否含有 |
D.混合物中一定不含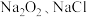 |
您最近一年使用:0次



