某工厂的工业废水中含有大量的FeSO4,较多的CuSO4和少量Na2SO4。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。
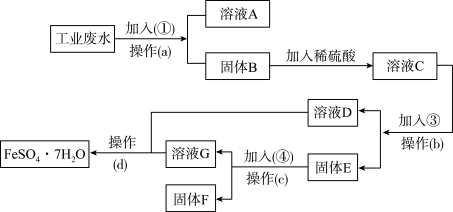
(1)加入的试剂①为______ (填化学式),加入试剂①的目的____________________ 。
(2)操作a的名称为过滤、洗涤,所需要的玻璃仪器为______ 。
(3)加入的试剂③为_______ (填化学式),发生的离子反应方程式为___________________________________________________ 。
(4)固体E的成分为_____ (填化学式),加入的试剂④为_____ (填化学式),发生的离子反应方程式为___________________________________________ 。
(5))从溶液D和溶液G中得到FeSO4•7H2O晶体的操作为蒸发浓缩、冷却结晶、______ 、洗涤、干燥。

(1)加入的试剂①为
(2)操作a的名称为过滤、洗涤,所需要的玻璃仪器为
(3)加入的试剂③为
(4)固体E的成分为
(5))从溶液D和溶液G中得到FeSO4•7H2O晶体的操作为蒸发浓缩、冷却结晶、
更新时间:2019-11-24 11:05:09
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl﹣、SO42﹣、和NO3﹣的分离.实验过程如下图所示:
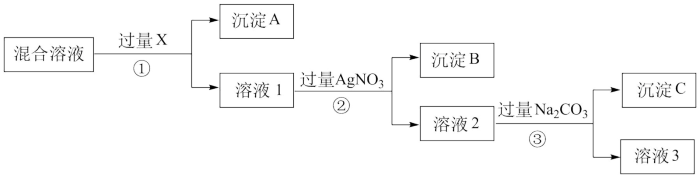
请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X:_______ ,沉淀A:_______ 。
(2)上述实验流程中加入过量的Na2CO3的目的是_______ 。
(3)按此实验方案得到的溶液3中肯定含有_______ (填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的_______ ,之后若要获得固体NaNO3需进行的实验操作是_______ (填操作名称)。

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X:
(2)上述实验流程中加入过量的Na2CO3的目的是
(3)按此实验方案得到的溶液3中肯定含有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物,试回答下列问题:

供选试剂:Na2SO4溶液、K2CO3溶液、K2SO4溶液、盐酸。
(1)操作①的名称是_________ 。
(2)试剂a是_________ ,试剂b 是_________ 。
(3)加入试剂a所发生反应的离子方程式为_________ 。加入试剂b所发生反应的离子方程式为_________ 。
(4)该方案能否达到实验目的:_____ (填“能”或“不能”)。若不能,应如何改进? _____ (若能,此问不用回答)。
(5)若要测定原混合物中BaCl2的质量分数,除了要准确称量混合物的质量外。至少还要获得的数据是_________ 的质量。

供选试剂:Na2SO4溶液、K2CO3溶液、K2SO4溶液、盐酸。
(1)操作①的名称是
(2)试剂a是
(3)加入试剂a所发生反应的离子方程式为
(4)该方案能否达到实验目的:
(5)若要测定原混合物中BaCl2的质量分数,除了要准确称量混合物的质量外。至少还要获得的数据是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】为了探究氯水能否和碳酸钡发生反应,某学生设计并完成了如下实验:
【实验一】向盛有饱和氯水的烧杯中加入足量碳酸钡,并充分搅拌,观察到氯水的黄绿色褪去并同时产生气体a。
【实验二】取实验一后烧杯中清液,分别进行如下实验:①往该清液中滴加盐酸时有大量气体产生,其主要成分为气体b;②往该清液中滴加硫酸钠溶液有白色沉淀产生;③将该清液滴在蓝色石蕊试纸上,试纸先变红后褪色。回答下列问题:
(1)写出气体的化学式:a___________ ,b___________
(2)在实验二中,清液使蓝色石蕊试纸先变红后褪色说明该清液中含有___________ (填化学式);清液中滴加硫酸钠溶液产生白色沉淀,该反应的离子方程式为___________ 。
(3)实验二中所得气体b可用右图所示装置净化。

①b中所含杂质气体为___________ (填化学式)。
②如果连接在该装置之后的另一活塞发生堵塞,则长颈漏斗中出现的现象为___________ 。
(4)写出产生气体b的反应的离子方程式___________ 。
(5)通过上述实验,可推知氯水和碳酸钡反应的化学方程式为___________ 。
【实验一】向盛有饱和氯水的烧杯中加入足量碳酸钡,并充分搅拌,观察到氯水的黄绿色褪去并同时产生气体a。
【实验二】取实验一后烧杯中清液,分别进行如下实验:①往该清液中滴加盐酸时有大量气体产生,其主要成分为气体b;②往该清液中滴加硫酸钠溶液有白色沉淀产生;③将该清液滴在蓝色石蕊试纸上,试纸先变红后褪色。回答下列问题:
(1)写出气体的化学式:a
(2)在实验二中,清液使蓝色石蕊试纸先变红后褪色说明该清液中含有
(3)实验二中所得气体b可用右图所示装置净化。

①b中所含杂质气体为
②如果连接在该装置之后的另一活塞发生堵塞,则长颈漏斗中出现的现象为
(4)写出产生气体b的反应的离子方程式
(5)通过上述实验,可推知氯水和碳酸钡反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】溴酸镉[Cd(BrO3)2]常用做分析试剂、生产荧光粉等。以镉铁矿(成分为CdO2、Fe2O3、FeO及少量的Al2O3和SiO2)为原料制备[Cd(BrO3)2]的工艺流程如下:

已知Cd(SO4)2溶于水,CdCO3难溶于水,请回答下列问题:
(1)Cd在周期表中位于第五周期第IIB族,则Cd元素的核电荷数是_______ 。
(2)为了提高酸浸速率,可以采取的措施是_____ (任写一种),滤渣1的化学式是______ 。
(3)还原镉时可产生使澄清石灰水变浑浊的气体,该反应的离子方程式为_______ 。
(4)为检验酸浸后溶液中是否含有Fe2+离子,可加入试剂X溶液,若有蓝色沉淀,则有Fe2+,X是_______ 。
(5)氧化步骤中需要加入H2O2的量比理论上明显要多,其可能原因为_______ 。
(6)调pH的目的是_______ 。
(7)沉镉所得的沉淀需进行洗涤,检验沉淀已经洗净的方法是_______ 。

已知Cd(SO4)2溶于水,CdCO3难溶于水,请回答下列问题:
(1)Cd在周期表中位于第五周期第IIB族,则Cd元素的核电荷数是
(2)为了提高酸浸速率,可以采取的措施是
(3)还原镉时可产生使澄清石灰水变浑浊的气体,该反应的离子方程式为
(4)为检验酸浸后溶液中是否含有Fe2+离子,可加入试剂X溶液,若有蓝色沉淀,则有Fe2+,X是
(5)氧化步骤中需要加入H2O2的量比理论上明显要多,其可能原因为
(6)调pH的目的是
(7)沉镉所得的沉淀需进行洗涤,检验沉淀已经洗净的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】高三老师设计了“Fe3+的氧化性实验探究”学案,课后选取一学生学案,其中部分内容如下。依据已有知识及学案相关内容。
回顾:Fe2+呈淡绿色、Fe3+呈棕黄色、Fe(OH)3胶体是红褐色液体。
提供资料:FeSO3是墨绿色沉淀
设置问题:Na2SO3溶液与FeCl3溶液反应猜想
猜提一:Na2SO3溶液与FeCl3溶液发生氧化还原反应;
猜想二:Na2SO3溶液与FeCl3溶液发生相互促进的水解反应,产生了Fe(OH)3胶体;
猜想三:_______。
(1)请将划线空白处补充完整_______ 。
问题探究:
(2)若猜想一正确,预测的实验现象是_______ ,反应的离子方程式为_______ 。
小组实验i:
现象记录:溶液黄色逐渐加深,最终得到红褐色溶液W
(3)观察实验现象证实猜想二合理,用红色激光笔照射该红褐色液体,预测的现象是_______ ;反应的离子方程式为_______ 。
(4)组织同学讨论:氧化还原反应是否发生,怎样检验。(归纳同学得出的检验方案)
方来①:取少量W液作,加铁氧化钾溶液,检验是否有Fe2+;
方来②:取少量W液伸,加酸性高锰酸钾漆液,检验是否有Fe2+;
方来③:取少量W液伸,加盐酸酸化,再加氯化钾溶液,检验是否有SO 。
。
你认为方案②_______ (填“合理”或“不合理”),理由是_______ 。
完善证据:
分组实验ⅱ:
现象记录:产生由色沉淀
分组实验ⅲ:取少量W液体,加铁氰化钾溶液,发现有蓝色沉淀生成。
探究结论:Fe3+与SO 的反应体系中,氧化还原反应与水解反应下仅共存而且存在竞争。
的反应体系中,氧化还原反应与水解反应下仅共存而且存在竞争。
回顾:Fe2+呈淡绿色、Fe3+呈棕黄色、Fe(OH)3胶体是红褐色液体。
提供资料:FeSO3是墨绿色沉淀
设置问题:Na2SO3溶液与FeCl3溶液反应猜想
猜提一:Na2SO3溶液与FeCl3溶液发生氧化还原反应;
猜想二:Na2SO3溶液与FeCl3溶液发生相互促进的水解反应,产生了Fe(OH)3胶体;
猜想三:_______。
(1)请将划线空白处补充完整
问题探究:
(2)若猜想一正确,预测的实验现象是
小组实验i:
| 装置 | 操作 |
 | 向2mLmol·L-1的FeCl3溶液中逐滴滴加1mLmol·L-1的Na2SO3溶液 |
(3)观察实验现象证实猜想二合理,用红色激光笔照射该红褐色液体,预测的现象是
(4)组织同学讨论:氧化还原反应是否发生,怎样检验。(归纳同学得出的检验方案)
方来①:取少量W液作,加铁氧化钾溶液,检验是否有Fe2+;
方来②:取少量W液伸,加酸性高锰酸钾漆液,检验是否有Fe2+;
方来③:取少量W液伸,加盐酸酸化,再加氯化钾溶液,检验是否有SO
 。
。你认为方案②
完善证据:
分组实验ⅱ:
| 装置 | 操作 |
 | 取1mLW液体于试管中,滴加过量盐酸,再滴加5滴BaCl溶液 |
分组实验ⅲ:取少量W液体,加铁氰化钾溶液,发现有蓝色沉淀生成。
探究结论:Fe3+与SO
 的反应体系中,氧化还原反应与水解反应下仅共存而且存在竞争。
的反应体系中,氧化还原反应与水解反应下仅共存而且存在竞争。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】某废旧金属材料含有Fe、Cu、Al、FeO、 、CuO和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收Al、Cu、绿矾等。
、CuO和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收Al、Cu、绿矾等。

回答下列问题:
(1)“焙烧”除了能将可燃性有机物除去外,还能___________ 。
(2)“碱浸”时反应的离子方程式是___________ 。
(3)制备金属铝时会向“滤液Ⅰ”通入一种过量的气体,此气体是___________ ,“滤渣Ⅱ”的成分是___________ 。
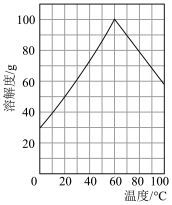
(4)绿矾溶解度曲线如图所示,操作Ⅲ包括___________ ,冷却至0℃结晶,过滤,少量冰水洗涤,低温干燥。
(5)绿矾往往会因为“操作Ⅲ”暴露在空气中而被氧化,为了解被氧化程度,质检小组按下列方法进行测定。取一定质量的产品溶于煮沸过的蒸馏水中,将所得溶液分为两等份。其中一份中加入 ,恰好使其中的
,恰好使其中的 离子完全沉淀;另一份加入42.5mL1mol/L氯水,恰好将其中的
离子完全沉淀;另一份加入42.5mL1mol/L氯水,恰好将其中的 完全氧化。
完全氧化。
①用“煮沸过的蒸馏水”溶解产品的目的是___________ 。
②测定实验中,可证明 被完全氧化的试剂为
被完全氧化的试剂为___________ ,现象是___________ 。
③产品中
___________ 。
 、CuO和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收Al、Cu、绿矾等。
、CuO和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收Al、Cu、绿矾等。
回答下列问题:
(1)“焙烧”除了能将可燃性有机物除去外,还能
(2)“碱浸”时反应的离子方程式是
(3)制备金属铝时会向“滤液Ⅰ”通入一种过量的气体,此气体是
(4)绿矾溶解度曲线如图所示,操作Ⅲ包括

(5)绿矾往往会因为“操作Ⅲ”暴露在空气中而被氧化,为了解被氧化程度,质检小组按下列方法进行测定。取一定质量的产品溶于煮沸过的蒸馏水中,将所得溶液分为两等份。其中一份中加入
 ,恰好使其中的
,恰好使其中的 离子完全沉淀;另一份加入42.5mL1mol/L氯水,恰好将其中的
离子完全沉淀;另一份加入42.5mL1mol/L氯水,恰好将其中的 完全氧化。
完全氧化。①用“煮沸过的蒸馏水”溶解产品的目的是
②测定实验中,可证明
 被完全氧化的试剂为
被完全氧化的试剂为③产品中

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】以印刷线路板的碱性蚀刻废液(主要成分为[Cu(NH3)4]Cl2)或焙烧过的铜精炼炉渣(主要成分为CuO、SiO2少量Fe2O3)为原料均能制备CuSO4·5H2O晶体。

(1)取一定量蚀刻废液和稍过量的NaOH溶液加入到如图所示实验装置的三颈瓶中,在搅拌下加热反应并通入空气,待产生大量的黑色沉淀时停止反应,趁热过滤、洗涤,得到CuO固体:所得固体经酸溶、结晶、过滤等操作,得到CuSO4·5H2O晶体。
①写出用蚀刻废液制备CuO反应的化学方程式______ 。
②检验CuO固体是否洗净的实验操作是______ 。
③装置图中装置X的作用是______ 。
(2)以焙烧过的铜精炼炉渣为原料制备CuSO4·5H2O晶体时,请补充完整相应的实验方案:取一定量培烧过的铜精炼炉渣,______ ,将滤液加热浓缩、冷却结晶、过滤、晾干,得到CuSO4·5H2O晶体。
已知:①SiO2属于酸性氧化物,不溶于盐酸或硫酸溶液;
②该实验中pH=3.2时,Fe3+完全沉淀:pH=4.7时,Cu2+开始沉淀;
③实验中可选用的试剂:1.0mol·L-1H2SO4、1.0mol·L-1HCl、1.0mol·L-1NaOH。

(1)取一定量蚀刻废液和稍过量的NaOH溶液加入到如图所示实验装置的三颈瓶中,在搅拌下加热反应并通入空气,待产生大量的黑色沉淀时停止反应,趁热过滤、洗涤,得到CuO固体:所得固体经酸溶、结晶、过滤等操作,得到CuSO4·5H2O晶体。
①写出用蚀刻废液制备CuO反应的化学方程式
②检验CuO固体是否洗净的实验操作是
③装置图中装置X的作用是
(2)以焙烧过的铜精炼炉渣为原料制备CuSO4·5H2O晶体时,请补充完整相应的实验方案:取一定量培烧过的铜精炼炉渣,
已知:①SiO2属于酸性氧化物,不溶于盐酸或硫酸溶液;
②该实验中pH=3.2时,Fe3+完全沉淀:pH=4.7时,Cu2+开始沉淀;
③实验中可选用的试剂:1.0mol·L-1H2SO4、1.0mol·L-1HCl、1.0mol·L-1NaOH。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】图1是氯碱工业中离子交换膜电解槽示意图,其中离子交换膜是“阳离子交换膜”,它有一特殊的性质——只允许阳离子通过而阻止阴离子和气体通过。
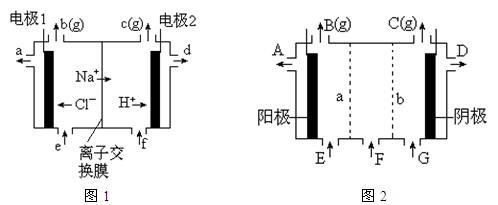
⑴、工业食盐含Ca2+、Mg2+等杂质。精制过程发生反应的离子方程式为_____ ,_____ 。
⑵、如果粗盐中SO 含量较高,必须添加钡式剂除去SO
含量较高,必须添加钡式剂除去SO ,该钡试剂可以是
,该钡试剂可以是______ 。
A.Ba(OH)2B.Ba(NO3)2C.BaCl2
⑶、为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为_______ 。
A.先加NaOH,后加Na2CO3,再加钡试剂
B.先加NaOH,后加钡试剂,再加Na2CO3
C.先加钡试剂,后加NaOH,再加Na2CO3
⑷、电解后得到的氢氧化钠溶液从______ 口流出,b口排出的是_______ 气体,电极1应连接电源的
_______ 极(填“正”或“负”极);理论上讲,从f口加入纯水即可,但实际生产中,纯水中要加入一定量的NaOH溶液,其原因是_______ 。
⑸、图2是根据氯碱工业中离子交换膜技术原理,设计的电解Na2SO4溶液生产NaOH和H2SO4溶液的装置。请回答:
①、a为_______ (填“阳”、“阴”)离子交换膜。
②、阳极的电极反应式是_______ 。
③、从D、E口流出或流进的物质的化学式分别为_______ ,_______ 。

⑴、工业食盐含Ca2+、Mg2+等杂质。精制过程发生反应的离子方程式为
⑵、如果粗盐中SO
 含量较高,必须添加钡式剂除去SO
含量较高,必须添加钡式剂除去SO ,该钡试剂可以是
,该钡试剂可以是A.Ba(OH)2B.Ba(NO3)2C.BaCl2
⑶、为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为
A.先加NaOH,后加Na2CO3,再加钡试剂
B.先加NaOH,后加钡试剂,再加Na2CO3
C.先加钡试剂,后加NaOH,再加Na2CO3
⑷、电解后得到的氢氧化钠溶液从
⑸、图2是根据氯碱工业中离子交换膜技术原理,设计的电解Na2SO4溶液生产NaOH和H2SO4溶液的装置。请回答:
①、a为
②、阳极的电极反应式是
③、从D、E口流出或流进的物质的化学式分别为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】用软锰矿[主要成分MnO2,还含SiO2 、Fe2O3、Al2O3、Cu2(OH)2CO3的等杂质]和酸洗厂废酸液(含1mol/LH2SO4的FeSO4溶液)联合生产硫酸锰和铁红(Fe2O3)生产过程如下

(1)含杂质的软锰矿使用前需将其粉碎,目的是______ 。
(2)滤渣1中含有的主要物质是_______ 。
(3)滤液1中,加氨水调控溶液pH至3.2,通入O2,反应的离子方程式是_______ 。若用H2O2代替O2,是否合理?理由是___________ 。
(4)软锰矿粉与硫酸和硫酸亚铁溶液反应的离子方程式是_________ 。
(5)滤液3中加入难溶电解质MnS的目的是(用离子方程式表示)_________ 。
(6)用重结晶法从滤液4中获取硫酸锰晶体的操作是:__________ 。

| Mn(OH)2 | Fe(OH)2 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | |
| 开始沉淀时 | 8.3 | 6.3 | 4.7 | 3.4 | 2.7 |
| 完全沉淀时 | 9.8 | 8.3 | 6.7 | 4.4 | 3.2 |
(1)含杂质的软锰矿使用前需将其粉碎,目的是
(2)滤渣1中含有的主要物质是
(3)滤液1中,加氨水调控溶液pH至3.2,通入O2,反应的离子方程式是
(4)软锰矿粉与硫酸和硫酸亚铁溶液反应的离子方程式是
(5)滤液3中加入难溶电解质MnS的目的是(用离子方程式表示)
(6)用重结晶法从滤液4中获取硫酸锰晶体的操作是:
您最近一年使用:0次



