有五瓶损坏标签的试剂,分别盛有AgNO3溶液、稀硝酸、盐酸、氯化钡溶液、碳酸钾溶液,为了确定各瓶中是什么试剂,将它们任意编号为A、B、C、D、E,用小试管各盛少量多次进行两两混合反应,反应现象为:A与B、A与E均可产生白色沉淀,其中A与B反应所产生沉淀不溶于酸,A与E反应所生成的白色沉淀可以溶于C或D;B与D、B与E产生沉淀;E与C、E与D反应均可产生二氧化碳气体;而C与D由于属于同一类物质,混合时无反应现象。
由此,可判定各试剂瓶中所盛试剂为(用化学式表示)
A________ ;B________ ;C________ ;D________ ;E________ 。
另外,请写出下面要求的离子方程式:
(1)A与E:
________________________________________________________ 。
(2)A与B:
_________________________________________________________ 。
(3)C与E:
__________________________________________________________ 。
由此,可判定各试剂瓶中所盛试剂为(用化学式表示)
A
另外,请写出下面要求的离子方程式:
(1)A与E:
(2)A与B:
(3)C与E:
更新时间:2019-11-25 19:57:19
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】有一包白色固体,可能含氯化钠、碳酸钠、硫酸钠、氢氧化钠、氢氧化钡中的一种或几种。某兴趣小组为探究其成分做了以下实验:
实验一:探究固体的组成。

(1)向固体样品中加入过量稀硝酸,产生的气体是
(2)生成白色滤渣甲反应的化学方程式为
(3)原固体中一定不含有的物质是
实验二:利用滤液A进一步探究固体中是否含氯化钠(方案如下图),最终得出结论:原固体中一定含NaCl。
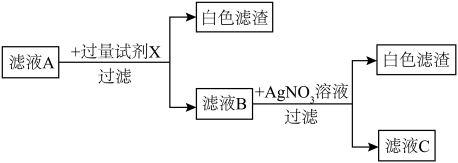
(4)试剂X是
(5)滤液C中除含
 外,一定还含有的溶质是
外,一定还含有的溶质是
您最近半年使用:0次
【推荐2】现有一包固体粉末,其中可能含有如下五种物质:CaCO3、K2CO3、Na2SO4、NaCl、CuSO4。现进行如下实验:①溶于水得无色溶液,溶液中无沉淀出现;②向溶液中加入BaCl2溶液生成白色沉淀,再加盐酸时沉淀消失。根据上述实验现象推断:
(1)一定不存在的物质是___________ ;
(2)写出加入盐酸时沉淀消失的离子反应方程式___________ ;
(3)可能存在的物质是___________ ;
(4)用化学反应的现象来检验可能存在的物质所用试剂为:__________ ;若不使用化学试剂还可用_________ 来检验该物质的存在。
(1)一定不存在的物质是
(2)写出加入盐酸时沉淀消失的离子反应方程式
(3)可能存在的物质是
(4)用化学反应的现象来检验可能存在的物质所用试剂为:
您最近半年使用:0次
【推荐3】某无色、澄清溶液中可能含有Na+、Cl-、 、
、 、Fe3+、OH-、
、Fe3+、OH-、 中的几种,依次进行下列实验,观察到的现象如下:
中的几种,依次进行下列实验,观察到的现象如下:
已知:2Al+2OH-+2H2O=2 +3H2↑。
+3H2↑。
(1)不需要通过实验就能判断原溶液中肯定没有_______ 离子,肯定有_______ 离子。
(2)写出Ⅲ中发生的反应的离子方程式_______ 。
(3)原溶液中可能存在_______ 离子,验证溶液中是否存在此离子的实验方法_______ 。
(4)若(2)中的离子不存在,则溶液中一定存在的阴离子_______ 。
 、
、 、Fe3+、OH-、
、Fe3+、OH-、 中的几种,依次进行下列实验,观察到的现象如下:
中的几种,依次进行下列实验,观察到的现象如下:已知:2Al+2OH-+2H2O=2
 +3H2↑。
+3H2↑。| 步骤 | 操作 | 现象 |
| Ⅰ | 取少量溶液,向其中加入适量铝粉 | 有气体生成 |
| Ⅱ | 另取少量溶液,向其中滴加足量BaCl2溶液 | 有白色沉淀生成 |
| Ⅲ | 向Ⅱ中滴加足量稀盐酸 | 沉淀部分溶解 |
(2)写出Ⅲ中发生的反应的离子方程式
(3)原溶液中可能存在
(4)若(2)中的离子不存在,则溶液中一定存在的阴离子
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】有一瓶澄清的溶液,其中可能含有NH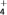 、K+、Mg2+、Ba2+、Al3+、Fe3+、SO42-、CO32-、NO3-、I-、Cl-,取该溶液进行以下实验:
、K+、Mg2+、Ba2+、Al3+、Fe3+、SO42-、CO32-、NO3-、I-、Cl-,取该溶液进行以下实验:
①用pH试纸测得该溶液呈酸性;
②取部分溶液,加入数滴新制的氯水及少量CCl4,经振荡、静置后,CCl4层呈紫红色;
③另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐变为碱性,在整个滴加过程中无沉淀生成;
④取部分上述碱性溶液,加入Na2CO3溶液,有白色沉淀生成;
⑤将③得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验事实回答问题:
(1)写出②所发生反应的离子方程式_________ 。
(2)该溶液中肯定存在的离子是________ 。
(3)该溶液中肯定不存在的离子是________ 。
(4)该溶液中还不能确定是否存在的离子是_________ 。
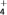 、K+、Mg2+、Ba2+、Al3+、Fe3+、SO42-、CO32-、NO3-、I-、Cl-,取该溶液进行以下实验:
、K+、Mg2+、Ba2+、Al3+、Fe3+、SO42-、CO32-、NO3-、I-、Cl-,取该溶液进行以下实验:①用pH试纸测得该溶液呈酸性;
②取部分溶液,加入数滴新制的氯水及少量CCl4,经振荡、静置后,CCl4层呈紫红色;
③另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐变为碱性,在整个滴加过程中无沉淀生成;
④取部分上述碱性溶液,加入Na2CO3溶液,有白色沉淀生成;
⑤将③得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验事实回答问题:
(1)写出②所发生反应的离子方程式
(2)该溶液中肯定存在的离子是
(3)该溶液中肯定不存在的离子是
(4)该溶液中还不能确定是否存在的离子是
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】Ⅰ.以黄铁矿(主要成分FeS2)为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。
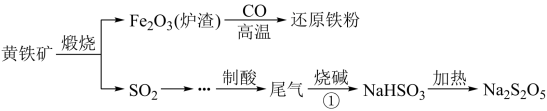
(1)黄铁矿中硫元素的化合价为___________ ;
(2)欲得到更纯的NaHSO3,反应①应通入___________ (填 “过量”或“不足量”)的SO2气体;
(3)因为Na2S2O5具有还原性,导致商品Na2S2O5中不可避免地存在Na2SO4,检验其中含有SO 的方法是
的方法是___________ 。
Ⅱ.黄铁矿煅烧后得到的炉渣(含Fe2O3、FeO、SiO2及Al2O3),还可以用来生产一种高效混凝剂聚合硫酸铁铝硅,工艺流程如下:

已知:mCaO·nAl2O3难溶于水。
(4)“过滤”所得滤渣为___________ (填化学式);
(5)“氧化”时发生反应的离子方程式为___________ ;
(6)“调节碱化度”时,mCaO·nAl2O3与溶液中H+反应的离子方程式为___________ 。

(1)黄铁矿中硫元素的化合价为
(2)欲得到更纯的NaHSO3,反应①应通入
(3)因为Na2S2O5具有还原性,导致商品Na2S2O5中不可避免地存在Na2SO4,检验其中含有SO
 的方法是
的方法是Ⅱ.黄铁矿煅烧后得到的炉渣(含Fe2O3、FeO、SiO2及Al2O3),还可以用来生产一种高效混凝剂聚合硫酸铁铝硅,工艺流程如下:

已知:mCaO·nAl2O3难溶于水。
(4)“过滤”所得滤渣为
(5)“氧化”时发生反应的离子方程式为
(6)“调节碱化度”时,mCaO·nAl2O3与溶液中H+反应的离子方程式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有一包白色固体粉末,其中可能含有NaCl、Ba(NO3)2、CuSO4、Na2CO3中的一种或几种,现做以下实验:
①取少量白色固体粉末于烧杯中,加水搅拌,有白色不溶物生成,过滤,滤液无色透明。
②取①的白色不溶物少量于试管中,加入足量稀硝酸,固体完全溶解,并有无色气泡产生。
③取①所得的滤液2mL于试管中,滴入几滴稀硫酸,有白色沉淀产生。
④另取①得到的无色透明溶液少量于试管中,加入足量硝酸酸化的AgNO3溶液,产生白色沉淀。
根据上述实验事实,回答下列问题:
(1)原白色粉末中一定含有的物质是___________ (写化学式,下同),一定不含有的物质是___________ 。
(2)写出各步变化的离子方程式。
①___________ ;
②___________ ;
③___________ ;
④___________ 。
①取少量白色固体粉末于烧杯中,加水搅拌,有白色不溶物生成,过滤,滤液无色透明。
②取①的白色不溶物少量于试管中,加入足量稀硝酸,固体完全溶解,并有无色气泡产生。
③取①所得的滤液2mL于试管中,滴入几滴稀硫酸,有白色沉淀产生。
④另取①得到的无色透明溶液少量于试管中,加入足量硝酸酸化的AgNO3溶液,产生白色沉淀。
根据上述实验事实,回答下列问题:
(1)原白色粉末中一定含有的物质是
(2)写出各步变化的离子方程式。
①
②
③
④
您最近半年使用:0次



