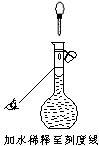
(1)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A 萃取分液 B 升华 C 结晶 D 过滤 E 蒸馏 F 分液
①分离饱和食盐水与沙子的混合物______ ;
②从硝酸钾和氯化钠的混合液中获得硝酸钾______ ;
③从碘水中提取碘单质______ ;
④分离水和汽油的混合物______ ;
⑤分离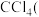 沸点为
沸点为 和甲苯
和甲苯 沸点为
沸点为 的混合物
的混合物______ 。
(2)0.4 mol某气体的体积为9.8L,则该气体的气体摩尔体积为_____ 。
(3)标准状况下,测得1.92克某气体的体积为672mL,则此气体的相对分子质量为___ 。
(4)实验室用Na2CO3·10H2O晶体配制0. 5mol/L的Na2CO3溶液970mL,应用托盘天平称取Na2CO3·10H2O的质量是____ 。
(5)已知两种碱AOH和BOH的摩尔质量之比为5:7,现将7mol AOH与5mol BOH混合后,从中取出5.6g,恰好可以中和100ml浓度为1.2mol/L的盐酸,则AOH的摩尔质量为_____ 。
(6)某学生欲用12mol·L-1浓盐酸和蒸馏水配制500 mL 0.3 mol·L-1的稀盐酸。
①该学生需要用量筒量取____ mL上述浓盐酸进行配制。
②下列实验操作会导致所配制的稀盐酸的物质的量浓度偏小的是____ (填序号)。
a 用量筒量取浓盐酸时俯视观察凹液面
b 将量取浓盐酸的量筒进行洗涤,并将洗涤液转移到容量瓶中
c 稀释浓盐酸时,未冷却到室温即转移到容量瓶中
d 定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
e 容量瓶洗涤干净后未干燥
A 萃取分液 B 升华 C 结晶 D 过滤 E 蒸馏 F 分液
①分离饱和食盐水与沙子的混合物
②从硝酸钾和氯化钠的混合液中获得硝酸钾
③从碘水中提取碘单质
④分离水和汽油的混合物
⑤分离
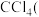 沸点为
沸点为 和甲苯
和甲苯 沸点为
沸点为 的混合物
的混合物(2)0.4 mol某气体的体积为9.8L,则该气体的气体摩尔体积为
(3)标准状况下,测得1.92克某气体的体积为672mL,则此气体的相对分子质量为
(4)实验室用Na2CO3·10H2O晶体配制0. 5mol/L的Na2CO3溶液970mL,应用托盘天平称取Na2CO3·10H2O的质量是
(5)已知两种碱AOH和BOH的摩尔质量之比为5:7,现将7mol AOH与5mol BOH混合后,从中取出5.6g,恰好可以中和100ml浓度为1.2mol/L的盐酸,则AOH的摩尔质量为
(6)某学生欲用12mol·L-1浓盐酸和蒸馏水配制500 mL 0.3 mol·L-1的稀盐酸。
①该学生需要用量筒量取
②下列实验操作会导致所配制的稀盐酸的物质的量浓度偏小的是
a 用量筒量取浓盐酸时俯视观察凹液面
b 将量取浓盐酸的量筒进行洗涤,并将洗涤液转移到容量瓶中
c 稀释浓盐酸时,未冷却到室温即转移到容量瓶中
d 定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
e 容量瓶洗涤干净后未干燥
更新时间:2019-11-29 22:14:48
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某学校化学兴趣小组从文献资料上获得如下信息: 在潮湿空气中会缓慢分解成
在潮湿空气中会缓慢分解成 、
、 和
和 。为了验证这一信息,该兴趣小组将一瓶在潮湿空气中久置的
。为了验证这一信息,该兴趣小组将一瓶在潮湿空气中久置的 样品混合均匀后,进行如下实验:
样品混合均匀后,进行如下实验:
(1)在一个质量为ag的蒸发皿中加入一些样品,称得总质量为bg。用酒精灯对其充分加热,冷却后称得其总质量为cg。残留在蒸发皿中的固体是_______ (填化学式)。
(2)另取相同质量的样品放入锥形瓶中,实验装置如下图所示。为了保证实验成功,所选用针筒的最大刻度值应大于_______ mL。(设实验在标准状况下进行)
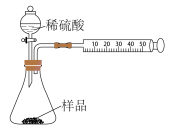
(3)打开活塞逐滴加入稀硫酸,直至没有气泡产生为止。针筒中收集到的气体体积折算成标准状况下的体积为 (滴入稀硫酸的体积及针筒活塞与内壁的摩擦力忽略不计)。该兴趣小组设称取的每份样品中
(滴入稀硫酸的体积及针筒活塞与内壁的摩擦力忽略不计)。该兴趣小组设称取的每份样品中 、
、 的物质的量分别为x、y,且没有利用化学方程式进行计算,就列出算式,
的物质的量分别为x、y,且没有利用化学方程式进行计算,就列出算式, ,他们依据的原理是
,他们依据的原理是_______ 。
 在潮湿空气中会缓慢分解成
在潮湿空气中会缓慢分解成 、
、 和
和 。为了验证这一信息,该兴趣小组将一瓶在潮湿空气中久置的
。为了验证这一信息,该兴趣小组将一瓶在潮湿空气中久置的 样品混合均匀后,进行如下实验:
样品混合均匀后,进行如下实验:(1)在一个质量为ag的蒸发皿中加入一些样品,称得总质量为bg。用酒精灯对其充分加热,冷却后称得其总质量为cg。残留在蒸发皿中的固体是
(2)另取相同质量的样品放入锥形瓶中,实验装置如下图所示。为了保证实验成功,所选用针筒的最大刻度值应大于

(3)打开活塞逐滴加入稀硫酸,直至没有气泡产生为止。针筒中收集到的气体体积折算成标准状况下的体积为
 (滴入稀硫酸的体积及针筒活塞与内壁的摩擦力忽略不计)。该兴趣小组设称取的每份样品中
(滴入稀硫酸的体积及针筒活塞与内壁的摩擦力忽略不计)。该兴趣小组设称取的每份样品中 、
、 的物质的量分别为x、y,且没有利用化学方程式进行计算,就列出算式,
的物质的量分别为x、y,且没有利用化学方程式进行计算,就列出算式, ,他们依据的原理是
,他们依据的原理是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】Ⅰ.铁是生产、生活及生命中的重要元素。
(1)现有一瓶放置了一段时间的某浓度的FeCl2溶液,请设计实验检验其中是否含有Fe3+:__ 。
(2)普通铁粉与水蒸气在高温下反应生成铁的某种氧化物和氢气,该氧化物和氢气在高温下发生逆反应得到“引火铁”。若一定量的普通铁粉和水蒸气在高温下反应生成33.6LH2(已换算到标况下),则转移电子数目为____ ;“引火铁”是一种极细的铁粉,它在空气中可以自燃,其原因是____ 。
Ⅱ.化合物M是某种具有磁学性质的新型电子材料的主要成分,由两种元素组成。为了研究其组成,设计如图实验:
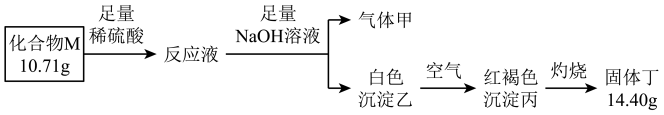
气体甲可使湿润红色石蕊试纸变蓝。请回答:
(3)白色沉淀乙在空气中变成红褐色沉淀丙的原因是(用化学方程式表示)___ 。
(4)M的化学式为___ 。
(5)高温条件下,丁与甲反应生成两种单质和水,该反应的化学方程式为___ 。
(1)现有一瓶放置了一段时间的某浓度的FeCl2溶液,请设计实验检验其中是否含有Fe3+:
(2)普通铁粉与水蒸气在高温下反应生成铁的某种氧化物和氢气,该氧化物和氢气在高温下发生逆反应得到“引火铁”。若一定量的普通铁粉和水蒸气在高温下反应生成33.6LH2(已换算到标况下),则转移电子数目为
Ⅱ.化合物M是某种具有磁学性质的新型电子材料的主要成分,由两种元素组成。为了研究其组成,设计如图实验:

气体甲可使湿润红色石蕊试纸变蓝。请回答:
(3)白色沉淀乙在空气中变成红褐色沉淀丙的原因是(用化学方程式表示)
(4)M的化学式为
(5)高温条件下,丁与甲反应生成两种单质和水,该反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A是一种重要的有机化工原料,其产量通常用来衡量一个国家的石油化学工业发展水平,通过一系列化学反应,可以制得成千上万种有用的物质。结合下图物质间转化关系回答问题。
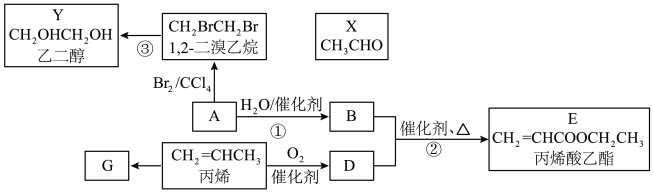
(1)A结构简式为_______ 。
(2)③的反应类型为_______ ,E中的含氧官能团名称是_______ 。
(3)高分子化合物G是一种常见的合成纤维——丙纶,其结构简式为_______ 。
(4)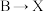 的反应所需的试剂与条件为
的反应所需的试剂与条件为_______ 。
(5)写出下列反应的化学方程式:
步骤①_______ ;
步骤②_______ 。
(6)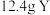 与足量的金属
与足量的金属 完全反应,生成标准状况下氢气的体积为
完全反应,生成标准状况下氢气的体积为_______ L。

(1)A结构简式为
(2)③的反应类型为
(3)高分子化合物G是一种常见的合成纤维——丙纶,其结构简式为
(4)
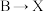 的反应所需的试剂与条件为
的反应所需的试剂与条件为(5)写出下列反应的化学方程式:
步骤①
步骤②
(6)
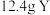 与足量的金属
与足量的金属 完全反应,生成标准状况下氢气的体积为
完全反应,生成标准状况下氢气的体积为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】三盐(3PbO·PbSO4·H2O,相对分子质量为990)可用作聚氯乙烯的热稳定剂, 不溶于水。以200.0t铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如下图所示。
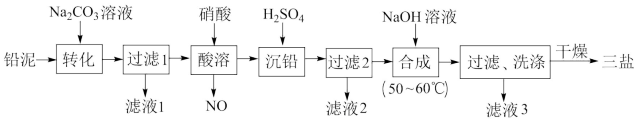
已知:Ksp(PbSO4)=1.82×l0-8;Ksp(PbCO3)=l.46×l0-13。
回答下列问题:
(1)加Na2CO3溶液转化的目的是_________ .
(2)酸溶时,不直接使用H2SO4溶液的原因可能是________ ;铅与硝酸在酸溶过程中发生反应的离子方程式为__________ .
(3)流程中可循环利用的物质是_________ ;洗涤操作时,检验沉淀是否洗涤干净的方法是________ 。
(4)当沉淀转化达平衡时,滤液l中c(SO42-)与c(CO32-)的比值为_____________ 。
(5) 50-60℃时合成三盐的化学方程式为______ ;若得到纯净干燥的三盐99.0t,假设铅泥中的铅元素有80%转化为三盐,则铅泥中铅元素的质量分数为_________ 。

已知:Ksp(PbSO4)=1.82×l0-8;Ksp(PbCO3)=l.46×l0-13。
回答下列问题:
(1)加Na2CO3溶液转化的目的是
(2)酸溶时,不直接使用H2SO4溶液的原因可能是
(3)流程中可循环利用的物质是
(4)当沉淀转化达平衡时,滤液l中c(SO42-)与c(CO32-)的比值为
(5) 50-60℃时合成三盐的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】自然资源的开发利用,金属铼(Re)是重要的新兴金属,应用于国防、石油化工以及电子制造等领域,通过还原高铼酸铵(NH4ReO4)可制取金属铼。以钼精矿(主要成分为钼的硫化物和少量铼的硫化物)制取高铼酸铵的流程如下图所示。回答下列问题:
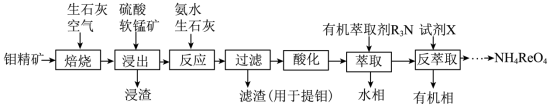
(1)“焙烧”过程加入生石灰的目的___________ 。
(2)“浸出”中,浸出率与温度的关系如下左图所示,浸出率与硫酸浓度的关系如下图所示。工业生产应选择的适宜条件是___________ 。

(3)“萃取”机理为: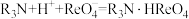 ,则“反萃取”对应的离子方程式为
,则“反萃取”对应的离子方程式为___________ 。
(4)硫酸铼(Ⅳ)铵[(NH4)aReb(SO4)c·mH2O]是制备高纯铼的基础产品,为测定其组成进行如下实验:
①称取3.300g样品配成100mL溶液M。
②取10.00mL溶液M,用0.05mol/L的BaCl2标准溶液滴定,恰好完全沉淀,进行三次平行实验,平均消耗40.00mLBaCl2标准溶液。
③另取10.00mL溶液M,加足量浓NaOH溶液并加热,生成标准状况下气体44.80mL。
通过计算可知铼的物质的量为___________ ,确定硫酸铼铵的化学式为___________ 。

(1)“焙烧”过程加入生石灰的目的
(2)“浸出”中,浸出率与温度的关系如下左图所示,浸出率与硫酸浓度的关系如下图所示。工业生产应选择的适宜条件是

(3)“萃取”机理为:
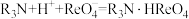 ,则“反萃取”对应的离子方程式为
,则“反萃取”对应的离子方程式为(4)硫酸铼(Ⅳ)铵[(NH4)aReb(SO4)c·mH2O]是制备高纯铼的基础产品,为测定其组成进行如下实验:
①称取3.300g样品配成100mL溶液M。
②取10.00mL溶液M,用0.05mol/L的BaCl2标准溶液滴定,恰好完全沉淀,进行三次平行实验,平均消耗40.00mLBaCl2标准溶液。
③另取10.00mL溶液M,加足量浓NaOH溶液并加热,生成标准状况下气体44.80mL。
通过计算可知铼的物质的量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】目前,世界上生产的镁有60%来自海水,其生产流程图如下:
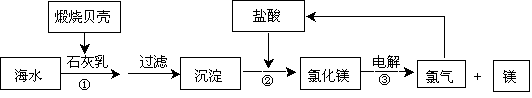
(1)贝壳的主要化学成分为____________________ (写化学式)。
(2)写出反应②的离子方程式_____________________________________ 。
(3)写出Mg与CO2反应的化学方程式__________________________________________ 。
(4)电解熔融氯化镁制取金属镁,若有0.4 mol电子发生转移,理论上能得到金属镁的质量是________________ 。

(1)贝壳的主要化学成分为
(2)写出反应②的离子方程式
(3)写出Mg与CO2反应的化学方程式
(4)电解熔融氯化镁制取金属镁,若有0.4 mol电子发生转移,理论上能得到金属镁的质量是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室用63%的浓HNO3(其密度为1.4g·mL-1)配制240mL0.50mol·L-1稀HNO3,若实验仪器有:
A.10mL量筒 B.50mL量筒 C.托盘天平 D.玻璃棒 E.100mL容量瓶 F.250mL容量瓶 G.500mL容量瓶 H.胶头滴管 I.200mL烧杯
(1)此浓硝酸的物质的量浓度为___ 。
(2)应量取63%的浓硝酸___ mL,应选用____ (填仪器的字母编号)。
(3)实验时还需选用的仪器有D、I、___ (填序号)。
(4)配制过程中,下列操作会使配制的稀硝酸溶液浓度偏高的是(填序号)___ 。
①量取过浓硝酸的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③溶解后未经冷却就移液
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
A.10mL量筒 B.50mL量筒 C.托盘天平 D.玻璃棒 E.100mL容量瓶 F.250mL容量瓶 G.500mL容量瓶 H.胶头滴管 I.200mL烧杯
(1)此浓硝酸的物质的量浓度为
(2)应量取63%的浓硝酸
(3)实验时还需选用的仪器有D、I、
(4)配制过程中,下列操作会使配制的稀硝酸溶液浓度偏高的是(填序号)
①量取过浓硝酸的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③溶解后未经冷却就移液
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某同学按下列步骤配制480 mL 0.20 mol·L-1NaCl溶液,请回答有关问题。
(6)你认为按上述步骤配制的NaCl溶液的浓度是否为0.200 mol·L-1,请说明理由。__________________________
| 实验步骤 | 有关问题 |
| (1)计算所需NaCl的质量 | 需要NaCl的质量为 |
| (2)称量NaCl固体 | 称量过程中主要用到的仪器是 |
| (3)将NaCl加入 | 为加快溶解,可采取的措施是 |
| (4)将溶液完全转移至 | 为防止溶液溅出,应该采取的措施是 |
| (5)向容量瓶中加蒸馏水至 | 在进行此操作时应注意的问题是 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】下列A、B、C、D是中学常见的混合物分离或提纯的基本装置。
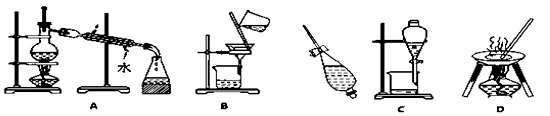
请根据混合物分离或提纯原理,回答在下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。
(1)除去Ca(OH)2溶液中悬浮的CaCO3___________ ;(2)用自来水制取蒸馏水 ___________ ;(3)分离植物油和水 ___________ ;(4)与海水晒盐原理相符的是 ___________ 。

请根据混合物分离或提纯原理,回答在下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。
(1)除去Ca(OH)2溶液中悬浮的CaCO3
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】观察下面实验装置图,回答有关问题。
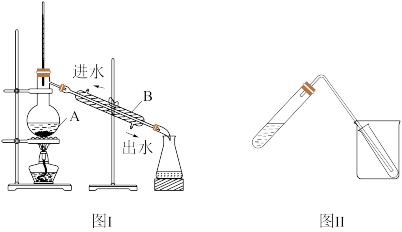
(1)图Ⅰ是实验室制取蒸馏水的常用装置,图中明显的错误是__________ 。
(2)仪器A的名称是_________ ,仪器B的名称是_________ 。
(3)实验时A中除加入一定量自来水外,还需加入少量_______ ,其作用是_______ 。
(4)图Ⅱ装置也可用于少量蒸馏水的制取(加热及固定仪器略),其原理与图Ⅰ相同。该装置中使用的玻璃导管较长,其作用是___________ 。

(1)图Ⅰ是实验室制取蒸馏水的常用装置,图中明显的错误是
(2)仪器A的名称是
(3)实验时A中除加入一定量自来水外,还需加入少量
(4)图Ⅱ装置也可用于少量蒸馏水的制取(加热及固定仪器略),其原理与图Ⅰ相同。该装置中使用的玻璃导管较长,其作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】锰酸钾在化工生产中应用广泛,实验室制备高锰酸钾方法如下:
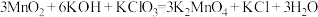 ,
,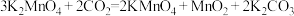 。
。
Ⅰ.制备锰酸钾溶液
称取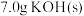 和
和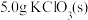 放入容器A中,加热,待混合物熔融后,加入
放入容器A中,加热,待混合物熔融后,加入
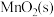 ,待反应物干涸后,加大火焰强热4-8 min,得墨绿色的锰酸钾,待物料冷却后,用
,待反应物干涸后,加大火焰强热4-8 min,得墨绿色的锰酸钾,待物料冷却后,用 溶液重复浸取,合并浸取液便得墨绿色的锰酸钾溶液。
溶液重复浸取,合并浸取液便得墨绿色的锰酸钾溶液。
Ⅱ.锰酸钾的歧化
在浸取液中通入适量 气体,使
气体,使 歧化为
歧化为 和
和 ,歧化完全后把溶液加热,趁热抽滤,滤去
,歧化完全后把溶液加热,趁热抽滤,滤去 残渣。
残渣。
Ⅲ.结晶
把滤液移至蒸发皿内,蒸发浓缩,停止加热,冷却结晶,抽滤、洗涤、干燥、称量至恒重.计算产率。
IV.纯度测定
称取制得的高锰酸钾产品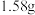 ,配成
,配成 溶液,用移液管量取
溶液,用移液管量取 待测液,选择
待测液,选择 滴定管,用
滴定管,用 草酸钠标准溶液进行滴定,发生反应
草酸钠标准溶液进行滴定,发生反应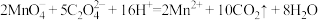 ,重复测定三次,计算纯度。
,重复测定三次,计算纯度。
请回答下列问题:
(1)步骤Ⅰ中仪器A可选用_______ 。
①蒸发皿 ②瓷坩埚 ③烧杯 ④铁坩埚

(2)已知 、
、 、
、 溶解度随温度变化曲线如图,步骤Ⅱ中
溶解度随温度变化曲线如图,步骤Ⅱ中 不能通得过多的原因是
不能通得过多的原因是___________ 。
(3)步骤Ⅱ中检验 歧化完全的实验方法是
歧化完全的实验方法是______________ 。
(4)步骤Ⅲ中有关说法正确的是_________ 。
A.为得到较大晶体颗粒,宜用冰水浴冷却结晶
B.蒸发浓缩至溶液表面出现晶膜时,停止加热
C.本实验应采用低温干燥的方法来干燥产品
D.放入比布氏漏斗内径略小的滤纸后,用蒸馏水润湿,微开水龙头使滤纸紧贴瓷板
(5)步骤Ⅳ配制高锰酸钾溶液时必须使用到的仪器的先后顺序为_____________ 。
a. 容量瓶 b.
容量瓶 b. 容量瓶 c.玻璃棒 d.烧杯 e.电子天平 f.胶头滴管 g.量筒
容量瓶 c.玻璃棒 d.烧杯 e.电子天平 f.胶头滴管 g.量筒
(6) 若移液管用蒸馏水洗净干燥后没有用待测液润洗就进行后面的实验,将___________ (填“偏大”“偏小”或“不变”)。
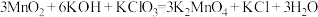 ,
,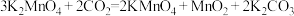 。
。Ⅰ.制备锰酸钾溶液
称取
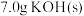 和
和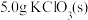 放入容器A中,加热,待混合物熔融后,加入
放入容器A中,加热,待混合物熔融后,加入
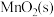 ,待反应物干涸后,加大火焰强热4-8 min,得墨绿色的锰酸钾,待物料冷却后,用
,待反应物干涸后,加大火焰强热4-8 min,得墨绿色的锰酸钾,待物料冷却后,用 溶液重复浸取,合并浸取液便得墨绿色的锰酸钾溶液。
溶液重复浸取,合并浸取液便得墨绿色的锰酸钾溶液。Ⅱ.锰酸钾的歧化
在浸取液中通入适量
 气体,使
气体,使 歧化为
歧化为 和
和 ,歧化完全后把溶液加热,趁热抽滤,滤去
,歧化完全后把溶液加热,趁热抽滤,滤去 残渣。
残渣。Ⅲ.结晶
把滤液移至蒸发皿内,蒸发浓缩,停止加热,冷却结晶,抽滤、洗涤、干燥、称量至恒重.计算产率。
IV.纯度测定
称取制得的高锰酸钾产品
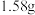 ,配成
,配成 溶液,用移液管量取
溶液,用移液管量取 待测液,选择
待测液,选择 滴定管,用
滴定管,用 草酸钠标准溶液进行滴定,发生反应
草酸钠标准溶液进行滴定,发生反应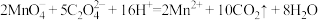 ,重复测定三次,计算纯度。
,重复测定三次,计算纯度。请回答下列问题:
(1)步骤Ⅰ中仪器A可选用
①蒸发皿 ②瓷坩埚 ③烧杯 ④铁坩埚

(2)已知
 、
、 、
、 溶解度随温度变化曲线如图,步骤Ⅱ中
溶解度随温度变化曲线如图,步骤Ⅱ中 不能通得过多的原因是
不能通得过多的原因是(3)步骤Ⅱ中检验
 歧化完全的实验方法是
歧化完全的实验方法是(4)步骤Ⅲ中有关说法正确的是
A.为得到较大晶体颗粒,宜用冰水浴冷却结晶
B.蒸发浓缩至溶液表面出现晶膜时,停止加热
C.本实验应采用低温干燥的方法来干燥产品
D.放入比布氏漏斗内径略小的滤纸后,用蒸馏水润湿,微开水龙头使滤纸紧贴瓷板
(5)步骤Ⅳ配制高锰酸钾溶液时必须使用到的仪器的先后顺序为
a.
 容量瓶 b.
容量瓶 b. 容量瓶 c.玻璃棒 d.烧杯 e.电子天平 f.胶头滴管 g.量筒
容量瓶 c.玻璃棒 d.烧杯 e.电子天平 f.胶头滴管 g.量筒(6) 若移液管用蒸馏水洗净干燥后没有用待测液润洗就进行后面的实验,将
您最近一年使用:0次