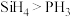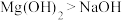某同学学习元素周期律后,作出以下推测,其中错误的是
| A.Ra是第七周期第IIA族的元素,推测Ra(OH)2碱性比Ba(OH)2强 |
| B.Sb是第四周期第VA族的元素,推测SbH3比NH3稳定 |
| C.Cs的原子半径大于Na的原子半径,推测Cs与水反应比Na与水反应更剧烈 |
| D.Cl的核电荷数比Al大,推测Cl的半径比Al的半径小 |
更新时间:2019-11-29 19:20:29
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】A、B、C三种元素的原子核外具有相同的电子层数,其最高价氧化物对应水化物的酸性强弱顺序是HAO4>H2BO4>H3CO4,则下列判断中错误的是
| A.原子序数C>B>A | B.气态氢化物的稳定性HA>H2B>H3C |
| C.阴离子还原性:C3->B2->A- | D.最外层电子数A>B>C |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列各组属性的比较中正确的是
| A.离子半径:Na+ <Mg2+ <Al3+ | B.原子半径:C<N<O |
| C.酸性:HClO4 <HBrO4 <HIO4 | D.稳定性:HCl>H2S>PH3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列各组比较,不正确的是( )
| A.热稳定性:HBr>HCl | B.碱性:Al(OH)3<Mg(OH)2 |
| C.氧化性:O<F | D.还原性:S2﹣>O2﹣ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列叙述中错误的是
| A.氧化性:Na +<Mg2+<Al3+ | B.沸点:H2Se>H2S>H2O |
| C.稳定性:HF>HCl>HBr | D.酸性:HClO4>H2SO4>H3PO4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】短周期主族元素X、Y、Z、W原子序数依次增大,X的单质是粮仓中常用的保护气;Y的+3价阳离子的核外电子排布与氖原子相同;Y和Z原子的最外层电子数之和等于W原子的最外层电子数;Z原子核外电子数是W原子最外层电子数的2倍。下列说法正确的是
| A.原子半径:r(Y)<r(X)<r(W)<r(Z) |
| B.元素X的最高价含氧酸的酸性比Z的强 |
| C.电解Y、W形成的化合物可制取Y单质 |
| D.Z的简单气态氢化物的热稳定性比W的强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列各组中的性质比较,正确的是( )
①酸性:HClO4>HBrO4>HIO4 ②碱性:Ba(OH)2>Ca(OH)2>Mg(OH)2 ③稳定性:HCl>H2S>PH3 ④还原性:F->Cl->Br-
①酸性:HClO4>HBrO4>HIO4 ②碱性:Ba(OH)2>Ca(OH)2>Mg(OH)2 ③稳定性:HCl>H2S>PH3 ④还原性:F->Cl->Br-
| A.①②④ | B.③④ | C.①②③ | D.①②③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】W、X、Y、Z为原子序数依次增大的四种短周期主族元素,W、X、Z分别属于三个不同周期。X是形成化合物种类最多的元素,Y与Z同主族,且Z的质子数为Y的2倍。下列叙述错误的是
| A.W与X形成的化合物中可能含有非极性共价键 |
| B.不可用澄清石灰水鉴别ZY2与XY2 |
| C.X与Y的简单气态氢化物稳定性X<Y |
| D.Y与Z形成的化合物溶于水都生成强酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列递变规律正确的是( )
| A.单质Na、Mg、Al的还原性逐渐增强 |
B. 、 、 、 、 的酸性依次增强 的酸性依次增强 |
| C.元素P、S、Cl的最高化合价依次降低 |
| D.Cl-、Br-、I-的还原性逐渐增强 |
您最近一年使用:0次