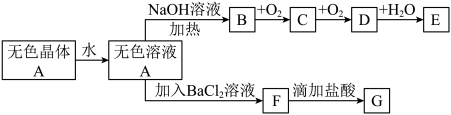
A、B、C、D为原子序数依次增大短周期元素,A的最外层电子数是其电子层数2倍;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E;D的L层电子数等于其它电子层上的电子数之和。
(1)A元素名称为______ ,D在周期表中的位置________ ,离子半径大小B___ C(填“>”“<”或“=”)。
(2)B的两种单质在常温下都是气体,它们互为____________ 。比较B的氢化物和D的氢化物沸点:B___ D(填“>”“<”或“=”),原因是_________________ 。
(3)E中含有化学键类型:_________ ,属于___________ 化合物(填“离子化合物”或“共价化合物”)。
(4)用电子式表示C与D的二元化合物的形成过程:_____________________ 。
(5)氢原子与B分别形成10电子和18电子分子,写出18电子分子转化成10电子分子的化学方程式__________________ 。
(1)A元素名称为
(2)B的两种单质在常温下都是气体,它们互为
(3)E中含有化学键类型:
(4)用电子式表示C与D的二元化合物的形成过程:
(5)氢原子与B分别形成10电子和18电子分子,写出18电子分子转化成10电子分子的化学方程式
更新时间:2019-12-05 13:28:41
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】有以下6种元素,其中R、W、X、Y、M是原子序数依次增大的五种短周期元素,R最常见同位素的原子核中不含中子。W与X可形成两种稳定的化合物:WX和WX2.工业革命以来,人类使用的化石燃料在燃烧过程中将大量WX2排入大气,在一定程度导致地球表面平均温度升高。Y与X是同一主族的元素,且在元素周期表中与X相邻。Q是第4周期第Ⅷ族元素,它的一种复杂的化合物是具有磁性的黑色晶体。
(1)若R的一种原子中质子数和中子数相等,则R的原子组成符号为___________ ;R2Y、R2X都属于___________ (填“离子”或“共价”)化合物。W在元素周期表中的位置___________ 。
(2)M是生活中常见的一种元素,它能与很多元素形成化合物。
①用电子式表示RM的形成过程___________ 。
②如图所示,将M单质水溶液滴入试管中。试管中的实验现象为___________ 。___________ 。
③MX2是一种高效消毒剂,工业上用其处理中性废水中的锰,使 转化为MnO2沉淀除去,M被还原至最低价,该反应的离子方程式为
转化为MnO2沉淀除去,M被还原至最低价,该反应的离子方程式为___________ 。
(3)元素硒(Se)的原子结构示意图为
根据元素周期律,下列推断正确的是___________ (填字母序号)
a.Se位于第4周期、与Y同主族 b.Se的最低负化合价为-2价
c.SeO2具有还原性 d.H2Se的还原性比H2Y强
e.H2SeO3的酸性强于H2SO4 f.SeO2在一定条件下可与NaOH溶液反应
(4)下列事实能判断元素金属性强弱的是___________ (填字母)。
a.常温下单质与水反应置换出氢的难易程度
b.最高价氧化物对应的水化物的碱性强弱
c.相同温度下,最高价氧化物对应的水化物的溶解度大小
(1)若R的一种原子中质子数和中子数相等,则R的原子组成符号为
(2)M是生活中常见的一种元素,它能与很多元素形成化合物。
①用电子式表示RM的形成过程
②如图所示,将M单质水溶液滴入试管中。试管中的实验现象为

③MX2是一种高效消毒剂,工业上用其处理中性废水中的锰,使
 转化为MnO2沉淀除去,M被还原至最低价,该反应的离子方程式为
转化为MnO2沉淀除去,M被还原至最低价,该反应的离子方程式为(3)元素硒(Se)的原子结构示意图为

根据元素周期律,下列推断正确的是
a.Se位于第4周期、与Y同主族 b.Se的最低负化合价为-2价
c.SeO2具有还原性 d.H2Se的还原性比H2Y强
e.H2SeO3的酸性强于H2SO4 f.SeO2在一定条件下可与NaOH溶液反应
(4)下列事实能判断元素金属性强弱的是
a.常温下单质与水反应置换出氢的难易程度
b.最高价氧化物对应的水化物的碱性强弱
c.相同温度下,最高价氧化物对应的水化物的溶解度大小
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】现有X、Y、Z、M、Q五种元素,其中X、Y、Z、M是原子序数逐渐增大的短周期主族元素,X为同周期中原子半径最小的金属元素,M为同周期中原子半径最大的金属元素,一定条件下,化合物YZ2与M的单质反应可制备目前最硬的一种非金属单质,X、Y、Z、M的核外电子总数与Q的核外电子总数相等。回答下列问题:
(1)X、Y、Z、M的原子半径由大到小的顺序为_______ (用元素符号表示)。
(2)写出M的单质在Z的单质中燃烧的化学方程式:_______ 。
(3)写出YZ2与M的单质反应的化学方程式(其中YZ2与M的化学计量数之比为3:4):_______ (不用标条件),该反应体现了YZ2的_______ 性质。
(4)由Q的单质制备的物质在空气中久置,表面会生成一层绿色的物质,该绿色物质的主要成分是_______ (填化学式)。
(1)X、Y、Z、M的原子半径由大到小的顺序为
(2)写出M的单质在Z的单质中燃烧的化学方程式:
(3)写出YZ2与M的单质反应的化学方程式(其中YZ2与M的化学计量数之比为3:4):
(4)由Q的单质制备的物质在空气中久置,表面会生成一层绿色的物质,该绿色物质的主要成分是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E、M、N六种短周期主族元素,它们的核电荷数依次增大。A可与D、E形成10电子分子,其中B的最外层电子数等于次外层电子数,C原子最外层电子数是次外层电子数的2倍,M的L层电子数为K层和M层电子数之和,D和M同主族。回答下列问题:
(1)元素B的名称是______ ,在周期表中的位置是_________________
(2)元素D的原子结构示意图为______________________________
(3)元素C与M可形成CM2,其电子式为:_________
(4)元素C与N可形成CN4,其结构式为:__________
(5)元素D、E的简单氢化物的沸点高低顺序为:_______ > _______ (填化学式)
(6)在一定条件下,A、D的单质和M的最高价氧化物对应水化物的溶液可构成原电池,该电池在放电过程中,电解质溶液的pH将_________ (填“增大”“减小”或“不变”)
(1)元素B的名称是
(2)元素D的原子结构示意图为
(3)元素C与M可形成CM2,其电子式为:
(4)元素C与N可形成CN4,其结构式为:
(5)元素D、E的简单氢化物的沸点高低顺序为:
(6)在一定条件下,A、D的单质和M的最高价氧化物对应水化物的溶液可构成原电池,该电池在放电过程中,电解质溶液的pH将
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】有X、Y、Z三种短周期元素,X的气态氢化物化学式为H2X,此氢化物的分子量与X最高价氧化物的分子量之比为17∶40,X原子核内质子数与中子数相等,Y与X可以形成离子化合物Y2X,Y 的阳离子电子层结构与Ne相同,Z与X同周期,其气态单质是双原子分子,两原子共用1对电子。试回答:
(1)写出各元素符号:X____________ 、Y____________ 、Z____________ 。
(2)X与Y形成的离子化合物的电子式为______________ 。
(3)Y 元素在周期表中的位置为__________ ,其单质在空气中燃烧产物的电子式为__________ 。
(1)写出各元素符号:X
(2)X与Y形成的离子化合物的电子式为
(3)Y 元素在周期表中的位置为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】五种短周期主族元素X、Y、Z、E、F,原子序数依次增大.X是非金属元素,且最外层电子数与其周期数相同;Y的最外层电子数是其所在周期数的2倍;Z的最外层电子数与最内层电子数之比为1∶3;E+与Z的最简单离子具有相同的电子数;X单质在F单质中燃烧,有苍白色火焰。回答下列问题:
(1)Z在周期表中的位置是______ 。
(2)E2Z2的电子式为______ 。
(3)XFZ的结构式为______ 。
(4)元素Z、E、F形成的最简单离子的半径由大到小为______ (用离子符号表示)。
(5)Y、Z的最简单气态氢化物的稳定性是:_______>_______(用化学式表示)。______
(6)设计一个简单的实验证明F和Y的非金属性强弱______ (用化学方程式表示)。
(1)Z在周期表中的位置是
(2)E2Z2的电子式为
(3)XFZ的结构式为
(4)元素Z、E、F形成的最简单离子的半径由大到小为
(5)Y、Z的最简单气态氢化物的稳定性是:_______>_______(用化学式表示)。
(6)设计一个简单的实验证明F和Y的非金属性强弱
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】短周期主族元素Q、T、U、V、W、X、Y、Z原子序数依次增大。已知:T与U、V同周期,W与X、Y、Z同周期,U和Y同族;元素Q的某种核素没有中子;元素T的最高正价与最低负价的代数和为0;Q与U形成的气态化合物在标准状况下的密度为0.76g/L;工业上通过分离液态空气获得V的单质,且该单质的某种同素异形体是保护地球地表环境的重要屏障;W、X、Z的最高价氧化物对应的水化物两两之间都能反应,且W、X、Z原子最外层电子数之和等于W的原子序数。按要求回答下列问题:
(1)V元素原子的L层电子数为___________ 。元素W在周期表中的位置为___________ 。
(2)用电子式表示化合物OZ的形成过程___________ 。
(3)沸点:
___________  (填“>”或“<”),判断依据是
(填“>”或“<”),判断依据是___________ 。
(4)写出X、Z两种元素最高价氧化物对应的水化物相互反应的离子方程式:___________ 。
(5)T、U、V形成的氢化物分子中共价键的极性由强到弱的顺序为___________ 。(填化学式)
(6)Q与T可形成一种化合物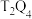 ,请写出该分子的结构式
,请写出该分子的结构式___________ 。
(7) 是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用该物质干燥的是
是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用该物质干燥的是___________ 。(填序号)
a. b.HI c.
b.HI c. d.
d.
(1)V元素原子的L层电子数为
(2)用电子式表示化合物OZ的形成过程
(3)沸点:

 (填“>”或“<”),判断依据是
(填“>”或“<”),判断依据是(4)写出X、Z两种元素最高价氧化物对应的水化物相互反应的离子方程式:
(5)T、U、V形成的氢化物分子中共价键的极性由强到弱的顺序为
(6)Q与T可形成一种化合物
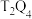 ,请写出该分子的结构式
,请写出该分子的结构式(7)
 是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用该物质干燥的是
是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用该物质干燥的是a.
 b.HI c.
b.HI c. d.
d.
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】同周期中A、B、C、D、E、F为原子序数依次增大的短周期元素。已知:A、C、F三种原子的最外层共有11个电子,且这三种元素的最高价氧化物对应的水化物之间两两皆能反应,均生成盐和水。请完成下列问题:
(1)根据以上条件一定能判断出的元素有几种,请在下列横线上写出相应的元素符号:
A._____________ ,B._____________ ,C._____________ ,
D._____________ ,E._______________ ,F._____________ 。
(2)已知D单质在F单质中燃烧可能生成两种化合物,请分别写出生成两种化合物的化学方程式:____________________ ;______________________ 。
(1)根据以上条件一定能判断出的元素有几种,请在下列横线上写出相应的元素符号:
A.
D.
(2)已知D单质在F单质中燃烧可能生成两种化合物,请分别写出生成两种化合物的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】W、X、Y、Z是原子序数依次增大的四种短周期元素。W的气态氢化物能使紫色石蕊溶液变蓝,W、X和Y三种元素的最高价氧化物对应的水化物两两之间可以发生反应,W、X、Y、Z的最外层电子数之和为16。回答下列问题:
(1)元素X在元素周期表中的位置是:_______ ,Z单质的电子式是_______ 。
(2)W的气态氢化物能使紫色石蕊溶液变蓝的原因:_______ (用化学用语表示)。
(3)X、Y、Z三种元素的简单离子的离子半径由大到小的顺序是:_______ (用离子符号表示)。
(4)Z最高价氧化物对应的水化物化学式为_______ 。
(5)W最高价氧化物对应的水化物稀溶液与Y最高价氧化物对应的水化物反应的离子方程式为_______ 。
(6)Z和氧元素、硫元素组成的SOZ2是一种液态化合物,沸点为77℃,遇水能剧烈水解,有白雾和带有刺激性气味的气体逸出,该气体可使滴有品红试液的滤纸褪色。请写出SOZ2和水反应的化学方程式_______ 。
(1)元素X在元素周期表中的位置是:
(2)W的气态氢化物能使紫色石蕊溶液变蓝的原因:
(3)X、Y、Z三种元素的简单离子的离子半径由大到小的顺序是:
(4)Z最高价氧化物对应的水化物化学式为
(5)W最高价氧化物对应的水化物稀溶液与Y最高价氧化物对应的水化物反应的离子方程式为
(6)Z和氧元素、硫元素组成的SOZ2是一种液态化合物,沸点为77℃,遇水能剧烈水解,有白雾和带有刺激性气味的气体逸出,该气体可使滴有品红试液的滤纸褪色。请写出SOZ2和水反应的化学方程式
您最近一年使用:0次