实验室用少量的溴水和足量的乙烯制备1,2-二溴乙烷的装置如图所示:
有关数据列表如下:
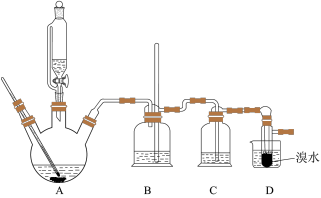
回答下列问题:
(1)烧瓶A中发生的主要的反应方程式:___________________________________ 。
(2)安全瓶B可以防倒吸,并可以检查实验进行时试管D是否发生堵塞.请写出发生堵塞时瓶B中的现象:______________________________________________________ 。
(3)在装置C中应加入_____ (填字母),(a.水 b.浓硫酸 c.氢氧化钠溶液)其目的是 ___________________________________________________________________ 。
(4)若产物中有少量副产物乙醚,可用________________ 的方法除去。
(5)反应过程中应用冷水冷却装置D,但又不能过度冷却(如用冰水),其原因是_________________________________________________________________________ 。
有关数据列表如下:

| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -l30 | 9 | -1l6 |
(1)烧瓶A中发生的主要的反应方程式:
(2)安全瓶B可以防倒吸,并可以检查实验进行时试管D是否发生堵塞.请写出发生堵塞时瓶B中的现象:
(3)在装置C中应加入
(4)若产物中有少量副产物乙醚,可用
(5)反应过程中应用冷水冷却装置D,但又不能过度冷却(如用冰水),其原因是
更新时间:2019-12-04 20:19:25
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】环己烯是重要的化工原料。其实验室制备流程如下:
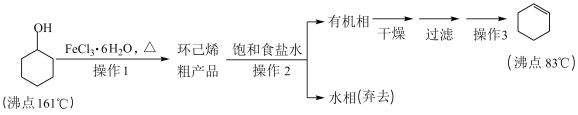
回答下列问题:
Ⅰ.环己烯的制备与提纯
(1)原料FeCl3·6H2O中若含FeCl2杂质,检验方法为:取一定量的该样品配成溶液,加入__________ (填化学式) 溶液,现象为__________ 。
(2)操作1的装置如图所示(加热和夹持装置已略去)。

①浓硫酸也可作该反应的催化剂,选择FeCl3·6H2O而不用浓硫酸的原因为___ (填序号)。
a 浓硫酸易使原料碳化并产生SO2
b FeCl3·6H2O污染小、可循环使用,符合绿色化学理念
c 同等条件下,用FeCl3·6H2O比浓硫酸的平衡转化率高
②仪器B的作用为____________ 。
(3)下列玻璃仪器中,操作2中需使用的有________ (填标号)。
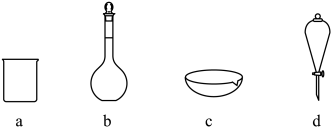
(4)将操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和沸石,________ (填序号)。
①弃去前馏分,收集83℃的馏分②加热③通冷凝水
Ⅱ.环己烯含量的测定
在一定条件下,向a g环己烯样品中加入b mol Br2。充分反应后,向所得溶液中加入足量的KI,再用c mol/L的Na2S2O3标准溶液滴定该溶液,终点时消耗Na2S2O3标准溶液v mL(以上数据均已扣除干扰因素)。 [已知: ]
]
(5)滴定所用指示剂为____________ 。样品中环己烯的质量分数为____________ (用字母表示)。
(6)上述滴定完成后,若滴定管尖嘴处留有气泡会导致最终测定的环己烯含量偏__________ 。(填“高”或“低”)

回答下列问题:
Ⅰ.环己烯的制备与提纯
(1)原料FeCl3·6H2O中若含FeCl2杂质,检验方法为:取一定量的该样品配成溶液,加入
(2)操作1的装置如图所示(加热和夹持装置已略去)。

①浓硫酸也可作该反应的催化剂,选择FeCl3·6H2O而不用浓硫酸的原因为
a 浓硫酸易使原料碳化并产生SO2
b FeCl3·6H2O污染小、可循环使用,符合绿色化学理念
c 同等条件下,用FeCl3·6H2O比浓硫酸的平衡转化率高
②仪器B的作用为
(3)下列玻璃仪器中,操作2中需使用的有

(4)将操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和沸石,
①弃去前馏分,收集83℃的馏分②加热③通冷凝水
Ⅱ.环己烯含量的测定
在一定条件下,向a g环己烯样品中加入b mol Br2。充分反应后,向所得溶液中加入足量的KI,再用c mol/L的Na2S2O3标准溶液滴定该溶液,终点时消耗Na2S2O3标准溶液v mL(以上数据均已扣除干扰因素)。 [已知:
 ]
](5)滴定所用指示剂为
(6)上述滴定完成后,若滴定管尖嘴处留有气泡会导致最终测定的环己烯含量偏
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
真题
名校
【推荐2】苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线:
 + H2O+H2SO4
+ H2O+H2SO4
 +NH4HSO4
+NH4HSO4
 +Cu(OH)2→(
+Cu(OH)2→( )2Cu+H2O
)2Cu+H2O
制备苯乙酸的装置示意图如下(加热和夹持装置等略):

已知:苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇。
回答下列问题:
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是
__________________________ 。
(2)将a中的溶液加热至100℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130℃继续反应。在装置中,仪器b的作用是_____________________ ;仪器c的名称是______________ ,其作用是___________________________________________ 。
反应结束后加适量冷水,再分离出苯乙酸粗品。加入冷水的目的是____________ 。下列仪器中可用于分离苯乙酸粗品的是________________ (填标号)。
(3)提纯粗苯乙酸的方法是_____________ ,最终得到44 g纯品,则苯乙酸的产率是________ 。
(4)用CuCl2• 2H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是____________________________________________ 。
(5)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是___________________ 。
 + H2O+H2SO4
+ H2O+H2SO4
 +NH4HSO4
+NH4HSO4 +Cu(OH)2→(
+Cu(OH)2→( )2Cu+H2O
)2Cu+H2O制备苯乙酸的装置示意图如下(加热和夹持装置等略):

已知:苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇。
回答下列问题:
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是
(2)将a中的溶液加热至100℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130℃继续反应。在装置中,仪器b的作用是
反应结束后加适量冷水,再分离出苯乙酸粗品。加入冷水的目的是
| A.分液漏斗 | B.漏斗 | C.烧杯 | D.直形冷凝管E.玻璃棒 |
(3)提纯粗苯乙酸的方法是
(4)用CuCl2• 2H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是
(5)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】实验室模仿工业上生产过氧化钙的主要流程如下:

已知: 呈白色,微溶于水,加热至
呈白色,微溶于水,加热至 左右开始分解放出氧气。
左右开始分解放出氧气。
(1)实验装置如下:

①请写出装置的连接顺序___________ (填序号)。
②写出沉淀生成的化学方程式___________ 。
(2)乙醇洗涤的目的是___________ 。
(3)请设计实验定性检验产品为 (简单地描述实验步骤和现象)
(简单地描述实验步骤和现象)___________ 。
(4)产品纯度测定实验步骤如下:
第一步:准确称取 产品于烧杯中,加入适量的盐酸使其完全溶解;
产品于烧杯中,加入适量的盐酸使其完全溶解;
第二步:向上述溶液中加入稍过量的 ,沉淀完全,过滤并洗涤沉淀;
,沉淀完全,过滤并洗涤沉淀;
第三步:将洗涤好的沉淀用稍过量的稀硫酸溶解,溶解液和洗涤液全部转移至锥形瓶中;
第四步:向锥形瓶中滴入几滴 溶液,然后逐滴滴入浓度为
溶液,然后逐滴滴入浓度为 的
的 溶液至终点,消耗
溶液至终点,消耗 溶液
溶液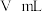 。
。
①滴定前,滴入 溶液的目的是
溶液的目的是___________ 。
②产品的纯度为___________ (用字母表示)。
③若第三步用稀盐酸溶解,所测纯度___________ (填“偏低”“不变”或“偏高”)。

已知:
 呈白色,微溶于水,加热至
呈白色,微溶于水,加热至 左右开始分解放出氧气。
左右开始分解放出氧气。(1)实验装置如下:

①请写出装置的连接顺序
②写出沉淀生成的化学方程式
(2)乙醇洗涤的目的是
(3)请设计实验定性检验产品为
 (简单地描述实验步骤和现象)
(简单地描述实验步骤和现象)(4)产品纯度测定实验步骤如下:
第一步:准确称取
 产品于烧杯中,加入适量的盐酸使其完全溶解;
产品于烧杯中,加入适量的盐酸使其完全溶解;第二步:向上述溶液中加入稍过量的
 ,沉淀完全,过滤并洗涤沉淀;
,沉淀完全,过滤并洗涤沉淀;第三步:将洗涤好的沉淀用稍过量的稀硫酸溶解,溶解液和洗涤液全部转移至锥形瓶中;
第四步:向锥形瓶中滴入几滴
 溶液,然后逐滴滴入浓度为
溶液,然后逐滴滴入浓度为 的
的 溶液至终点,消耗
溶液至终点,消耗 溶液
溶液 。
。①滴定前,滴入
 溶液的目的是
溶液的目的是②产品的纯度为
③若第三步用稀盐酸溶解,所测纯度
您最近一年使用:0次



