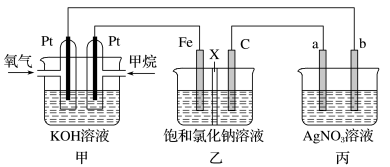
如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为离子交换膜。
请按要求回答相关问题:
(1)甲烷燃料电池负极电极反应式是:____________________________________ 。
(2)向乙中加入几滴酚酞溶液,工作一段时间后铁电极附近溶液变红,请用化学用语解释相关原因__________________________________
(3)若在标准状况下,有4.48 L氧气参加反应,则乙装置中C电极上生成的气体的物质的量为__________ 。
(4)欲用丙装置给铜镀银,b应是____________ (填化学式)。

请按要求回答相关问题:
(1)甲烷燃料电池负极电极反应式是:
(2)向乙中加入几滴酚酞溶液,工作一段时间后铁电极附近溶液变红,请用化学用语解释相关原因
(3)若在标准状况下,有4.48 L氧气参加反应,则乙装置中C电极上生成的气体的物质的量为
(4)欲用丙装置给铜镀银,b应是
更新时间:2019-12-10 19:20:33
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航空航天。如图1所示装置中,以稀土金属材料作惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导正极生成的O2-离子(O2+4e-=2O2-)。
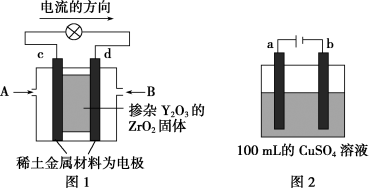
(1)c电极为___________ 极,d电极上的电极反应式为___________
(2)如图2所示为用惰性电极电解100mLCuSO4溶液,a电极上的电极反应式为___________ ;电解一段时间后,a电极产生气体,b电极不产生气体,则溶液的pH___________ (填“减小”或“增大”),要使电解质溶液恢复到电解前的状态,可加入___________ (填序号)
a.CuO b.Cu(OH)2 c.CuCO3 d.Cu2(OH)2CO3
(3)在工业上,利用该电池电解NaOH溶液生产Na2FeO4,装置如图。
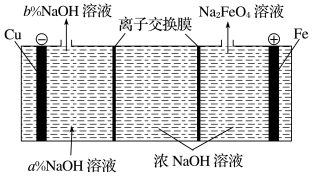
①阳极的电极反应式为___________ 。
②阴极产生的气体为___________ 。
③右侧的离子交换膜为___________ (填“阴”或“阳”)离子交换膜,阴极区a%___________ b%(填“>”“=”或“<”)。

(1)c电极为
(2)如图2所示为用惰性电极电解100mLCuSO4溶液,a电极上的电极反应式为
a.CuO b.Cu(OH)2 c.CuCO3 d.Cu2(OH)2CO3
(3)在工业上,利用该电池电解NaOH溶液生产Na2FeO4,装置如图。

①阳极的电极反应式为
②阴极产生的气体为
③右侧的离子交换膜为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。工业上以硫铁矿为原料制硫酸所产生的尾气除了含有N2、O2外,还含有SO2。为了保护环境,同时提高硫酸工业的综合经济效益,应尽可能将尾气中的SO2转化为有用的产品。
治理方案Ⅰ:
(1)将尾气通入氨水中,能发生多个反应,写出其中可能发生的两个氧化还原反应的化学方程式:_______________ 、_______________ 。
治理方案Ⅱ:
某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下流程既去除尾气中的SO2,又制得电池材料MnO2 (反应条件已省略)。
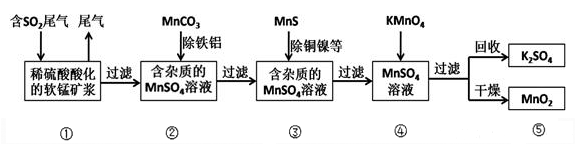
请回答下列问题:
(2)用MnCO3能除去溶液中Al3+和Fe3+其原因是___________________________ ,用MnS除去溶液中的Cu2+的离子方程式为_______________ 。
(3)流程图④过程中发生的主要反应的化学方程式为___________________ 。
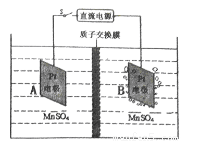
(4)MnO2可作超级电容器材料。工业上用下图所示装置制备MnO2。接通电源后,A电极的电极反应式为:_______________ ,当制备lmol MnO2,则膜两侧电解液的质量变化差(△m左-△m右)为_______________ g。
治理方案Ⅰ:
(1)将尾气通入氨水中,能发生多个反应,写出其中可能发生的两个氧化还原反应的化学方程式:
治理方案Ⅱ:
某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下流程既去除尾气中的SO2,又制得电池材料MnO2 (反应条件已省略)。

请回答下列问题:
(2)用MnCO3能除去溶液中Al3+和Fe3+其原因是
(3)流程图④过程中发生的主要反应的化学方程式为
(4)MnO2可作超级电容器材料。工业上用下图所示装置制备MnO2。接通电源后,A电极的电极反应式为:

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】化学能与电能可相互转化,根据下图回答问题。
(1)若两装置中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲装置中的______ 棒,乙装置中的____________ 棒。(填“铁”或“碳”)
②乙装置中阳极上发生的电极反应式为________________________ 。
(2)若两装置中均为饱和NaCl溶液:
①甲装置中碳棒上电极反应属于_________________ (填“氧化反应”或“还原反应”)。
②乙装置中反应的化学方程式为__________________ 。
③若乙装置转移0.1mole-后停止实验,且溶液体积为1L,则溶液混匀后的c(OH-)=_____ 。(不考虑所生成气体在溶液中的溶解)
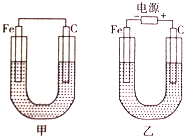
(1)若两装置中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲装置中的
②乙装置中阳极上发生的电极反应式为
(2)若两装置中均为饱和NaCl溶液:
①甲装置中碳棒上电极反应属于
②乙装置中反应的化学方程式为
③若乙装置转移0.1mole-后停止实验,且溶液体积为1L,则溶液混匀后的c(OH-)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
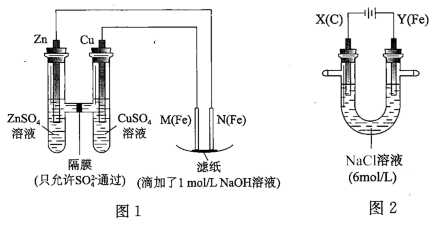
【推荐1】某课外小组分别用如图所示装置对原电池和电解原理进行实验探究。
请回答:
Ⅰ.用图 1 所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代 Cu 作电极的是__ (填字母序号)。
A 铝 B 石墨 C 银 D 铂
(2)N 极发生反应的电极反应式为__ 。
Ⅱ.用图 2 所示装置进行第二组实验。实验过程中,观察到与第一组实验不同的现象:两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。 查阅资料得知,高铁酸根离子(FeO42-)在溶液中呈紫红色。
(3)电解过程中,X 极区溶液的 pH__ (填“增大”“减小”或“不变”)。
(4)电解过程中,Y 极发生的电极反应之一为 Fe﹣6e﹣+8OH﹣= FeO42-+4H2O 若在 X 极收集到672 mL 气体,在 Y 极收集到 168 mL 气体(均已折算为标准状况时气体体积),则 Y 电极(铁电极)质量减少____ g。
(5)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为 2K2FeO4+3Z=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的反应的电极反应式为__ 。

请回答:
Ⅰ.用图 1 所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代 Cu 作电极的是
A 铝 B 石墨 C 银 D 铂
(2)N 极发生反应的电极反应式为
Ⅱ.用图 2 所示装置进行第二组实验。实验过程中,观察到与第一组实验不同的现象:两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。 查阅资料得知,高铁酸根离子(FeO42-)在溶液中呈紫红色。
(3)电解过程中,X 极区溶液的 pH
(4)电解过程中,Y 极发生的电极反应之一为 Fe﹣6e﹣+8OH﹣= FeO42-+4H2O 若在 X 极收集到672 mL 气体,在 Y 极收集到 168 mL 气体(均已折算为标准状况时气体体积),则 Y 电极(铁电极)质量减少
(5)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为 2K2FeO4+3Z=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的反应的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某课外活动小组用如图装置进行实验,试回答下列问题:

(1)若开始时开关K与a连接,则B极的电极反应式为______________ 。
(2)若开始时开关K与b连接,则B极的电极反应式为__________ ,总反应的离子方程式为____________ 。
(3)若开始时开关K与b连接.下列说法正确的是_______ 。
A.溶液中Na+向A极移动
B.从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
C.反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
D.若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(4)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阳极反应式为________ 。
②制得的氢氧化钾溶液从出口(填“A”、“B”、“C”或 “D”)________ 导出。
③电解过程中阴极区碱性明显增强,用平衡移动原理解释原因_________________________ 。

(1)若开始时开关K与a连接,则B极的电极反应式为
(2)若开始时开关K与b连接,则B极的电极反应式为
(3)若开始时开关K与b连接.下列说法正确的是
A.溶液中Na+向A极移动
B.从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
C.反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
D.若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(4)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阳极反应式为
②制得的氢氧化钾溶液从出口(填“A”、“B”、“C”或 “D”)
③电解过程中阴极区碱性明显增强,用平衡移动原理解释原因
您最近一年使用:0次
【推荐3】I.甲醇是一种重要的化工原料和新型燃料。如图是甲醇燃料电池工作的示意图,工作一段时间后,断开K。
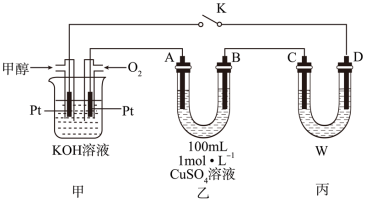
(1)甲中负极的电极反应式为_______ 。
(2)若丙中C为铝,D为石墨,W溶液为稀 ,若能使铝的表面生成一层致密的氧化膜,则C电极反应式为
,若能使铝的表面生成一层致密的氧化膜,则C电极反应式为_______ 。
(3)若A、B、C、D均为石墨,W溶液为饱和氯化钠溶液:
a.丙中电解的总化学方程式为_______ 。·
b.工作一段时间后,向乙中所得溶液加入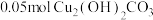 后恰好使电解质溶液复原,则丙中D电极上生成的气体标况下的体积为
后恰好使电解质溶液复原,则丙中D电极上生成的气体标况下的体积为_______ 。
(4)若把乙装置改为精炼铜装置(粗铜含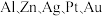 等杂质),下列说法正确的是_______。
等杂质),下列说法正确的是_______。
(5)用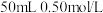 盐酸和
盐酸和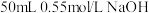 溶液反应测定中和热,实验中测得起始平均温度为
溶液反应测定中和热,实验中测得起始平均温度为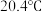 ,反应后最高温度为
,反应后最高温度为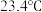 ,反应后溶液的比热容为
,反应后溶液的比热容为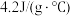 盐酸和
盐酸和 溶液的密度都近似认为是
溶液的密度都近似认为是 ,则中和热
,则中和热
_______ 。
II.甲烷是一种重要的化工原料和清洁能源,研究其相关反应并合理利用具有重要意义。请回答下列问题:
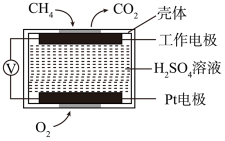
(6)甲烷属于易燃易爆气体,可用电化学原理测定空气中甲烷的含量防止爆炸事故的发生,其原理如图所示,则负极的电极反应式为_______ ﹔若测得标准状况下空气中甲烷的含量为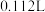 ,当甲烷完全被氧化时消耗的
,当甲烷完全被氧化时消耗的 为
为_______  。
。

(1)甲中负极的电极反应式为
(2)若丙中C为铝,D为石墨,W溶液为稀
 ,若能使铝的表面生成一层致密的氧化膜,则C电极反应式为
,若能使铝的表面生成一层致密的氧化膜,则C电极反应式为(3)若A、B、C、D均为石墨,W溶液为饱和氯化钠溶液:
a.丙中电解的总化学方程式为
b.工作一段时间后,向乙中所得溶液加入
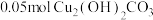 后恰好使电解质溶液复原,则丙中D电极上生成的气体标况下的体积为
后恰好使电解质溶液复原,则丙中D电极上生成的气体标况下的体积为(4)若把乙装置改为精炼铜装置(粗铜含
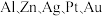 等杂质),下列说法正确的是_______。
等杂质),下列说法正确的是_______。| A.电解过程中,阳极减少的质量与阴极增加的质量相等 |
| B.A为粗铜,发生氧化反应 |
C. 溶液的浓度保持不变 溶液的浓度保持不变 |
| D.杂质都将以单质的形式沉淀到池底 |
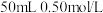 盐酸和
盐酸和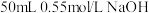 溶液反应测定中和热,实验中测得起始平均温度为
溶液反应测定中和热,实验中测得起始平均温度为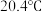 ,反应后最高温度为
,反应后最高温度为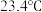 ,反应后溶液的比热容为
,反应后溶液的比热容为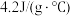 盐酸和
盐酸和 溶液的密度都近似认为是
溶液的密度都近似认为是 ,则中和热
,则中和热
II.甲烷是一种重要的化工原料和清洁能源,研究其相关反应并合理利用具有重要意义。请回答下列问题:
(6)甲烷属于易燃易爆气体,可用电化学原理测定空气中甲烷的含量防止爆炸事故的发生,其原理如图所示,则负极的电极反应式为
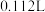 ,当甲烷完全被氧化时消耗的
,当甲烷完全被氧化时消耗的 为
为 。
。
您最近一年使用:0次



