对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。
Ⅰ.现有以下物质:①H2O ②Cu ③BaCO3 ④Fe(OH)3胶体 ⑤酒精 ⑥CO2 ⑦稀硫酸
(1)以上物质中属于混合物的是________ (填序号,下同),属于电解质的是________ 。
(2)向④中逐滴滴加⑦,可观察到的现象是_____________________ 。
Ⅱ.虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
(3)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是________ (填字母)。

(4)有同学认为所有酸碱中和反应均可表示为H++OH-=H2O。请举个例子反驳上述观点(用离子方程式表示)_____________ 。
Ⅰ.现有以下物质:①H2O ②Cu ③BaCO3 ④Fe(OH)3胶体 ⑤酒精 ⑥CO2 ⑦稀硫酸
(1)以上物质中属于混合物的是
(2)向④中逐滴滴加⑦,可观察到的现象是
Ⅱ.虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
(3)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

(4)有同学认为所有酸碱中和反应均可表示为H++OH-=H2O。请举个例子反驳上述观点(用离子方程式表示)
更新时间:2019-12-19 19:17:28
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有下列10种物质:①铁② ③
③ 溶液④浓盐酸⑤氨气⑥
溶液④浓盐酸⑤氨气⑥ 固体⑦熔融的
固体⑦熔融的 ⑧
⑧ 固体⑨高锰酸钾粉末⑩氢氧化铁胶体。回答下列问题:
固体⑨高锰酸钾粉末⑩氢氧化铁胶体。回答下列问题:
(1)上述物质中能导电的有___________ (填序号,下同);属于电解质的有___________ 。
(2) 不但是日常生活中的调味品,也是一种重要的工业原料;工业上常采用电解饱和食盐水的方法生产
不但是日常生活中的调味品,也是一种重要的工业原料;工业上常采用电解饱和食盐水的方法生产 ,同时得到两种副产品
,同时得到两种副产品 和
和 ,写出电解饱和食盐水的离子方程式:
,写出电解饱和食盐水的离子方程式:___________ 。
(3) 在熔融时的电离方程式为:
在熔融时的电离方程式为:___________ 。将 溶液逐滴加入
溶液逐滴加入 溶液中至溶液呈中性,反应的离子方程式为
溶液中至溶液呈中性,反应的离子方程式为___________ 。
(4) 和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表示为:
和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表示为: ,
,
①请用“双线桥”表示上述反应电子转移的方向和数目___________ 。
②浓盐酸在反应中显示出来的性质是___________ 。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(5) 是三元弱酸,磷还有一种含氧酸叫亚磷酸
是三元弱酸,磷还有一种含氧酸叫亚磷酸 ,它是一种二元弱酸,则
,它是一种二元弱酸,则 为
为________ (填“正盐”或“酸式盐”),写出 与足量
与足量 溶液反应的化学方程式
溶液反应的化学方程式________ 。
 ③
③ 溶液④浓盐酸⑤氨气⑥
溶液④浓盐酸⑤氨气⑥ 固体⑦熔融的
固体⑦熔融的 ⑧
⑧ 固体⑨高锰酸钾粉末⑩氢氧化铁胶体。回答下列问题:
固体⑨高锰酸钾粉末⑩氢氧化铁胶体。回答下列问题:(1)上述物质中能导电的有
(2)
 不但是日常生活中的调味品,也是一种重要的工业原料;工业上常采用电解饱和食盐水的方法生产
不但是日常生活中的调味品,也是一种重要的工业原料;工业上常采用电解饱和食盐水的方法生产 ,同时得到两种副产品
,同时得到两种副产品 和
和 ,写出电解饱和食盐水的离子方程式:
,写出电解饱和食盐水的离子方程式:(3)
 在熔融时的电离方程式为:
在熔融时的电离方程式为: 溶液逐滴加入
溶液逐滴加入 溶液中至溶液呈中性,反应的离子方程式为
溶液中至溶液呈中性,反应的离子方程式为(4)
 和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表示为:
和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表示为: ,
,①请用“双线桥”表示上述反应电子转移的方向和数目
②浓盐酸在反应中显示出来的性质是
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(5)
 是三元弱酸,磷还有一种含氧酸叫亚磷酸
是三元弱酸,磷还有一种含氧酸叫亚磷酸 ,它是一种二元弱酸,则
,它是一种二元弱酸,则 为
为 与足量
与足量 溶液反应的化学方程式
溶液反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】金属及其化合物在许多领域有着广泛的应用。
①绿矾 是一种良好的絮凝剂。将绿矾溶于水后,加入适量NaOH溶液可观察到的现象为
是一种良好的絮凝剂。将绿矾溶于水后,加入适量NaOH溶液可观察到的现象为___________ ;若将少量 固体加入
固体加入 溶液中,发生的反应为
溶液中,发生的反应为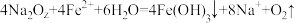 ,反应中被氧化的元素为
,反应中被氧化的元素为___________ (填元素符号)
(2)“钢是虎,钒是翼,钢含钒犹如虎添翼”,钒是“现代工业味精”, 是两性氧化物,与强碱反应生成钒酸盐(阴离子为
是两性氧化物,与强碱反应生成钒酸盐(阴离子为 ),溶于强酸生成含钒氧离子(
),溶于强酸生成含钒氧离子( )的盐。请写出
)的盐。请写出 分别与烧碱溶液和稀硫酸反应生成的盐的化学式:
分别与烧碱溶液和稀硫酸反应生成的盐的化学式:___________ 、___________ 。
(3)科学研究表明,向 和
和 的混合溶液中加入适量KOH,在一定条件下可制得化学式通式为
的混合溶液中加入适量KOH,在一定条件下可制得化学式通式为 的特殊磁流体材料。
的特殊磁流体材料。
①在加热条件下,请写出生成难溶于水的 的化学方程式:
的化学方程式:___________ 。
②若 ,则
,则 中
中 和
和 的物质的量之比为
的物质的量之比为___________ 。
①绿矾
 是一种良好的絮凝剂。将绿矾溶于水后,加入适量NaOH溶液可观察到的现象为
是一种良好的絮凝剂。将绿矾溶于水后,加入适量NaOH溶液可观察到的现象为 固体加入
固体加入 溶液中,发生的反应为
溶液中,发生的反应为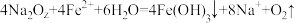 ,反应中被氧化的元素为
,反应中被氧化的元素为(2)“钢是虎,钒是翼,钢含钒犹如虎添翼”,钒是“现代工业味精”,
 是两性氧化物,与强碱反应生成钒酸盐(阴离子为
是两性氧化物,与强碱反应生成钒酸盐(阴离子为 ),溶于强酸生成含钒氧离子(
),溶于强酸生成含钒氧离子( )的盐。请写出
)的盐。请写出 分别与烧碱溶液和稀硫酸反应生成的盐的化学式:
分别与烧碱溶液和稀硫酸反应生成的盐的化学式:(3)科学研究表明,向
 和
和 的混合溶液中加入适量KOH,在一定条件下可制得化学式通式为
的混合溶液中加入适量KOH,在一定条件下可制得化学式通式为 的特殊磁流体材料。
的特殊磁流体材料。①在加热条件下,请写出生成难溶于水的
 的化学方程式:
的化学方程式:②若
 ,则
,则 中
中 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】将下列对应物质的序号填写在下列恰当的空白处
①CO2 ②HCl ③NaOH ④Na2O2 ⑤Cu2(OH)2CO3 ⑥Mg(OH)2 ⑦NH4HCO3 ⑧MgCl2 ⑨H2SO4 ⑩Na2O
(1)属于酸的是________ 、属于含氧酸的是________ 、属于无氧酸的是_________ 。
(2)属于碱的是___________ 。
(3)属于盐的是___________ 、属于碱式盐的是___________ 、属于镁盐的是___________ 、属于碳酸盐的是___________ 。
(4)属于金属氧化物的是___________ 、属于非金属氧化物的是___________ 、属于强酸的是___________ 、属于铵盐的是___________ 。
①CO2 ②HCl ③NaOH ④Na2O2 ⑤Cu2(OH)2CO3 ⑥Mg(OH)2 ⑦NH4HCO3 ⑧MgCl2 ⑨H2SO4 ⑩Na2O
(1)属于酸的是
(2)属于碱的是
(3)属于盐的是
(4)属于金属氧化物的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。
Ⅰ.现有以下物质:① ②Cu ③
②Cu ③ ④
④ 胶体 ⑤酒精 ⑥
胶体 ⑤酒精 ⑥ ⑦稀硫酸
⑦稀硫酸
(1)以上物质中属于混合物的是___________ (填序号,下同),属于电解质的是___________ 。
Ⅱ.虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
(2)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是___________ (填字母)。

(3)有同学认为所有强酸强碱中和反应均可表示为 。请举个例子反驳上述观点(用离子方程式表示):
。请举个例子反驳上述观点(用离子方程式表示):___________ 。
Ⅰ.现有以下物质:①
 ②Cu ③
②Cu ③ ④
④ 胶体 ⑤酒精 ⑥
胶体 ⑤酒精 ⑥ ⑦稀硫酸
⑦稀硫酸(1)以上物质中属于混合物的是
Ⅱ.虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
(2)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

(3)有同学认为所有强酸强碱中和反应均可表示为
 。请举个例子反驳上述观点(用离子方程式表示):
。请举个例子反驳上述观点(用离子方程式表示):
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有下列几种物质:① 晶体;②
晶体;② ;③
;③ 溶液;④
溶液;④ ;⑤
;⑤ 溶液;⑥
溶液;⑥ (酒精);⑦
(酒精);⑦ ;⑧氨水;⑨饱和
;⑧氨水;⑨饱和 溶液。根据要求回答下列问题:
溶液。根据要求回答下列问题:
1.上述各物质属于强电解质的是___________ (填物质编号,下同);属于非电解质的是___________ 。
2.写出少量④通入⑤中反应的离子方程式:___________ ;③和⑧在水溶液中反应的离子方程式:___________ 。
3.将⑨加入到沸水中,继续加热溶液呈红褐色,制得 胶体,该反应的离子方程式:
胶体,该反应的离子方程式:___________ 。
4.向③中加入⑤至溶液中恰好呈中性,写出该反应的离子方程式:___________ 。
 晶体;②
晶体;② ;③
;③ 溶液;④
溶液;④ ;⑤
;⑤ 溶液;⑥
溶液;⑥ (酒精);⑦
(酒精);⑦ ;⑧氨水;⑨饱和
;⑧氨水;⑨饱和 溶液。根据要求回答下列问题:
溶液。根据要求回答下列问题:1.上述各物质属于强电解质的是
2.写出少量④通入⑤中反应的离子方程式:
3.将⑨加入到沸水中,继续加热溶液呈红褐色,制得
 胶体,该反应的离子方程式:
胶体,该反应的离子方程式:4.向③中加入⑤至溶液中恰好呈中性,写出该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有下列物质:① ;②熔融NaCl;③
;②熔融NaCl;③ ;④
;④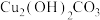 ;⑤液态氯化氢;⑥澄清石灰水;⑦
;⑤液态氯化氢;⑥澄清石灰水;⑦ ;⑧Zn。回答下列问题:
;⑧Zn。回答下列问题:
(1)以上物质中属于电解质的是_____ (填序号,下同),属于非电解质的是_____ ,属于盐的是_____ 。
(2)写出物质③溶于水的电离方程式_____ ;写出⑧加入③的水溶液中发生反应的离子方程式_____ 。
(3)写出少量⑦通入⑥中发生反应的离子方程式_____ 。
(4)根据交叉分类法,④属于_____ (填字母标号)。
A.酸 B.碱 C.铜盐 D.碱式盐 E.碳酸盐 F.混合物
 ;②熔融NaCl;③
;②熔融NaCl;③ ;④
;④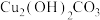 ;⑤液态氯化氢;⑥澄清石灰水;⑦
;⑤液态氯化氢;⑥澄清石灰水;⑦ ;⑧Zn。回答下列问题:
;⑧Zn。回答下列问题:(1)以上物质中属于电解质的是
(2)写出物质③溶于水的电离方程式
(3)写出少量⑦通入⑥中发生反应的离子方程式
(4)根据交叉分类法,④属于
A.酸 B.碱 C.铜盐 D.碱式盐 E.碳酸盐 F.混合物
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.现有下列几种物质:①盐酸 ②石墨 ③酒精 ④SO2 ⑤熔融KHSO4 ⑥Ba(OH)2固体 ⑦氨水⑧硝酸
(1)属于强电解质的有_____________ ;属于非电解质的有_____________ 。(填序号)
(2)⑧和铜在一定条件下可发生如下反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,酸性介质与氧化剂的物质的量之比为________ ;请用双线桥法分析电子转移方向和数目_______ 。
Ⅱ.向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
(1)写出反应的离子方程式___________________________________________ 。
(2)下列三种情况下,离子方程式与(1)相同的是______ (填字母)。
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
(3)若缓缓加入稀硫酸至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用下图中的______ 曲线表示(填字母)。
(1)属于强电解质的有
(2)⑧和铜在一定条件下可发生如下反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,酸性介质与氧化剂的物质的量之比为
Ⅱ.向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
(1)写出反应的离子方程式
(2)下列三种情况下,离子方程式与(1)相同的是
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
(3)若缓缓加入稀硫酸至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用下图中的

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】金属及其化合物在生产生活中占有极其重要的地位,请结合金属及其化合物的相关知识回答下列问题。
(1)含碳量在0.03%~2%之间某合金,是目前使用量最大的合金,这种合金是_______。
(2)FeCl3溶液用于腐蚀铜箔印刷线路板,反应的离子方程式为_______ 。
(3)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入足量的Na2O2后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是 (填字母)
(4)Fe(NO3)3的高纯度结晶体是一种紫色潮解性固体,适合于制磁性氧化铁纳米粉末,工业上用废铁屑(含Fe和Fe2O3及其它不反应的物质)制取Fe(NO3)3晶体的方法如下:

①第1步反应若温度过高,将导致硝酸分解,浓硝酸受热分解的化学方程式为_____ 。
②磁性氧化铁的化学式为_____ ,试写出Fe2O3与硝酸反应的离子方程式_____ 。
③操作1的名称为_____ ,操作2的步骤为:_____ ,过滤,洗涤。
(1)含碳量在0.03%~2%之间某合金,是目前使用量最大的合金,这种合金是_______。
| A.铝合金 | B.青铜 | C.镁合金 | D.钢 |
(3)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入足量的Na2O2后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是 (填字母)
| A.Mg2+ | B.Fe2+ | C.Al3+ | D.Cu2+ |

①第1步反应若温度过高,将导致硝酸分解,浓硝酸受热分解的化学方程式为
②磁性氧化铁的化学式为
③操作1的名称为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】以下是与绿色化学、环境保护和人类健康息息相关的三个主题,请根据已知信息回答下列问题:
(1)下列制备氯乙烷的反应中原子经济性最高的是_____ (填字母)。
A.CH2=CH2+HCl→CH3CH2Cl
B.CH3CH2OH+HCl CH3CH2Cl+H2O
CH3CH2Cl+H2O
C.CH3CH3+Cl2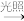 CH3CH2Cl+HCl
CH3CH2Cl+HCl
D.CH2=CHCl+H2 CH3CH2Cl
CH3CH2Cl
由上述四个反应可归纳出,原子经济性最高的是______ (填反应类型)。
(2)有毒物质的无害化处理也是绿色化学研究的内容之一。ClO2是一种性能优良的消毒剂,它可将废水中少量的CN-等有毒的酸根离子氧化而除去。请写出用ClO2将废水中的CN-氧化成无毒气体的离子方程式:______ ,该方法的优点是_______ 。
(3)某饮用水厂由天然水制备纯净水(去离子水)的工艺流程示意图如图:
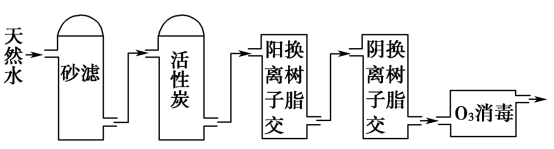
活性炭的作用是_______ ;O3消毒的优点是_______ 。
(1)下列制备氯乙烷的反应中原子经济性最高的是
A.CH2=CH2+HCl→CH3CH2Cl
B.CH3CH2OH+HCl
 CH3CH2Cl+H2O
CH3CH2Cl+H2OC.CH3CH3+Cl2
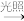 CH3CH2Cl+HCl
CH3CH2Cl+HClD.CH2=CHCl+H2
 CH3CH2Cl
CH3CH2Cl由上述四个反应可归纳出,原子经济性最高的是
(2)有毒物质的无害化处理也是绿色化学研究的内容之一。ClO2是一种性能优良的消毒剂,它可将废水中少量的CN-等有毒的酸根离子氧化而除去。请写出用ClO2将废水中的CN-氧化成无毒气体的离子方程式:
(3)某饮用水厂由天然水制备纯净水(去离子水)的工艺流程示意图如图:

活性炭的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
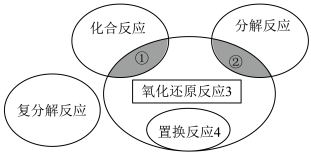
(1)氧化还原反应与四种基本类型反应的关系如图,则下列化学反应属于区域3的反应是 (填序号)。
(2)高锰酸钾和氢溴酸溶液可以发生如下反应: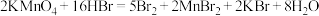 。
。
①其中_______ 元素被氧化(填化学式,下同),_______ 作氧化剂。
②参加反应的 体现出
体现出_______ 性和_______ 性。
③用“双线桥”标出该方程式电子转移的方向和数目:_______ 。
④当反应转移的电子数为15个时,有_______ 个 参与了该化学反应。
参与了该化学反应。
(3)写出下列氧化还原反应方程式或离子方程式:
①在海水提取溴的工艺中,溴气与二氧化硫同时通入水中可以得到一种含氧酸与一种无氧酸。化学方程式:_______ 。
②工业废水中的 有毒,常在酸性条件下用
有毒,常在酸性条件下用 做处理剂,将
做处理剂,将 转化为
转化为 。离子方程式:
。离子方程式:_______ 。
③酸性高锰酸钾溶液与过氧化氢混合可以得到氧气, 只发生了如下过程:
只发生了如下过程: 。离子方程式:
。离子方程式:_______ 。
(1)氧化还原反应与四种基本类型反应的关系如图,则下列化学反应属于区域3的反应是 (填序号)。

A. | B.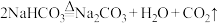 |
C. | D. |
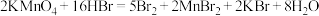 。
。①其中
②参加反应的
 体现出
体现出③用“双线桥”标出该方程式电子转移的方向和数目:
④当反应转移的电子数为15个时,有
 参与了该化学反应。
参与了该化学反应。(3)写出下列氧化还原反应方程式或离子方程式:
①在海水提取溴的工艺中,溴气与二氧化硫同时通入水中可以得到一种含氧酸与一种无氧酸。化学方程式:
②工业废水中的
 有毒,常在酸性条件下用
有毒,常在酸性条件下用 做处理剂,将
做处理剂,将 转化为
转化为 。离子方程式:
。离子方程式:③酸性高锰酸钾溶液与过氧化氢混合可以得到氧气,
 只发生了如下过程:
只发生了如下过程: 。离子方程式:
。离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按化学反应中元素化合价是否发生变化,无机反应可以分为氧化还原反应和非氧化还原反应。这种分类方法与将无机反应按反应形式的不同分为四种基本反应类型是完全不同的分类方式,这二者的关系如图。

图中方框内区域表示所有的化学反应,大圆内区域表示氧化还原反应,大圆外区域表示非氧化还原反应,其中A~D分别表示四种基本反应类型。请分别填出:
(1)化学反应可以分为哪四种基本反应类型:___ 、___ 、___ 、___ 。
(2)若图中B圈表示化合反应,则:
B圈与氧化还原反应重叠的阴影部分表示哪一类反应?___________ ;
C圈与氧化还原反应重叠的阴影部分表示哪一类反应?______________ ;
请分别举出符合以上两种情况的一个例子:________ ; ___________ 。
(3)下列说法正确的是___ 。
A.置换反应一定属于氧化还原反应
B.有单质参加和有单质生成的化学反应一定是氧化还原反应
C.化学反应中有一种物质被氧化,必定有另外一种物质被还原
D.氧化还原反应发生的本质是化合价发生了变化

图中方框内区域表示所有的化学反应,大圆内区域表示氧化还原反应,大圆外区域表示非氧化还原反应,其中A~D分别表示四种基本反应类型。请分别填出:
(1)化学反应可以分为哪四种基本反应类型:
(2)若图中B圈表示化合反应,则:
B圈与氧化还原反应重叠的阴影部分表示哪一类反应?
C圈与氧化还原反应重叠的阴影部分表示哪一类反应?
请分别举出符合以上两种情况的一个例子:
(3)下列说法正确的是
A.置换反应一定属于氧化还原反应
B.有单质参加和有单质生成的化学反应一定是氧化还原反应
C.化学反应中有一种物质被氧化,必定有另外一种物质被还原
D.氧化还原反应发生的本质是化合价发生了变化
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】水是生命之源,与生活生产关系密切。保护水环境、珍爱水资源,是每个公民应尽的责任和义务。
(1)“四种基本反应类型与氧化还原反应的关系”可用如图表达。

试写出有水参加的符合反应类型Ⅳ的一个化学方程式:____________________________ ,其中水为________ 剂。
(2)为了防止水的污染,下列做法有利于保护水资源的是__________ (填编号)。
①抑制水中所有动、植物的生长; ②不任意排放工业废水;
③大量使用化肥农药; ④生活污水经过净化处理后再排放。
(3)天然水中含有许多杂质,自来水生产过程中,常用过滤的方法除去水中悬浮的杂质,同时还必须进行消毒。氯气是最早用于饮用水消毒的物质,氯气进行自来水消毒时,该反应的离子方程式为______________________________ 。
已知亚铁盐是常见的还原剂,多余的氯气可用绿矾(FeSO4·7H2O)吸收,反应的离子方程式为________________________________________ 。
(4)用氯气消毒的水可能有臭味,长期饮用还可能对人造成潜在危害;ClO2是一种消毒杀菌效率高、二次污染小的水处理剂,工业上可用SO2与NaClO3溶液反应制得,反应方程式为SO2 + 2NaClO3== Na2SO4+ 2ClO2。
①NaClO3中Cl元素的化合价为__________
②该反应过程中,氧化剂和还原剂的物质的量之比为__________ 。
(5)漂白粉也可用于饮用水、游泳池水等的杀菌和消毒,工业上利用氯气和氢氧化钙反应可制得漂白粉,其化学方程式为____________________________________ 。
(1)“四种基本反应类型与氧化还原反应的关系”可用如图表达。

试写出有水参加的符合反应类型Ⅳ的一个化学方程式:
(2)为了防止水的污染,下列做法有利于保护水资源的是
①抑制水中所有动、植物的生长; ②不任意排放工业废水;
③大量使用化肥农药; ④生活污水经过净化处理后再排放。
(3)天然水中含有许多杂质,自来水生产过程中,常用过滤的方法除去水中悬浮的杂质,同时还必须进行消毒。氯气是最早用于饮用水消毒的物质,氯气进行自来水消毒时,该反应的离子方程式为
已知亚铁盐是常见的还原剂,多余的氯气可用绿矾(FeSO4·7H2O)吸收,反应的离子方程式为
(4)用氯气消毒的水可能有臭味,长期饮用还可能对人造成潜在危害;ClO2是一种消毒杀菌效率高、二次污染小的水处理剂,工业上可用SO2与NaClO3溶液反应制得,反应方程式为SO2 + 2NaClO3== Na2SO4+ 2ClO2。
①NaClO3中Cl元素的化合价为
②该反应过程中,氧化剂和还原剂的物质的量之比为
(5)漂白粉也可用于饮用水、游泳池水等的杀菌和消毒,工业上利用氯气和氢氧化钙反应可制得漂白粉,其化学方程式为
您最近一年使用:0次



