现有下列物质:① ;②熔融NaCl;③
;②熔融NaCl;③ ;④
;④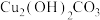 ;⑤液态氯化氢;⑥澄清石灰水;⑦
;⑤液态氯化氢;⑥澄清石灰水;⑦ ;⑧Zn。回答下列问题:
;⑧Zn。回答下列问题:
(1)以上物质中属于电解质的是_____ (填序号,下同),属于非电解质的是_____ ,属于盐的是_____ 。
(2)写出物质③溶于水的电离方程式_____ ;写出⑧加入③的水溶液中发生反应的离子方程式_____ 。
(3)写出少量⑦通入⑥中发生反应的离子方程式_____ 。
(4)根据交叉分类法,④属于_____ (填字母标号)。
A.酸 B.碱 C.铜盐 D.碱式盐 E.碳酸盐 F.混合物
 ;②熔融NaCl;③
;②熔融NaCl;③ ;④
;④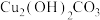 ;⑤液态氯化氢;⑥澄清石灰水;⑦
;⑤液态氯化氢;⑥澄清石灰水;⑦ ;⑧Zn。回答下列问题:
;⑧Zn。回答下列问题:(1)以上物质中属于电解质的是
(2)写出物质③溶于水的电离方程式
(3)写出少量⑦通入⑥中发生反应的离子方程式
(4)根据交叉分类法,④属于
A.酸 B.碱 C.铜盐 D.碱式盐 E.碳酸盐 F.混合物
更新时间:2023-10-21 11:20:03
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】以下十种物质 ①Na2O2;②二氧化碳;③氯化钠溶液;④NaOH固体;⑤氯化氢;⑥氯化铵;⑦硫酸氢钠;⑧蔗糖;⑨铜; ⑩氖。
(1)以上属于非电解质的是_______ (填序号)
(2)⑦溶于水,被破坏的是_______ 。
(3)②的电子式为_______ ;⑥的电子式为 _______
(4)配制90mL 0.500mol/L④的溶液,除烧杯、量筒、玻璃棒外还需的玻璃仪器是_______ ,需要称量④的质量为_______ g (保留三位有效数字)。
(1)以上属于非电解质的是
(2)⑦溶于水,被破坏的是
(3)②的电子式为
(4)配制90mL 0.500mol/L④的溶液,除烧杯、量筒、玻璃棒外还需的玻璃仪器是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有下列物质:①Fe2(SO4)3溶液 ②酒精 ③二氧化硫 ④铜 ⑤过氧化钠 ⑥FeSO4溶液 ⑦CuO ⑧漂白粉,回答下列问题:
(1)在表格空白处填写符合条件物质的序号
(2)从上述物质中选择试剂,证明氧化性Fe3+>Cu2+:_______ (用离子方程式表示)。
(3)⑥中混有少量的①,除杂过程中选用的试剂和操作方法为_________ 。
(4)将1.12g铁粉加入25mL2 mol•L-1的①中,充分反应后溶液中n(Fe3+)∶n(Fe2+)=______ 。
(5)设计实验证明某溶液含有①、⑥中的两种阳离子_________ 。
(1)在表格空白处填写符合条件物质的序号
| 条件 | 序号 |
| 能导电 | |
| 属于碱性氧化物 | |
| 属于电解质 |
(2)从上述物质中选择试剂,证明氧化性Fe3+>Cu2+:
(3)⑥中混有少量的①,除杂过程中选用的试剂和操作方法为
(4)将1.12g铁粉加入25mL2 mol•L-1的①中,充分反应后溶液中n(Fe3+)∶n(Fe2+)=
(5)设计实验证明某溶液含有①、⑥中的两种阳离子
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】结合本节学习内容,完成下列题目。
(1)列举一些你熟悉的电解质_______ 。
(2)在KCl溶液、AgNO3溶液中大量存在的微粒分别有哪些_______ ?
(3)将KCl溶液与AgNO3溶液混合,分析KCl溶液与AgNO3溶液反应的实质,写出该反应的离子方程式_______ 。
(4)离子方程式可以表示一类化学反应。请列举2~3个与上述反应实质相同的化学反应_______ 。
(5)请从多个角度谈谈你对酸、碱、盐以及酸、碱、盐之间反应关系的认识_______ 。
(1)列举一些你熟悉的电解质
(2)在KCl溶液、AgNO3溶液中大量存在的微粒分别有哪些
(3)将KCl溶液与AgNO3溶液混合,分析KCl溶液与AgNO3溶液反应的实质,写出该反应的离子方程式
(4)离子方程式可以表示一类化学反应。请列举2~3个与上述反应实质相同的化学反应
(5)请从多个角度谈谈你对酸、碱、盐以及酸、碱、盐之间反应关系的认识
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】随着生活水平的提高,人们越来越关注营养平衡和自身健康。
(1)人体内缺乏某种微量元素会导致贫血,该元素是________ ;可为人体提供能量的物质有糖类,______________ 和________________ 。
(2)以下描述正确的是__________ (填字母代号,下同)。
A.食品添加剂可以改变食品的某些性质,如颜色和口感等,因此使用时 不必考虑用量
B.青霉素是一种天然抗生素,因此使用时可以不必做皮肤过敏试验
C.误服重金属盐中毒后,可服用鸡蛋清、生牛奶等缓解中毒症状
D.医用维生素C片常在药片外包裹上一层“糖衣”,主要是为了改善口感
(3)下列药物中属于抑酸剂的是___________________ 。
A.胃舒平 B.阿司匹林 C.青霉素
其有效成分发生作用的离子方程式为____________ 。
(1)人体内缺乏某种微量元素会导致贫血,该元素是
(2)以下描述正确的是
A.食品添加剂可以改变食品的某些性质,如颜色和口感等,因此使用时 不必考虑用量
B.青霉素是一种天然抗生素,因此使用时可以不必做皮肤过敏试验
C.误服重金属盐中毒后,可服用鸡蛋清、生牛奶等缓解中毒症状
D.医用维生素C片常在药片外包裹上一层“糖衣”,主要是为了改善口感
(3)下列药物中属于抑酸剂的是
A.胃舒平 B.阿司匹林 C.青霉素
其有效成分发生作用的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】肼(N2H4)是一种重要的液态火箭燃料,具有弱碱性和强还原性.工业上利用尿素[CO(NH2)2]、NaClO在NaOH溶液中发生反应生成水合肼(N2H4•H2O)、Na2CO3等产物.请回答:
(1)上述生成水合肼的反应中尿素是________ ( 填“氧化剂”或“还原剂”),反应的化学方程式为________ .
(2)肼与盐酸反应可生成N2H6Cl2 , N2H6Cl2的水溶液显________ 性( 填“酸”或“碱”或“中”),用离子方程式表示其原因________ .
(3)查资料得,在高温下肼可将锅炉内壁表面的铁锈转化为致密的氧化膜.取3.2g肼与96g该铁锈样品(可看作是Fe2O3)在高温下恰好完全反应生成氮气等产物,写出该反应的化学方程式________ .
若要设计实验方案检验上述反应生成固体产物中的金属阳离子,补充完整下列实验步骤:
①所得固体溶入浓盐酸中; ②________
(1)上述生成水合肼的反应中尿素是
(2)肼与盐酸反应可生成N2H6Cl2 , N2H6Cl2的水溶液显
(3)查资料得,在高温下肼可将锅炉内壁表面的铁锈转化为致密的氧化膜.取3.2g肼与96g该铁锈样品(可看作是Fe2O3)在高温下恰好完全反应生成氮气等产物,写出该反应的化学方程式
若要设计实验方案检验上述反应生成固体产物中的金属阳离子,补充完整下列实验步骤:
①所得固体溶入浓盐酸中; ②
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】为在冬奥会期间营造良好环境,京津冀地区开展秋冬季大气污染综合治理攻坚行动,取得显著成效。已知氮氧化物(NO、NO2)、SO2是大气污染物。回答下列问题:
(1)以上污染物会造成的环境问题有____ (写一种即可)。
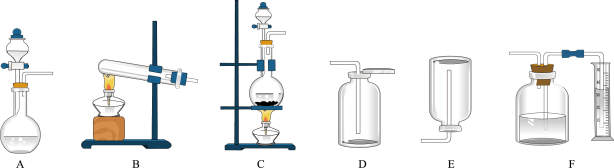
(2)如图包含气体发生装置和收集装置(部分装置的夹持仪器已省略),实验室以Cu与浓HNO3反应制备并收集NO2,应选择的装置是____ (填字母)。
(3)SCR脱硝技术已成为使用广泛和成熟的烟气净化技术,脱硝效率高达90%以上。催化反应机理如图所示,写出该反应发生的化学方程式:____ 。

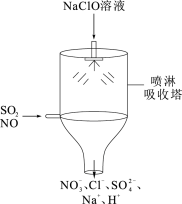
(4)目前,NaClO溶液广泛地应用于脱硫脱硝。某课外小组同学设计了如图喷淋吸收塔装置(如图)。设计该装置的优点是____ ,脱硝(NO)反应的离子方程式为____ 。
(5)某兴趣小组用Fe2(SO4)3溶液吸收含SO2的尾气(SO2的体积分数约10%,其余为空气),实验装置如图所示:

①装置A中用Fe2(SO4)3溶液吸收SO2反应的离子方程式:____ 。
②反应后,若要检验SO2是否过量,可用试剂为____ 。
(1)以上污染物会造成的环境问题有
(2)如图包含气体发生装置和收集装置(部分装置的夹持仪器已省略),实验室以Cu与浓HNO3反应制备并收集NO2,应选择的装置是

(3)SCR脱硝技术已成为使用广泛和成熟的烟气净化技术,脱硝效率高达90%以上。催化反应机理如图所示,写出该反应发生的化学方程式:

(4)目前,NaClO溶液广泛地应用于脱硫脱硝。某课外小组同学设计了如图喷淋吸收塔装置(如图)。设计该装置的优点是

(5)某兴趣小组用Fe2(SO4)3溶液吸收含SO2的尾气(SO2的体积分数约10%,其余为空气),实验装置如图所示:

①装置A中用Fe2(SO4)3溶液吸收SO2反应的离子方程式:
②反应后,若要检验SO2是否过量,可用试剂为
您最近一年使用:0次



