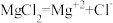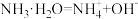结合本节学习内容,完成下列题目。
(1)列举一些你熟悉的电解质_______ 。
(2)在KCl溶液、AgNO3溶液中大量存在的微粒分别有哪些_______ ?
(3)将KCl溶液与AgNO3溶液混合,分析KCl溶液与AgNO3溶液反应的实质,写出该反应的离子方程式_______ 。
(4)离子方程式可以表示一类化学反应。请列举2~3个与上述反应实质相同的化学反应_______ 。
(5)请从多个角度谈谈你对酸、碱、盐以及酸、碱、盐之间反应关系的认识_______ 。
(1)列举一些你熟悉的电解质
(2)在KCl溶液、AgNO3溶液中大量存在的微粒分别有哪些
(3)将KCl溶液与AgNO3溶液混合,分析KCl溶液与AgNO3溶液反应的实质,写出该反应的离子方程式
(4)离子方程式可以表示一类化学反应。请列举2~3个与上述反应实质相同的化学反应
(5)请从多个角度谈谈你对酸、碱、盐以及酸、碱、盐之间反应关系的认识
更新时间:2022-11-25 22:21:52
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】价类二维图是以元素化合价为纵坐标,以物质类别为横坐标的二维平面图像。如图为氯元素价类二维图,据此回答下列问题:

(1)根据化合价和物质类别写出有关物质的化学式:①HCl、②Cl2、③________ 、④_______ 、⑤NaCl、⑥NaClO。
(2)工业上用水吸收HCl气体来生产质量分数为36.5%、密度为1.19g/mL的盐酸,该盐酸的物质的量浓度为_______ ;若用该盐酸配制220mL0.5mol•L-1稀盐酸除玻璃棒、胶头滴管还需用到_______ (填字母)。
a.10mL量筒 b.20mL量筒 c.100mL容量瓶 d.250mL容量瓶
(3)用NaOH溶液吸收②Cl2可制备某漂白液。已知1molCl2可反应生成等物质的量的NaCl和NaClO,则该反应化学方程式为:_______ ;NaClO在水溶液中的电离方程式为:_______ 。
(4)已知:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。实验室用8.7gMnO2(Mr为87)与100mL11.9mol•L-1盐酸混合共热,若MnO2完全反应则生成Cl2在标准状况下的体积为
MnCl2+Cl2↑+2H2O。实验室用8.7gMnO2(Mr为87)与100mL11.9mol•L-1盐酸混合共热,若MnO2完全反应则生成Cl2在标准状况下的体积为_______ ,反应消耗HCl的物质的量为_______ ,反应后溶液中c(Cl-)为_______ (溶液的体积变化忽略不计)。

(1)根据化合价和物质类别写出有关物质的化学式:①HCl、②Cl2、③
(2)工业上用水吸收HCl气体来生产质量分数为36.5%、密度为1.19g/mL的盐酸,该盐酸的物质的量浓度为
a.10mL量筒 b.20mL量筒 c.100mL容量瓶 d.250mL容量瓶
(3)用NaOH溶液吸收②Cl2可制备某漂白液。已知1molCl2可反应生成等物质的量的NaCl和NaClO,则该反应化学方程式为:
(4)已知:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O。实验室用8.7gMnO2(Mr为87)与100mL11.9mol•L-1盐酸混合共热,若MnO2完全反应则生成Cl2在标准状况下的体积为
MnCl2+Cl2↑+2H2O。实验室用8.7gMnO2(Mr为87)与100mL11.9mol•L-1盐酸混合共热,若MnO2完全反应则生成Cl2在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】从物质分类的角度指出下列各组物质中与其他物质类型不同的一种物质:
(1)Na2O CaO SO2 CuO_______ 。
(2)NaCl KCl NaClO3 CaCl2_______ 。
(3)HClO3 KClO3 HCl NaClO3_______ 。
(4)NaHCO3 Ca(HCO3)2 NH4HCO3 K2CO3_______ 。
(5)NaClO、HClO、KClO3、Cl2:_______ 。
(1)Na2O CaO SO2 CuO
(2)NaCl KCl NaClO3 CaCl2
(3)HClO3 KClO3 HCl NaClO3
(4)NaHCO3 Ca(HCO3)2 NH4HCO3 K2CO3
(5)NaClO、HClO、KClO3、Cl2:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】对于数以千万计的化学物质和如此丰富的化学变化,分类法的作用几乎是无可替代的。已知有下列物质:
①熔融CaO ②Na ③干冰 ④Ca(OH)2固体 ⑤酒精(C2H5OH) ⑥小苏打粉末 ⑦稀硫酸 ⑧稀氨水 ⑨有色玻璃 ⑩稀醋酸
请回答:
(1)属于盐的有___________ (填序号,下同),属于酸性氧化物的有___________ ,属于胶体的有___________ 。
(2)电解质有___________ ,非电解质有___________ ,能导电的电解质有___________ 。
(3)通常情况下,在弱酸及弱碱的稀溶液中,弱酸、弱碱的电离程度均较小。据此可判断,向⑩中逐滴加入⑧直至过量,溶液的导电能力[电流(I)]随⑧的滴入量[质量(m)]的变化趋势正确的是___________ 。
A.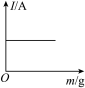 B.
B. 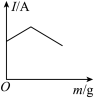 C.
C. 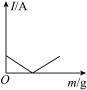
①熔融CaO ②Na ③干冰 ④Ca(OH)2固体 ⑤酒精(C2H5OH) ⑥小苏打粉末 ⑦稀硫酸 ⑧稀氨水 ⑨有色玻璃 ⑩稀醋酸
请回答:
(1)属于盐的有
(2)电解质有
(3)通常情况下,在弱酸及弱碱的稀溶液中,弱酸、弱碱的电离程度均较小。据此可判断,向⑩中逐滴加入⑧直至过量,溶液的导电能力[电流(I)]随⑧的滴入量[质量(m)]的变化趋势正确的是
A.
 B.
B.  C.
C. 
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】人体胃液中含有胃酸( %
%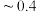 %的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,当胃酸过多时,医生通常用“小苏打片”(主要成分是
%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,当胃酸过多时,医生通常用“小苏打片”(主要成分是 )或“胃舒平”[主要成分是
)或“胃舒平”[主要成分是 ]给病人治疗。
]给病人治疗。
(1)胃酸___________ (填“是”或“不是”,下同)电解质,
___________ 电解质。
(2) 在水中的电离方程式为
在水中的电离方程式为___________ 。
(3)用小苏打片治疗胃酸过多,发生反应的化学方程式为___________ 。
(4)如果病人同时患有胃溃疡,此时最好服用胃舒平,发生反应的离子方程式为___________ 。
 %
%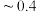 %的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,当胃酸过多时,医生通常用“小苏打片”(主要成分是
%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,当胃酸过多时,医生通常用“小苏打片”(主要成分是 )或“胃舒平”[主要成分是
)或“胃舒平”[主要成分是 ]给病人治疗。
]给病人治疗。(1)胃酸

(2)
 在水中的电离方程式为
在水中的电离方程式为(3)用小苏打片治疗胃酸过多,发生反应的化学方程式为
(4)如果病人同时患有胃溃疡,此时最好服用胃舒平,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下列物质中:①空气 ②氧气 ③食盐水 ④ ⑤铜 ⑥
⑤铜 ⑥ ⑦
⑦ ⑧酒精
⑧酒精
(1)属于电解质的是___________ ;
(2)属于非电解质的是___________ ;
(3)请写出
 在水溶液中的电离方程式
在水溶液中的电离方程式___________ ;
 在水溶液中的电离方程式
在水溶液中的电离方程式___________ ;
 ⑤铜 ⑥
⑤铜 ⑥ ⑦
⑦ ⑧酒精
⑧酒精(1)属于电解质的是
(2)属于非电解质的是
(3)请写出
 在水溶液中的电离方程式
在水溶液中的电离方程式 在水溶液中的电离方程式
在水溶液中的电离方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有下列十种物质:
①H₂②铝 ③CH3COOH ④CO₂ ⑤HCl(g)⑥Ba(OH)₂固体
⑦氨水 ⑧稀硝酸 ⑨熔融Al2(SO₄)₃ ⑩固体 NaHSO₄。
按物质的分类方法回答下列问题(填序号):
(1)属于非电解质的是_______ ;
(2)属于电解质的是_______ ;
(3)能导电的是_______ 。
①H₂②铝 ③CH3COOH ④CO₂ ⑤HCl(g)⑥Ba(OH)₂固体
⑦氨水 ⑧稀硝酸 ⑨熔融Al2(SO₄)₃ ⑩固体 NaHSO₄。
按物质的分类方法回答下列问题(填序号):
(1)属于非电解质的是
(2)属于电解质的是
(3)能导电的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】现有下列十二种物质:①H2 ②铜 ③CaO固体 ④CO2 ⑤H2SO4溶液 ⑥Ba(OH)2⑦熔融的KNO3 ⑧液氨 ⑨稀硝酸 ⑩Al2(SO4)3 ⑪葡萄糖 ⑫FeCl3
(1)⑩在水中的电离方程式为_______
(2)以上属于电解质的共有_______ 种,属于非电解质的是_______ (填序号,下同),能导电的物质有_______ 。
(3)将少量的④通入⑥的溶液中反应的离子方程式:_______ 。上述十二种物质中有两物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学方程式为:_______ 。
(4)将FeCl3的饱和溶液滴入沸水中可以制得Fe(OH)3胶体,写出该化学方程式为:_______ 。
(1)⑩在水中的电离方程式为
(2)以上属于电解质的共有
(3)将少量的④通入⑥的溶液中反应的离子方程式:
(4)将FeCl3的饱和溶液滴入沸水中可以制得Fe(OH)3胶体,写出该化学方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】准确掌握化学基本概念和研究方法是学好化学的重要手段。按要求回答下列问题:
(1)下列是某同学对有关物质进行分类的列表:
每组分类均有错误,其错误的物质分别是___________ 、___________ (填化学式)。
(2)有以下物质:
①熔融氯化钠 ②铝 ③乙醇 ④氨水 ⑤氯化氢气体 ⑥ 固体
固体
i.其中能导电的是___________ (填序号,下同);属于非电解质的是___________ ;属于电解质的是___________ ;属于混合物的是___________ 。
ii.写出物质⑥溶于水时的电离方程式:___________ 。
(3)关于酸、碱、盐的下列各种说法中,正确的是___________(填字母)。
(1)下列是某同学对有关物质进行分类的列表:
| 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| 第一组 |  |  |  |  |
| 第二组 |  |  |  |  |
(2)有以下物质:
①熔融氯化钠 ②铝 ③乙醇 ④氨水 ⑤氯化氢气体 ⑥
 固体
固体i.其中能导电的是
ii.写出物质⑥溶于水时的电离方程式:
(3)关于酸、碱、盐的下列各种说法中,正确的是___________(填字母)。
| A.化合物电离时,生成的阳离子有氢离子的是酸 |
| B.化合物电离时,生成的阴离子有氢氧根离子的是碱 |
| C.化合物电离时,生成金属阳离子(或铵根离子)和酸根离子的是盐 |
| D.酸溶液一定显酸性,碱溶液一定显碱性,盐溶液一定显中性 |
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
名校
【推荐1】用含有A1203、SiO2和少量FeO·xFe2O3的铝灰制备A12(SO4)3·18H2O。,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品。
(1)H2SO4溶解A12O3的离子方程式是_______________ 1;
(2)KMnO4-氧化Fe2+的离子方程式补充完整:______
 1MnO
1MnO +
+ Fe2++
Fe2++ ______=
______= Mn2++
Mn2++ Fe3++
Fe3++ ______
______
(3)已知:
生成氢氧化物沉淀的pH
注:金属离子的起始浓度为0.1mol·L-1
根据表中数据解释步骤Ⅱ的目的:._________________ ;
(4)已知:一定条件下,MnO 可与Mn2+反应生成MnO2,
可与Mn2+反应生成MnO2,
①向Ⅲ的沉淀中加入浓HCI并加热,能说明沉淀中存在MnO2的现象是_____________ ;
②Ⅳ中加入MnSO4的目的是:______________ ;
Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品。
(1)H2SO4溶解A12O3的离子方程式是
(2)KMnO4-氧化Fe2+的离子方程式补充完整:
 1MnO
1MnO +
+ Fe2++
Fe2++ ______=
______= Mn2++
Mn2++ Fe3++
Fe3++ ______
______(3)已知:
生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
根据表中数据解释步骤Ⅱ的目的:.
(4)已知:一定条件下,MnO
 可与Mn2+反应生成MnO2,
可与Mn2+反应生成MnO2,①向Ⅲ的沉淀中加入浓HCI并加热,能说明沉淀中存在MnO2的现象是
②Ⅳ中加入MnSO4的目的是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据条件写出有关反应方程式:
(1)石灰水吸收过量CO2的离子反应方程式:_________________
(2)CuSO4溶液检验H2S气体的离子反应方程式:________________
(3)制备氢氧化铁胶体的化学方程式:______________________
(4)过量的KHCO3与少量石灰乳反应的离子方程式:____________________
(5)稀盐酸除去铜绿[Cu2(OH)2CO3]的化学方程式:__________________
(1)石灰水吸收过量CO2的离子反应方程式:
(2)CuSO4溶液检验H2S气体的离子反应方程式:
(3)制备氢氧化铁胶体的化学方程式:
(4)过量的KHCO3与少量石灰乳反应的离子方程式:
(5)稀盐酸除去铜绿[Cu2(OH)2CO3]的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)元素M的离子与NH4+所含电子数和质子数均相同,则M的原子结构示意图为________ 。
(2)硫酸铝溶液与过量氨水反应的离子方程式为_______________________________ 。
(3)能证明Na2SO3溶液中存在SO32-+H2O⇌HSO3-+OH-水解平衡的事实是________ (填序号)。
A.滴入酚酞溶液变红,再加入H2SO4溶液后红色褪去
B.滴入酚酞溶液变红,再加入氯水后红色褪去
C.滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去
(4)某学生用中和滴定法测定某NaOH溶液的物质的量浓度,选酚酞作指示剂。盛装0.2000 mol/L盐酸标准液应该用______________ 式滴定管;用盐酸滴定待测液NaOH,滴定终点时的颜色变化是_____________ 且30s不变色。
(2)硫酸铝溶液与过量氨水反应的离子方程式为
(3)能证明Na2SO3溶液中存在SO32-+H2O⇌HSO3-+OH-水解平衡的事实是
A.滴入酚酞溶液变红,再加入H2SO4溶液后红色褪去
B.滴入酚酞溶液变红,再加入氯水后红色褪去
C.滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去
(4)某学生用中和滴定法测定某NaOH溶液的物质的量浓度,选酚酞作指示剂。盛装0.2000 mol/L盐酸标准液应该用
您最近一年使用:0次