判断电离方程式的正误并改正。
(1)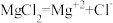
_________ 。
(2)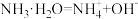
_________ 。
(1)
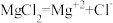
(2)
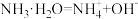
22-23高二上·全国·课时练习 查看更多[1]
(已下线)3.1 电离平衡-同步学习必备知识
更新时间:2022-12-15 18:34:41
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下列物质①NaHSO4、②H2O、③NaOH、④BaSO4、⑤NH3、⑥CO2、⑦CH3COOH、⑧CH3OH、⑨Fe、⑩氯化钠溶液
(1)属于非电解质的是______ ;属于强电解质的是______ ;既不是电解质也不是非电解质,且常温下能导电的物质是______ (均填序号)。
(2)已知碳酸、亚硫酸、次氯酸的电离平衡常数如下表。
①写出H2SO3的第二步电离方程式______ 。
②试比较 、
、 和HCIO的酸性强弱:
和HCIO的酸性强弱:______ 。
③写出少量CO2与NaClO反应的离子方程式______ 。
(1)属于非电解质的是
(2)已知碳酸、亚硫酸、次氯酸的电离平衡常数如下表。
| 物质 | H2CO3 | H2SO3 | HClO | |
| 电离平衡常数 | Ka1 | 4.40×10-7 | 1.54×10-2 | 2.95×10-8 |
| Ka2 | 5.61×10-11 | 1.02×10-7 | ||
②试比较
 、
、 和HCIO的酸性强弱:
和HCIO的酸性强弱:③写出少量CO2与NaClO反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有化学中常见的一些物质:①空气 ②氯气 ③氢氧化钠 ④熔融状态的硝酸钾 ⑤铁 ⑥葡萄糖 ⑦硫酸 ⑧氯化铁溶液⑨碳酸氢钠⑩氨气。在以上物质中:
(1)属于单质的是_______ ,属于混合物的是_______ ;
(2)属于电解质的是_______ ,属于非电解质的是_______ ;
(3)属于酸的是_______ ,属于碱的是_______ ,属于盐(包括盐溶液)的是_______ ;
(4)上述物质在该状态下能导电的是_______
(5)写出⑨在水中的电离方程式:_______
(6)写出下列离子方程式
i.③和⑧反应:_______
ii.用⑨治疗胃酸(主要成分为盐酸)过多:_______ 。
(1)属于单质的是
(2)属于电解质的是
(3)属于酸的是
(4)上述物质在该状态下能导电的是
(5)写出⑨在水中的电离方程式:
(6)写出下列离子方程式
i.③和⑧反应:
ii.用⑨治疗胃酸(主要成分为盐酸)过多:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】①Cu丝 ②熔融的MgCl2 ③NaCl溶液 ④蔗糖 ⑤CH3COOH ⑥CaCO3 ⑦NaHCO3 ⑧CO2 ⑨氨水,请用相应的数字编号和化学用语回答问题:
(1)属于电解质的是______________ ;(2)能导电的是 ___________________ ;
(3)属于强电解质的是____________ ;(4)属于非电解质的是 ____________ ;
(5)NaHCO3的电离方程式_________________________ ;
(6)写出以上物质能发生中和反应的离子方程式_______________________________ 。
(1)属于电解质的是
(3)属于强电解质的是
(5)NaHCO3的电离方程式
(6)写出以上物质能发生中和反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】弱电解质的电离平衡、盐类的水解平衡均属于化学平衡。根据要求回答问题。
(1)一定温度下,向1L0.1mol·L-1CH3COOH溶液中加入0.1molCH3COONa固体,则醋酸的电离平衡向___________ (填“正”或“逆”)反应方向移动;水的电离程度将___________ (填“增大”“减小”或“不变”)。
(2)99℃时,Kw=1.0×10-12,该温度下测得0.1mol·L-1Na2A溶液的pH=6。
①H2A在水溶液中的电离方程式为___________ 。
②体积相等、pH=1的盐酸与H2A溶液分别与足量的Zn反应,产生的氢气___________ 。
A.盐酸多 B.H2A多 C.一样多 D.无法确定
③将0.1mol·L-1H2A溶液与0.2mol·L-1氨水等体积混合,完全反应后溶液中各离子浓度的电荷守恒关系式为___________ 。
(3)已知常温下,H2SO3的电离常数为Kal=1.54×10-2,Ka2=1.02×10-7,H2CO3的电离常数为Kal=4.30×10-7,Ka2=5.60×10-11。
①下列微粒可以大量共存的是___________ (填字母)。
a、 、
、 b、
b、 、
、 c、
c、 、
、 d、H2SO3、
d、H2SO3、
②常温下,NaHSO3溶液显___________ 性(填“酸”“碱”或“中”),溶液中离子浓度从大到小的排列顺序是___________ 。
(1)一定温度下,向1L0.1mol·L-1CH3COOH溶液中加入0.1molCH3COONa固体,则醋酸的电离平衡向
(2)99℃时,Kw=1.0×10-12,该温度下测得0.1mol·L-1Na2A溶液的pH=6。
①H2A在水溶液中的电离方程式为
②体积相等、pH=1的盐酸与H2A溶液分别与足量的Zn反应,产生的氢气
A.盐酸多 B.H2A多 C.一样多 D.无法确定
③将0.1mol·L-1H2A溶液与0.2mol·L-1氨水等体积混合,完全反应后溶液中各离子浓度的电荷守恒关系式为
(3)已知常温下,H2SO3的电离常数为Kal=1.54×10-2,Ka2=1.02×10-7,H2CO3的电离常数为Kal=4.30×10-7,Ka2=5.60×10-11。
①下列微粒可以大量共存的是
a、
 、
、 b、
b、 、
、 c、
c、 、
、 d、H2SO3、
d、H2SO3、
②常温下,NaHSO3溶液显
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)常温下将0.2mol/LHCl溶液与0.2mol/LMOH溶液等体积混合,测得混合溶液的pH=6,则混合溶液中由水电离出的c(H+)__ 0.2mol/LHCl溶液中由水电离出的c(H+)。(填“>”“<”或“=”),该混合溶液的物料守恒式为__ 。
(2)常温下若将0.2mol/LMOH溶液与0.1mol/LHCl溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下MOH的电离程度__ MCl的水解程度。(填“>”“<”或“=”)。
(3)常温下若将pH=3的HR溶液与pH=11的NaOH溶液等体积混合,测得混合溶液的pH≠7,则混合溶液的pH__ 。(填“>7”“<7”或“无法确定”)
(4)某温度时,测得0.01mol/L的NaOH溶液pH为11,在此温度下,将pH=a的NaOH溶液VaL与pH=b的硫酸VbL混合。若所得混合溶液为中性,且a=12,b=2,求Va∶Vb=__ 。
(2)常温下若将0.2mol/LMOH溶液与0.1mol/LHCl溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下MOH的电离程度
(3)常温下若将pH=3的HR溶液与pH=11的NaOH溶液等体积混合,测得混合溶液的pH≠7,则混合溶液的pH
(4)某温度时,测得0.01mol/L的NaOH溶液pH为11,在此温度下,将pH=a的NaOH溶液VaL与pH=b的硫酸VbL混合。若所得混合溶液为中性,且a=12,b=2,求Va∶Vb=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)某温度时,水的 ,该温度下,
,该温度下, 的溶液呈
的溶液呈_______ (填“酸性”“碱性”或“中性”)。
(2)在25℃时, 的两种一元酸溶液A、B各1 mL,分别加水稀释到1000 mL,其pH与溶液体积V的关系如图所示,则下列说法正确的是_______
的两种一元酸溶液A、B各1 mL,分别加水稀释到1000 mL,其pH与溶液体积V的关系如图所示,则下列说法正确的是_______

(3)甲酸(HCOOH)和乙酸( )一样属于一元弱酸,请写出甲酸的电离方程式:
)一样属于一元弱酸,请写出甲酸的电离方程式:_______ ,常温下,测的同浓度的甲酸溶液和乙酸溶液的pH,甲酸pH更小,则
_______  (填写“<”“>”“=”)。
(填写“<”“>”“=”)。
(4)25℃时,0.1mol/L下列物质的溶液,水电离出的 由大到小的顺序是
由大到小的顺序是_______ (填序号)。
① ②
② ③HCOOH ④
③HCOOH ④
(5)25℃时, 的HA溶液中
的HA溶液中 ,此溶液的
,此溶液的
_______ 。
(6)25℃时,在体积为 的
的 的NaOH溶液中,加入体积为
的NaOH溶液中,加入体积为 的
的 的
的 溶液。若反应后溶液的
溶液。若反应后溶液的 ,(反应后溶液体积等于NaOH溶液与
,(反应后溶液体积等于NaOH溶液与 溶液的体积之和),则
溶液的体积之和),则
_______ 。
(1)某温度时,水的
 ,该温度下,
,该温度下, 的溶液呈
的溶液呈(2)在25℃时,
 的两种一元酸溶液A、B各1 mL,分别加水稀释到1000 mL,其pH与溶液体积V的关系如图所示,则下列说法正确的是_______
的两种一元酸溶液A、B各1 mL,分别加水稀释到1000 mL,其pH与溶液体积V的关系如图所示,则下列说法正确的是_______
| A.稀释后,A酸溶液的导电性比B酸溶液强 |
| B.稀释前,两种酸溶液的物质的量浓度相等 |
| C.若a=5,则A是强酸,B是弱酸 |
D.若 ,则A、B都是弱酸 ,则A、B都是弱酸 |
 )一样属于一元弱酸,请写出甲酸的电离方程式:
)一样属于一元弱酸,请写出甲酸的电离方程式:
 (填写“<”“>”“=”)。
(填写“<”“>”“=”)。(4)25℃时,0.1mol/L下列物质的溶液,水电离出的
 由大到小的顺序是
由大到小的顺序是①
 ②
② ③HCOOH ④
③HCOOH ④
(5)25℃时,
 的HA溶液中
的HA溶液中 ,此溶液的
,此溶液的
(6)25℃时,在体积为
 的
的 的NaOH溶液中,加入体积为
的NaOH溶液中,加入体积为 的
的 的
的 溶液。若反应后溶液的
溶液。若反应后溶液的 ,(反应后溶液体积等于NaOH溶液与
,(反应后溶液体积等于NaOH溶液与 溶液的体积之和),则
溶液的体积之和),则
您最近一年使用:0次



