下列物质①NaHSO4、②H2O、③NaOH、④BaSO4、⑤NH3、⑥CO2、⑦CH3COOH、⑧CH3OH、⑨Fe、⑩氯化钠溶液
(1)属于非电解质的是______ ;属于强电解质的是______ ;既不是电解质也不是非电解质,且常温下能导电的物质是______ (均填序号)。
(2)已知碳酸、亚硫酸、次氯酸的电离平衡常数如下表。
①写出H2SO3的第二步电离方程式______ 。
②试比较 、
、 和HCIO的酸性强弱:
和HCIO的酸性强弱:______ 。
③写出少量CO2与NaClO反应的离子方程式______ 。
(1)属于非电解质的是
(2)已知碳酸、亚硫酸、次氯酸的电离平衡常数如下表。
| 物质 | H2CO3 | H2SO3 | HClO | |
| 电离平衡常数 | Ka1 | 4.40×10-7 | 1.54×10-2 | 2.95×10-8 |
| Ka2 | 5.61×10-11 | 1.02×10-7 | ||
②试比较
 、
、 和HCIO的酸性强弱:
和HCIO的酸性强弱:③写出少量CO2与NaClO反应的离子方程式
更新时间:2023-11-27 14:26:04
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】有下列物质:①二氧化碳;②硝酸钾晶体;③铝;④空气;⑤熔融氯化钠;⑥稀硫酸;⑦氢氧化钠固体。请用序号回答下列问题:
(1)属于混合物的是________ ;属于盐的是___________ 。
(2)属于电解质的是__________ ;能够导电的是__________ 。
(3)①~⑦中,有一种物质能与稀盐酸发生氧化还原反应,该反应的离子方程式为___________ 。
(1)属于混合物的是
(2)属于电解质的是
(3)①~⑦中,有一种物质能与稀盐酸发生氧化还原反应,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)实验室常用浓盐酸与高锰酸钾发生反应快速制备少量氯气,该反应的化学方程式为: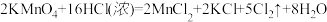 用双线桥法表示该反应过程中的电子转移情况
用双线桥法表示该反应过程中的电子转移情况______________________ ,该反应中氧化剂为____________ ,HCl的作用是______________________ 。
(2)KMnO4能与热的经硫酸酸化的Na2C2O4反应,生成Mn2+和CO2,该反应的离子方程式是_________________________________ 。
(3)已知在碱性溶液中可发生如下反应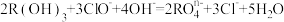 ,则
,则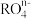 中R的化合价是
中R的化合价是________ 。
A.+3 B.+4 C.+5 D.+6
(4)填写下列空白:
①等物质的量的CO和CO2中:所含的分子数目之比为_______ ,相同条件下体积之比为_______ ,所含的原子总数目之比为_______ 。
②有下列物质:
a.硫酸 b.盐酸 c.氯气 d.硫酸钡 e.甲烷 f.铜 g.CH3COOH h.氯化氢 i.蔗糖 j.氨气 k.CO2 l.NaHCO3 m.Al(OH)3 n.NaOH溶液
其中属于非电解质的为_____________ (填序号,下同。),属于电解质的为____________ 。
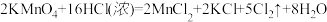 用双线桥法表示该反应过程中的电子转移情况
用双线桥法表示该反应过程中的电子转移情况(2)KMnO4能与热的经硫酸酸化的Na2C2O4反应,生成Mn2+和CO2,该反应的离子方程式是
(3)已知在碱性溶液中可发生如下反应
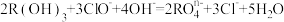 ,则
,则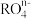 中R的化合价是
中R的化合价是A.+3 B.+4 C.+5 D.+6
(4)填写下列空白:
①等物质的量的CO和CO2中:所含的分子数目之比为
②有下列物质:
a.硫酸 b.盐酸 c.氯气 d.硫酸钡 e.甲烷 f.铜 g.CH3COOH h.氯化氢 i.蔗糖 j.氨气 k.CO2 l.NaHCO3 m.Al(OH)3 n.NaOH溶液
其中属于非电解质的为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】有下列物质:①Na2CO3•10H2O晶体 ②铜 ③硫酸溶液 ④CO2 ⑤NaHSO4固体 ⑥Ba(OH)2固体 ⑦红褐色的氢氧化铁胶体 ⑧氨水 ⑨稀硝酸 ⑩Al2(SO4)3固体。
(1)上述物质属于电解质的有__ (填编号),能导电的物质有__ (填编号)。
(2)上述物质中有两种物质之间可发生离子反应:H++OH-=H2O,写出该离子反应对应的化学方程式___ 。
(3)写出固体⑤熔化时的电离方程式__ 。
(4)当⑤与⑥1:1混合后,写出该离子方程式__ 。
(5)写出⑦的制备方法__ 。
(1)上述物质属于电解质的有
(2)上述物质中有两种物质之间可发生离子反应:H++OH-=H2O,写出该离子反应对应的化学方程式
(3)写出固体⑤熔化时的电离方程式
(4)当⑤与⑥1:1混合后,写出该离子方程式
(5)写出⑦的制备方法
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求完成。
(1)现有下列物质:①干冰②NaOH③氨水④纯醋酸⑤BaSO4⑥铜⑦蔗糖⑧NH3⑨Ba(OH)2溶液。其中属于电解质的是___________ 、属于非电解质的是___________ (填序号)。
(2)Ba(OH)2的电离方程式:___________ 。
(3)写出⑨与少量NaHSO4水溶液反应的离子方程式:___________ 。
(4)胶体是一种常见的分散系,向煮沸的蒸馏水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,可制得Fe(OH)3胶体,区分胶体和溶液可用什么方法:___________ 。
(1)现有下列物质:①干冰②NaOH③氨水④纯醋酸⑤BaSO4⑥铜⑦蔗糖⑧NH3⑨Ba(OH)2溶液。其中属于电解质的是
(2)Ba(OH)2的电离方程式:
(3)写出⑨与少量NaHSO4水溶液反应的离子方程式:
(4)胶体是一种常见的分散系,向煮沸的蒸馏水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,可制得Fe(OH)3胶体,区分胶体和溶液可用什么方法:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有以下7种物质,请回答下列问题:
①干冰②氯化钠③蔗糖④稀硫酸⑤NaHSO4溶液⑥碳酸氢钠⑦氢氧化钡溶液
(1)属于电解质的是_______ 。属于非电解质的是_______ 。
(2)写出物质⑤在水中的电离方程式_______ 。
(3)写出物质④和⑦反应的化学方程式_______ 。
①干冰②氯化钠③蔗糖④稀硫酸⑤NaHSO4溶液⑥碳酸氢钠⑦氢氧化钡溶液
(1)属于电解质的是
(2)写出物质⑤在水中的电离方程式
(3)写出物质④和⑦反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求完成下列各小题:
(1)实验室中用铝和盐酸在常温条件下制备AlCl3其化学方程式为___________ 。工业上在高温条件下用碳氯化法制备AlCl3,其化学方程式Al2O3+xC+3Cl2 2AlCl3+3M,则M为
2AlCl3+3M,则M为___________ 。
(2)已知每100g葡萄糖中含碳元素40.00g、氢元素6.67g,其余为氧元素,试求葡萄糖中碳、氢、氧3种元素的原子个数之比___________ 。
(3)已知乙醇(C2H5OH)能与K2C2O4和H2SO4的混合溶液在一定条件下发生反应:2K2Cr2O7+3C2H5OH+8H2SO4=2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O, 和Cr3+和在溶液中分别显橙色和绿色,该反应
和Cr3+和在溶液中分别显橙色和绿色,该反应___________ (填“是”或“不是”)离子反应,写出Cr2(SO4)3的电离方程式___________ 。你认为能否用这一反应来检测司机是否酒驾___________ (填“能”或“不能“),简述其原理:___________ 。
(1)实验室中用铝和盐酸在常温条件下制备AlCl3其化学方程式为
 2AlCl3+3M,则M为
2AlCl3+3M,则M为(2)已知每100g葡萄糖中含碳元素40.00g、氢元素6.67g,其余为氧元素,试求葡萄糖中碳、氢、氧3种元素的原子个数之比
(3)已知乙醇(C2H5OH)能与K2C2O4和H2SO4的混合溶液在一定条件下发生反应:2K2Cr2O7+3C2H5OH+8H2SO4=2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O,
 和Cr3+和在溶液中分别显橙色和绿色,该反应
和Cr3+和在溶液中分别显橙色和绿色,该反应
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1) Al(OH)3具有一元弱酸的性质,在水中电离时产生的含铝微粒具有正四面体结构,写出电离方程式:___________ 。
(2)人体血液里主要通过碳酸氢盐缓冲体系( )维持pH稳定。已知正常体温人体血液中,H2CO3的一级电离常数Ka1=10-6.1,
)维持pH稳定。已知正常体温人体血液中,H2CO3的一级电离常数Ka1=10-6.1, ≈
≈ ,1g2=03.由题给数据可算得正常人体血液的pH约为
,1g2=03.由题给数据可算得正常人体血液的pH约为___________ ,当过量的酸进入血液中时,血液缓冲体系中 的值将
的值将___________ (填“变大、变小、不变”)。
(2)人体血液里主要通过碳酸氢盐缓冲体系(
 )维持pH稳定。已知正常体温人体血液中,H2CO3的一级电离常数Ka1=10-6.1,
)维持pH稳定。已知正常体温人体血液中,H2CO3的一级电离常数Ka1=10-6.1, ≈
≈ ,1g2=03.由题给数据可算得正常人体血液的pH约为
,1g2=03.由题给数据可算得正常人体血液的pH约为 的值将
的值将
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请根据信息回答下列问题。
(1)硒酸(H2SeO4)在水溶液中的电离方程式如下:H2SeO4=H++HSeO ,HSeO
,HSeO ⇌H++SeO
⇌H++SeO 。
。
①写出NaHSeO4在水溶液中的电离方程式_______ 。
②已知25℃时,1mol/L的H2SeO4溶液中,HSeO 的电离度为α,则其电离常数Ka=
的电离度为α,则其电离常数Ka=_______ (用含α的计算式表示,忽略水的电离)
(2)亚磷酸(H3PO3)是二元酸,25℃时,Ka1=1×10-2、Ka2=2.6×10-7,HF的电离常数的值为Ka=3.6×10-4,将足量H3PO3溶液和NaF溶液反应,其离子方程式为_______ 。
(3)在常温下,有硫酸和盐酸的混合液20 mL,向该溶液中加入0.05 mol/L的Ba(OH)2时,生成的BaSO4沉淀的质量和混合溶液的pH有如图所示关系。
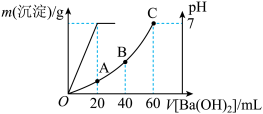
①C点溶液中的主要溶质是_______ (写化学式)。
②当滴加Ba(OH)2的体积至80 mL时,溶液的pH值为_______ (已知lg2=0.3,混合后溶液体积变化忽略不计)
(1)硒酸(H2SeO4)在水溶液中的电离方程式如下:H2SeO4=H++HSeO
 ,HSeO
,HSeO ⇌H++SeO
⇌H++SeO 。
。①写出NaHSeO4在水溶液中的电离方程式
②已知25℃时,1mol/L的H2SeO4溶液中,HSeO
 的电离度为α,则其电离常数Ka=
的电离度为α,则其电离常数Ka=(2)亚磷酸(H3PO3)是二元酸,25℃时,Ka1=1×10-2、Ka2=2.6×10-7,HF的电离常数的值为Ka=3.6×10-4,将足量H3PO3溶液和NaF溶液反应,其离子方程式为
(3)在常温下,有硫酸和盐酸的混合液20 mL,向该溶液中加入0.05 mol/L的Ba(OH)2时,生成的BaSO4沉淀的质量和混合溶液的pH有如图所示关系。

①C点溶液中的主要溶质是
②当滴加Ba(OH)2的体积至80 mL时,溶液的pH值为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】查阅资料获得25℃时部分弱电解质的电离平衡常数数据:
回答下列问题:
(1) 的电离方程式为
的电离方程式为___________ 。
(2)物质的量浓度相同的HF、HClO、 、
、 中,
中, 由大到小的顺序是
由大到小的顺序是___________ 。
(3)常温下, 的氨水的pH约为
的氨水的pH约为___________ ( )。
)。
(4)常温下, 的水溶液的pH
的水溶液的pH___________ 7(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
(5)常温下,在 的
的 溶液中,水电离出来的
溶液中,水电离出来的 为
为___________  。
。
| 化学式 | HF | HClO |  |  |  |
| 电离常数 | 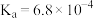 | 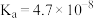 | 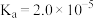 | 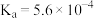 | 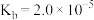 |
(1)
 的电离方程式为
的电离方程式为(2)物质的量浓度相同的HF、HClO、
 、
、 中,
中, 由大到小的顺序是
由大到小的顺序是(3)常温下,
 的氨水的pH约为
的氨水的pH约为 )。
)。(4)常温下,
 的水溶液的pH
的水溶液的pH ”、“
”、“ ”或“
”或“ ”)。
”)。(5)常温下,在
 的
的 溶液中,水电离出来的
溶液中,水电离出来的 为
为 。
。
您最近一年使用:0次



