有下列物质:①二氧化碳;②硝酸钾晶体;③铝;④空气;⑤熔融氯化钠;⑥稀硫酸;⑦氢氧化钠固体。请用序号回答下列问题:
(1)属于混合物的是________ ;属于盐的是___________ 。
(2)属于电解质的是__________ ;能够导电的是__________ 。
(3)①~⑦中,有一种物质能与稀盐酸发生氧化还原反应,该反应的离子方程式为___________ 。
(1)属于混合物的是
(2)属于电解质的是
(3)①~⑦中,有一种物质能与稀盐酸发生氧化还原反应,该反应的离子方程式为
更新时间:2020-10-23 10:02:07
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】下列物质:① 晶体②稀盐酸③
晶体②稀盐酸③ 固体④熔融
固体④熔融 ⑤酒精⑥铜⑦
⑤酒精⑥铜⑦ ⑧牛奶⑨液态
⑧牛奶⑨液态 ⑩
⑩ 溶液
溶液
(1)属于分散系的是_______ ;(填序号,下同)
(2)上述状态下能导电的是_______
(3)属于电解质的是_______ ;
(4)属于非电解质的是_______ 。
 晶体②稀盐酸③
晶体②稀盐酸③ 固体④熔融
固体④熔融 ⑤酒精⑥铜⑦
⑤酒精⑥铜⑦ ⑧牛奶⑨液态
⑧牛奶⑨液态 ⑩
⑩ 溶液
溶液(1)属于分散系的是
(2)上述状态下能导电的是
(3)属于电解质的是
(4)属于非电解质的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下列物质中:A.KI(s) B.C2H5OH(l) C.Cl2(g) D.CH3COOH(l)E.BaSO4(s) F.NaHSO4(aq) G.石墨(s) H.蔗糖(s) I.NaOH(l) J.硫酸 K.盐酸
(1)属于非电解质的是____________ (填序号,下同),属于强电解质的是____________ ,属于弱电解质的是____________ 。
(2)能直接导电的是________________ ,电解质中能溶于水,且水溶液能导电是________________ 。
(1)属于非电解质的是
(2)能直接导电的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有下列10种物质:
① ②熔融的
②熔融的 ③盐酸 ④
③盐酸 ④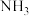 ⑤
⑤ ⑥
⑥ 固体 ⑦纯净醋酸 ⑧氢氧化铁胶体 ⑨乙醇
固体 ⑦纯净醋酸 ⑧氢氧化铁胶体 ⑨乙醇
(1)上述物质中能导电的有___________ (填序号,下同)。
(2)属于电解质的有___________ ,属于弱电解质的有___________ ,属于非电解质的有___________ 。
(3)向⑧中逐滴加入③,该过程中可观察到现象为___________ ,其中反应的离子方程式为___________ 。
(4)若用实验证明⑥中含氯元素,你的操作方法是___________ 。
①
 ②熔融的
②熔融的 ③盐酸 ④
③盐酸 ④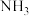 ⑤
⑤ ⑥
⑥ 固体 ⑦纯净醋酸 ⑧氢氧化铁胶体 ⑨乙醇
固体 ⑦纯净醋酸 ⑧氢氧化铁胶体 ⑨乙醇(1)上述物质中能导电的有
(2)属于电解质的有
(3)向⑧中逐滴加入③,该过程中可观察到现象为
(4)若用实验证明⑥中含氯元素,你的操作方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】有下列物质:①Cl2;②Na2O2;③NaOH溶液;④HCl ;⑤H2O2;⑥MgF2; ⑦NH4Cl。
(1)只由离子键构成的物质是______ 。
(2)只由共价键构成的物质是______ 。
(3)既有共价键又有离子键构成的电解质是______ 。
(1)只由离子键构成的物质是
(2)只由共价键构成的物质是
(3)既有共价键又有离子键构成的电解质是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】有以下物质:①石墨 ②铝 ③酒精 ④氨水 ⑤二氧化碳 ⑥碳酸钠固体 ⑦氢氧化钡溶液 ⑧ 熔融氯化钠 ⑨氧化钠固体 ⑩氯化氢气体 其中能导电的是____ (填序号,下同);属于非电解质的是______ ;属于电解质的是_____
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】对于成千上万、形形色色的化学物质,用分类的思想对其进行学习和研究极其重要。有以下物质,请按要求作答。
现有下列10种物质:①铝;②纯醋酸;③CO2;④H2SO4;⑤NaOH;⑥硫酸铜溶液;⑦熔融的NaCl;⑧NaHSO4;⑨硝酸钾晶体;⑩乙醇。
(1)上述物质中属于电解质的有___________ (填序号,下同);属于非电解质的有___________ ;①②⑥⑦⑨⑩六种物质中能导电的有___________ 。
(2)向⑥中加入⑤的离子方程式是___________ 。
(3)②在水中的电离方程式为___________ 。
(4)向Ba(OH)2的水溶液中逐滴滴加⑧的水溶液,当溶液恰好呈中性时NaHSO4与Ba(OH)2反应的化学计量数之比为___________ ,其离子反应方程式为___________ 。
现有下列10种物质:①铝;②纯醋酸;③CO2;④H2SO4;⑤NaOH;⑥硫酸铜溶液;⑦熔融的NaCl;⑧NaHSO4;⑨硝酸钾晶体;⑩乙醇。
(1)上述物质中属于电解质的有
(2)向⑥中加入⑤的离子方程式是
(3)②在水中的电离方程式为
(4)向Ba(OH)2的水溶液中逐滴滴加⑧的水溶液,当溶液恰好呈中性时NaHSO4与Ba(OH)2反应的化学计量数之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题。
Ⅰ.纳米磁珠(纳米 )颗粒中含有人体代谢生长必需的微量元素铁,不含其他有毒的金属元素,可以用于对比增强磁共振成像、免疫检测、组织修复、药物运输和细胞分离等方面。
)颗粒中含有人体代谢生长必需的微量元素铁,不含其他有毒的金属元素,可以用于对比增强磁共振成像、免疫检测、组织修复、药物运输和细胞分离等方面。
【查阅资料】
 为黑色固体,硬度较大,有磁性,不溶于
为黑色固体,硬度较大,有磁性,不溶于 、碱和
、碱和 ,纳米
,纳米 在潮湿的
在潮湿的 中容易被
中容易被 氧化,高温下被
氧化,高温下被 氧化成
氧化成 ,溶于
,溶于 的溶液中,生成
的溶液中,生成 和
和 。向含有一定配比的
。向含有一定配比的 和
和 的混合盐溶液中,加入过量的碱性物质,如
的混合盐溶液中,加入过量的碱性物质,如 、
、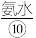 ,使其达到某个pH范围,在适当的温度和高速搅拌下发生反应合成纳米
,使其达到某个pH范围,在适当的温度和高速搅拌下发生反应合成纳米 颗粒。
颗粒。
(1)①~⑩,能导电的是_______ (填编号,后同),属于非电解质的是___________ 。
(2)将⑥气体通入⑩,写出发生反应的离子方程式:___________ 。
Ⅱ.空气与我们的生存息息相关。 是主要的温室气体,
是主要的温室气体, 是主要的大气污染物之一。
是主要的大气污染物之一。
(3)写出 与NaOH反应的离子方程式
与NaOH反应的离子方程式___________ 。
(4) 、
、 均属于酸性氧化物,类比
均属于酸性氧化物,类比 下列物质中可以与
下列物质中可以与 发生反应的是_______。
发生反应的是_______。
(5)双碱法脱硫过程如下图所示。
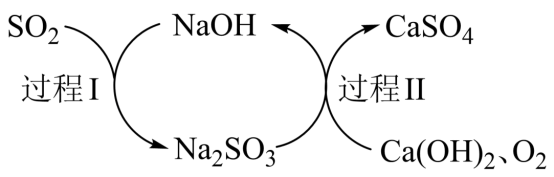
①下列反应中,不能用同一离子方程式表示的是_______ (填序号)。
A. 溶液和稀
溶液和稀 B.NaOH和稀
B.NaOH和稀
C. 溶液与稀
溶液与稀 D.NaOH和稀盐酸
D.NaOH和稀盐酸
②类比 与碱反应,过程Ⅰ的离子方程式是
与碱反应,过程Ⅰ的离子方程式是_______ 。
③双碱法脱硫过程中,循环利用的物质是_______ (填化学式)。
Ⅰ.纳米磁珠(纳米
 )颗粒中含有人体代谢生长必需的微量元素铁,不含其他有毒的金属元素,可以用于对比增强磁共振成像、免疫检测、组织修复、药物运输和细胞分离等方面。
)颗粒中含有人体代谢生长必需的微量元素铁,不含其他有毒的金属元素,可以用于对比增强磁共振成像、免疫检测、组织修复、药物运输和细胞分离等方面。【查阅资料】
 为黑色固体,硬度较大,有磁性,不溶于
为黑色固体,硬度较大,有磁性,不溶于 、碱和
、碱和 ,纳米
,纳米 在潮湿的
在潮湿的 中容易被
中容易被 氧化,高温下被
氧化,高温下被 氧化成
氧化成 ,溶于
,溶于 的溶液中,生成
的溶液中,生成 和
和 。向含有一定配比的
。向含有一定配比的 和
和 的混合盐溶液中,加入过量的碱性物质,如
的混合盐溶液中,加入过量的碱性物质,如 、
、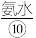 ,使其达到某个pH范围,在适当的温度和高速搅拌下发生反应合成纳米
,使其达到某个pH范围,在适当的温度和高速搅拌下发生反应合成纳米 颗粒。
颗粒。(1)①~⑩,能导电的是
(2)将⑥气体通入⑩,写出发生反应的离子方程式:
Ⅱ.空气与我们的生存息息相关。
 是主要的温室气体,
是主要的温室气体, 是主要的大气污染物之一。
是主要的大气污染物之一。(3)写出
 与NaOH反应的离子方程式
与NaOH反应的离子方程式(4)
 、
、 均属于酸性氧化物,类比
均属于酸性氧化物,类比 下列物质中可以与
下列物质中可以与 发生反应的是_______。
发生反应的是_______。A. | B.NaCl | C.HCl | D. |

①下列反应中,不能用同一离子方程式表示的是
A.
 溶液和稀
溶液和稀 B.NaOH和稀
B.NaOH和稀
C.
 溶液与稀
溶液与稀 D.NaOH和稀盐酸
D.NaOH和稀盐酸②类比
 与碱反应,过程Ⅰ的离子方程式是
与碱反应,过程Ⅰ的离子方程式是③双碱法脱硫过程中,循环利用的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)①熔融BaSO4②盐酸③胆矾④KOH固体⑤Fe⑥氨水⑦乙醇⑧冰醋酸⑨NaCl溶液⑩CO,能导电的是_______ ,电解质是_______ ,强电解质是_______ 。
(2)写出下列物质的电离方程式:①熔融的NaHSO4____ ②NaHCO3溶液___
(3)写出下列反应的离子方程式:①氢氧化铜与稀盐酸反应__________ ②四氧化三铁与稀盐酸反应______________ ③碳酸钙与硝酸反应_________________ ④硫酸氢钠溶液中滴加氢氧化钡溶液至硫酸根刚好沉淀完全___________________ 。
(2)写出下列物质的电离方程式:①熔融的NaHSO4
(3)写出下列反应的离子方程式:①氢氧化铜与稀盐酸反应
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】钠是一种非常活泼、具有广泛应用的金属。
(1)金属钠非常活泼,通常保存在___________ 里,以隔绝空气。
(2)汽车安全气囊的气体发生剂 :可由金属钠生产。某汽车安全气囊内含
:可由金属钠生产。某汽车安全气囊内含 、
、 和
和 等物质。
等物质。
①当汽车发生较严重的碰撞时,引发 分解
分解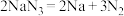 ,从而为气囊充气。用单线桥表示该反应电子转移的方向数目
,从而为气囊充气。用单线桥表示该反应电子转移的方向数目___________ 。
②产生的Na立即与 发生置换反应生成
发生置换反应生成 ,化学方程式是:
,化学方程式是:___________ 。
③ 是冷却剂,吸收产气过程释放的热量。
是冷却剂,吸收产气过程释放的热量。 起冷却作用时发生反应的化学方程式为:
起冷却作用时发生反应的化学方程式为:___________ 。
(3)工业通过电解NaCl生产金属钠: ,过程如图:
,过程如图:
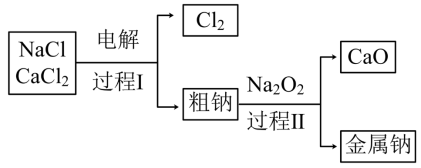
已知:电解时需要将NaCl加热至熔融状态。NaCl的熔点为801℃,为降低能耗,通常加入 从而把培点降至约580℃。
从而把培点降至约580℃。
①NaCl固体加热至熔融状态,目的是___________ 。
②粗钠中含有少量杂质Ca,过程Ⅱ在加热条件下除去Ca的化学方程式是:___________ 。
③过程Ⅰ中, 能发生像NaCl那样的电解反应而被消耗。但在过程1中
能发生像NaCl那样的电解反应而被消耗。但在过程1中 却不断地被重新生成,原因是:
却不断地被重新生成,原因是:___________ 。
(1)金属钠非常活泼,通常保存在
(2)汽车安全气囊的气体发生剂
 :可由金属钠生产。某汽车安全气囊内含
:可由金属钠生产。某汽车安全气囊内含 、
、 和
和 等物质。
等物质。①当汽车发生较严重的碰撞时,引发
 分解
分解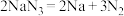 ,从而为气囊充气。用单线桥表示该反应电子转移的方向数目
,从而为气囊充气。用单线桥表示该反应电子转移的方向数目②产生的Na立即与
 发生置换反应生成
发生置换反应生成 ,化学方程式是:
,化学方程式是:③
 是冷却剂,吸收产气过程释放的热量。
是冷却剂,吸收产气过程释放的热量。 起冷却作用时发生反应的化学方程式为:
起冷却作用时发生反应的化学方程式为:(3)工业通过电解NaCl生产金属钠:
 ,过程如图:
,过程如图:
已知:电解时需要将NaCl加热至熔融状态。NaCl的熔点为801℃,为降低能耗,通常加入
 从而把培点降至约580℃。
从而把培点降至约580℃。①NaCl固体加热至熔融状态,目的是
②粗钠中含有少量杂质Ca,过程Ⅱ在加热条件下除去Ca的化学方程式是:
③过程Ⅰ中,
 能发生像NaCl那样的电解反应而被消耗。但在过程1中
能发生像NaCl那样的电解反应而被消耗。但在过程1中 却不断地被重新生成,原因是:
却不断地被重新生成,原因是:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氧化还原反应和离子反应是高一所学过的重要化学反应类型,仔细思考回答下列问题。
(Ⅰ)下列一组有水参与的反应
①2Na+2H2O=2NaOH+H2↑
②2Na2O2+2H2O=4NaOH+O2↑
③Na2O+H2O=2NaOH
④3Fe+4H2O Fe3O4+4H2
Fe3O4+4H2
⑤2H2O 2H2↑+O2↑
2H2↑+O2↑
⑥2F2+2H2O=4HF+O2
(1)其中不属于氧化还原反应的是_____________ (填编号)。
(2)在这些氧化还原反应中,水既作氧化剂,又作还原剂是___________ (填编号),水既不作氧化剂,又不作还原剂是__________ (填编号)。
(3)请你运用所学知识分析3NO2+H2O=2HNO3+NO是否属于氧化还原反应?___________ (填“是”或“不是”),若是,这个反应的氧化剂和还原剂的质量比是________ ;
(Ⅱ)写出下列反应的离子方程式
①铜片与稀硝酸的反应_____________________________________ ;
②往氯化铝溶液中加入过量的NaOH溶液______________________ ;
(Ⅲ)写出下列反应的化学方程式
①二氧化硫发生催化氧化反应_________________________________ ;
②制漂白液的反应____________________________ 。
(Ⅰ)下列一组有水参与的反应
①2Na+2H2O=2NaOH+H2↑
②2Na2O2+2H2O=4NaOH+O2↑
③Na2O+H2O=2NaOH
④3Fe+4H2O
 Fe3O4+4H2
Fe3O4+4H2 ⑤2H2O
 2H2↑+O2↑
2H2↑+O2↑ ⑥2F2+2H2O=4HF+O2
(1)其中不属于氧化还原反应的是
(2)在这些氧化还原反应中,水既作氧化剂,又作还原剂是
(3)请你运用所学知识分析3NO2+H2O=2HNO3+NO是否属于氧化还原反应?
(Ⅱ)写出下列反应的离子方程式
①铜片与稀硝酸的反应
②往氯化铝溶液中加入过量的NaOH溶液
(Ⅲ)写出下列反应的化学方程式
①二氧化硫发生催化氧化反应
②制漂白液的反应
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铁酸钠(Na2FeO4)是水处理过程使用的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为Fe3+离子。
(1)配平制取铁酸钠的化学方程式____________
Fe(NO3)3 + NaOH + Cl2 = Na2FeO4 + NaNO3 + NaCl+ H2O
反应中______ 元素被氧化,转移电子总数为_______ 。
(2)若制取8.3g铁酸钠需要标准状况下______ L Cl2。
(3)已知CuO具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下CuO和NH3反应的化学方程式____________________________________________ 。
(1)配平制取铁酸钠的化学方程式
Fe(NO3)3 + NaOH + Cl2 = Na2FeO4 + NaNO3 + NaCl+ H2O
反应中
(2)若制取8.3g铁酸钠需要标准状况下
(3)已知CuO具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下CuO和NH3反应的化学方程式
您最近一年使用:0次



