铁酸钠(Na2FeO4)是水处理过程使用的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为Fe3+离子。
(1)配平制取铁酸钠的化学方程式____________
Fe(NO3)3 + NaOH + Cl2 = Na2FeO4 + NaNO3 + NaCl+ H2O
反应中______ 元素被氧化,转移电子总数为_______ 。
(2)若制取8.3g铁酸钠需要标准状况下______ L Cl2。
(3)已知CuO具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下CuO和NH3反应的化学方程式____________________________________________ 。
(1)配平制取铁酸钠的化学方程式
Fe(NO3)3 + NaOH + Cl2 = Na2FeO4 + NaNO3 + NaCl+ H2O
反应中
(2)若制取8.3g铁酸钠需要标准状况下
(3)已知CuO具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下CuO和NH3反应的化学方程式
更新时间:2017-12-09 21:51:25
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】我国政府为了消除碘缺乏病,规定在食盐中必须加入适量的碘酸钾。检验食盐中是否加碘,可利用如下反应:
KIO3+ KI+ H2SO4═ K2SO4+ I2 + H2O
(1)配平该方程式,并且用双线桥法表示该方程式电子转移的方向与数目:____________________
(2)该反应中氧化剂和还原剂的物质的量之比为______________ ;
(3)如果反应中转移0.5mol电子,则生成I2的物质的量为____________ ;
KIO3+ KI+ H2SO4═ K2SO4+ I2 + H2O
(1)配平该方程式,并且用双线桥法表示该方程式电子转移的方向与数目:
(2)该反应中氧化剂和还原剂的物质的量之比为
(3)如果反应中转移0.5mol电子,则生成I2的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氮是生命物质的重要组成元素之一,以氮气为原料的合成氨工业可以实现大规模固氮,氨可用于生成氯化铵、硫酸铵等化学肥料。
(1)科学家已成功合成少量N4分子,N4和N2互为_____ ,NH3分子的空间构型为型______ 。
(2)叠氮化钠(NaN3)受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生40.32L(标况下)氮气,至少需要叠氮酸钠_____ g,转移电子____ 个。
(3)检验铵态氮肥中铵根离子的实验方案是(补充写出步骤,现象):取样,溶于水_________________________________________________ 。
(4)等物质的量浓度的两溶液,pH大小为:氯化铵__________ 硫酸铵(选填>、=或< ,下同);铵根离子浓度相同的两溶液,两者的浓度大小关系为:氯化铵_____ 硫酸铵;
最新“人工固氮”的研究报道:常温常压、催化剂条件下, N2在催化剂表面与水发生反应:与水发生反应: 2N2(g)+6H2O(g) 4NH3(g)+3O2(g)-Q,(Q>0)
4NH3(g)+3O2(g)-Q,(Q>0)
(5)如果反应的平衡常数K值变小,该反应正反应速率_______ (选填增大、减小或不变,下同),逆反应速率_______ .
(6)若反应在恒容条件下进行,请用上述反应中的有关物理量来说明该反应已达到平衡状态_______ .
(7)下列能够提高氮气转化率的措施是:_____
A.适当升高温度 b.增加水的用量
C.使用高效催化剂 d.扩大容器体积
(1)科学家已成功合成少量N4分子,N4和N2互为
(2)叠氮化钠(NaN3)受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生40.32L(标况下)氮气,至少需要叠氮酸钠
(3)检验铵态氮肥中铵根离子的实验方案是(补充写出步骤,现象):取样,溶于水
(4)等物质的量浓度的两溶液,pH大小为:氯化铵
最新“人工固氮”的研究报道:常温常压、催化剂条件下, N2在催化剂表面与水发生反应:与水发生反应: 2N2(g)+6H2O(g)
 4NH3(g)+3O2(g)-Q,(Q>0)
4NH3(g)+3O2(g)-Q,(Q>0)(5)如果反应的平衡常数K值变小,该反应正反应速率
(6)若反应在恒容条件下进行,请用上述反应中的有关物理量来说明该反应已达到平衡状态
(7)下列能够提高氮气转化率的措施是:
A.适当升高温度 b.增加水的用量
C.使用高效催化剂 d.扩大容器体积
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】请完成下列填空:
(1)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4。生成0.1 mol K2FeO4转移的电子的物质的量_______ mol。
(2)二氧化铈(CeO2)是一种重要的稀土氧化物,在平板电视显示屏中有着重要的应用CeO2在稀硫酸和H2O2的作用下可生成Ce3+,H2O2在该反应中作_______ (填“氧化”“还原”)剂,每有1 mol H2O2参加反应,转移电子的物质的量为_______ 。
(3)反应2LiBH4=2LiH+2B+3H2↑,生成22.4 L的H2(标准状况)时,转移电子的物质的量为_______ mol。
(4)用酸性高锰酸钾溶液滴定法可测定双氧水中H2O2的含量:H2O2+KMnO4+H2SO4→MnSO4+K2SO4+O2↑+H2O(未配平),若滴定中消耗0.50 mol/L的高锰酸钾溶液40.00 mL,则此双氧水溶液中溶质的质量为_______ g。
(5)取300 mL0.2 mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是_______ mol。
(1)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4。生成0.1 mol K2FeO4转移的电子的物质的量
(2)二氧化铈(CeO2)是一种重要的稀土氧化物,在平板电视显示屏中有着重要的应用CeO2在稀硫酸和H2O2的作用下可生成Ce3+,H2O2在该反应中作
(3)反应2LiBH4=2LiH+2B+3H2↑,生成22.4 L的H2(标准状况)时,转移电子的物质的量为
(4)用酸性高锰酸钾溶液滴定法可测定双氧水中H2O2的含量:H2O2+KMnO4+H2SO4→MnSO4+K2SO4+O2↑+H2O(未配平),若滴定中消耗0.50 mol/L的高锰酸钾溶液40.00 mL,则此双氧水溶液中溶质的质量为
(5)取300 mL0.2 mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
(1)该反应中的还原剂是___ 。
(2)该反应中,发生还原反应的过程是__ →__ 。
(3)写出该反应的化学方程式:___ 。
(4)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为___ 。
(1)该反应中的还原剂是
(2)该反应中,发生还原反应的过程是
(3)写出该反应的化学方程式:
(4)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)X、Y、Z三种物质存在如图所示转化关系。

回答下列问题:
①若X为黑色固体单质,A为 ,写出
,写出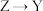 的化学方程式:
的化学方程式:__________________ 。
②若X为 溶液,则写出
溶液,则写出 的化学方程式:
的化学方程式:__________________ 。
(2)已知常温下在溶液中可发生如下两个反应:


由此可以确定 、
、 、
、 三种离子的氧化性由强到弱的顺序是
三种离子的氧化性由强到弱的顺序是__________________ 。
(3) 、
、 、
、 、
、 、
、 、
、 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 的反应过程。
的反应过程。
①该反应中,被氧化的元素是______ (填元素符号),氧化剂是______ (填化学式)。
②将以上物质分别填入下面对应的横线上,组成一个未配平的化学方程式:___
______+______+______→______+______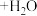 。
。

回答下列问题:
①若X为黑色固体单质,A为
 ,写出
,写出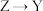 的化学方程式:
的化学方程式:②若X为
 溶液,则写出
溶液,则写出 的化学方程式:
的化学方程式:(2)已知常温下在溶液中可发生如下两个反应:


由此可以确定
 、
、 、
、 三种离子的氧化性由强到弱的顺序是
三种离子的氧化性由强到弱的顺序是(3)
 、
、 、
、 、
、 、
、 、
、 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 的反应过程。
的反应过程。①该反应中,被氧化的元素是
②将以上物质分别填入下面对应的横线上,组成一个未配平的化学方程式:
______+______+______→______+______
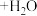 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】配平下列离子方程式。
(1)___________Fe3++___________SO2+___________H2O=___________Fe2++___________SO +___________H+
+___________H+___________
(2)___________MnO +___________H++___________Cl-=___________Mn2++___________Cl2↑+___________H2O
+___________H++___________Cl-=___________Mn2++___________Cl2↑+___________H2O___________
(1)___________Fe3++___________SO2+___________H2O=___________Fe2++___________SO
 +___________H+
+___________H+(2)___________MnO
 +___________H++___________Cl-=___________Mn2++___________Cl2↑+___________H2O
+___________H++___________Cl-=___________Mn2++___________Cl2↑+___________H2O
您最近一年使用:0次
【推荐2】汽车尾气中的氮氧化物(NOx)对环境有危害,可利用化学方法实现氮的转化,从而减少氮氧化物排放。
(1)① 在氮的转化过程中体现了
在氮的转化过程中体现了___________ 性。
② 、碳氢化合物和
、碳氢化合物和 等均可在催化剂作用下,将NOx转化为N2。
等均可在催化剂作用下,将NOx转化为N2。 和
和 反应的化学方程式为
反应的化学方程式为___________ 。
(2)利用电解装置可以将尾气中的 转化为尿素[CO(NH2)2],其中碳元素的化合价为+4价,属于非电解质,工作原理如图。
转化为尿素[CO(NH2)2],其中碳元素的化合价为+4价,属于非电解质,工作原理如图。

装置中离子交换膜是___________ (“阴离子”或“阳离子”)交换膜反应一段时间后,阳极区的 基本不变,结合化学用语解释原因为
基本不变,结合化学用语解释原因为___________ 。
(1)①
 在氮的转化过程中体现了
在氮的转化过程中体现了②
 、碳氢化合物和
、碳氢化合物和 等均可在催化剂作用下,将NOx转化为N2。
等均可在催化剂作用下,将NOx转化为N2。 和
和 反应的化学方程式为
反应的化学方程式为(2)利用电解装置可以将尾气中的
 转化为尿素[CO(NH2)2],其中碳元素的化合价为+4价,属于非电解质,工作原理如图。
转化为尿素[CO(NH2)2],其中碳元素的化合价为+4价,属于非电解质,工作原理如图。
装置中离子交换膜是
 基本不变,结合化学用语解释原因为
基本不变,结合化学用语解释原因为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有下列九种物质:① ②铜③
②铜③ ④
④ ⑤
⑤ ⑥熔融的
⑥熔融的 ⑦氨水⑧稀硝酸⑨
⑦氨水⑧稀硝酸⑨
(1)上述九种物质中有两种物质之间可发生离子反应: ,该离子反应对应的化学方程式为
,该离子反应对应的化学方程式为___________ 。
(2)⑨在水中的电离方程式为___________ 。
(3)以上属于电解质的共有___________ 种。
(4)将少量的③通入⑤的溶液中反应的离子方程式为___________ 。
(5) 和③都属于酸性氧化物,尝试写出
和③都属于酸性氧化物,尝试写出 与氢氧化钠溶液反应的离子方程式:
与氢氧化钠溶液反应的离子方程式:_____ 。
(6)配平②与⑧发生反应的化学方程式,并用双线桥法标明该反应中电子转移的方向和数目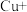



 ,
,___________ 。;当有1个 发生反应时,转移电子的个数为
发生反应时,转移电子的个数为___________ 个;当有3个 发生反应时被还原的
发生反应时被还原的 的个数为
的个数为___________ 个。
 ②铜③
②铜③ ④
④ ⑤
⑤ ⑥熔融的
⑥熔融的 ⑦氨水⑧稀硝酸⑨
⑦氨水⑧稀硝酸⑨
(1)上述九种物质中有两种物质之间可发生离子反应:
 ,该离子反应对应的化学方程式为
,该离子反应对应的化学方程式为(2)⑨在水中的电离方程式为
(3)以上属于电解质的共有
(4)将少量的③通入⑤的溶液中反应的离子方程式为
(5)
 和③都属于酸性氧化物,尝试写出
和③都属于酸性氧化物,尝试写出 与氢氧化钠溶液反应的离子方程式:
与氢氧化钠溶液反应的离子方程式:(6)配平②与⑧发生反应的化学方程式,并用双线桥法标明该反应中电子转移的方向和数目
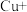



 ,
, 发生反应时,转移电子的个数为
发生反应时,转移电子的个数为 发生反应时被还原的
发生反应时被还原的 的个数为
的个数为
您最近一年使用:0次



