现有下列10种物质:
① ②熔融的
②熔融的 ③盐酸 ④
③盐酸 ④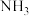 ⑤
⑤ ⑥
⑥ 固体 ⑦纯净醋酸 ⑧氢氧化铁胶体 ⑨乙醇
固体 ⑦纯净醋酸 ⑧氢氧化铁胶体 ⑨乙醇
(1)上述物质中能导电的有___________ (填序号,下同)。
(2)属于电解质的有___________ ,属于弱电解质的有___________ ,属于非电解质的有___________ 。
(3)向⑧中逐滴加入③,该过程中可观察到现象为___________ ,其中反应的离子方程式为___________ 。
(4)若用实验证明⑥中含氯元素,你的操作方法是___________ 。
①
 ②熔融的
②熔融的 ③盐酸 ④
③盐酸 ④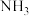 ⑤
⑤ ⑥
⑥ 固体 ⑦纯净醋酸 ⑧氢氧化铁胶体 ⑨乙醇
固体 ⑦纯净醋酸 ⑧氢氧化铁胶体 ⑨乙醇(1)上述物质中能导电的有
(2)属于电解质的有
(3)向⑧中逐滴加入③,该过程中可观察到现象为
(4)若用实验证明⑥中含氯元素,你的操作方法是
更新时间:2023-10-02 20:52:41
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】有下列物质:①Na2CO3•10H2O晶体②铜③硫酸溶液④CO2⑤KHSO4固体⑥Ba(OH)2固体⑦红褐色的氢氧化铁胶体⑧氨水⑨稀硝酸⑩Al2(SO4)3固体。
(1)上述物质属于电解质的有_______ (填编号),能导电的物质有_______ (填编号)。
(2)上述物质中有两种物质之间可发生离子反应:H++OH-=H2O,写出该离子反应对应的化学方程式_______ 。
(3)写出固体⑤熔化时的电离方程式_______ 。
(4)写出⑦的制备方程式_______ 。
(1)上述物质属于电解质的有
(2)上述物质中有两种物质之间可发生离子反应:H++OH-=H2O,写出该离子反应对应的化学方程式
(3)写出固体⑤熔化时的电离方程式
(4)写出⑦的制备方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】胶体是一种常见的分散系,回答下列问题:
(1)向大量沸腾的蒸馏水中滴加几滴___________ 溶液,继续加热至___________ ,停止加热,可制得 胶体;
胶体;
(2)用激光笔照射 胶体,观察到的现象是
胶体,观察到的现象是___________ 。将此液体加入浑浊的水中,静置一段时间后水变得较澄清,试从微观角度分析原因___________ ;
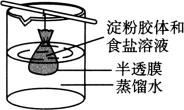
(3)如图所示,将淀粉与 形成的混合液放入半透膜中。下列说法正确的是
形成的混合液放入半透膜中。下列说法正确的是
(1)向大量沸腾的蒸馏水中滴加几滴
 胶体;
胶体;(2)用激光笔照射
 胶体,观察到的现象是
胶体,观察到的现象是(3)如图所示,将淀粉与
 形成的混合液放入半透膜中。下列说法正确的是
形成的混合液放入半透膜中。下列说法正确的是
| A.能用丁达尔效应区分淀粉胶体和泥浆 |
B.该半透膜的孔径大小可能为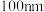 |
| C.本操作需要若干次更换烧杯内的蒸馏水 |
| D.取少量烧杯中的液体于试管中,滴加几滴碘水后溶液变蓝色 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】纳米铁是一种黑色粉末,分散于水中形成纳米铁胶体,纳米铁可用于制作高密度磁性记录材料、磁性液体、电磁波吸收材料等。
(1)证明纳米铁粉分散于水中形成的是胶体的简单方法是_______ 。
(2)一种制备纳米铁粉的实验步骤如下:

①洗涤时,能说明固体已洗涤干净的依据是_______ 。
②当草酸亚铁全部转变为纳米铁粉时,将纳米铁粉快速倒在石棉网上,纳米铁粉立刻发生自燃并产生火星,上层为红棕色粉末,下层为黑色粉末,上层红棕色物质为_______ (填化学式)。
(3)活性炭负载纳米铁可高效去除含铬强酸性废水中的六价铬(以Cr2O 表示),其原理为在强酸性条件下Cr2O
表示),其原理为在强酸性条件下Cr2O 首先被Fe2+还原为Cr3+,随溶液pH上升(pH始终小于7)再形成CrxFe1-x(OH)3沉淀而除去。上述两步反应的离子方程式分别是
首先被Fe2+还原为Cr3+,随溶液pH上升(pH始终小于7)再形成CrxFe1-x(OH)3沉淀而除去。上述两步反应的离子方程式分别是_______ ,_______ 。
(1)证明纳米铁粉分散于水中形成的是胶体的简单方法是
(2)一种制备纳米铁粉的实验步骤如下:

①洗涤时,能说明固体已洗涤干净的依据是
②当草酸亚铁全部转变为纳米铁粉时,将纳米铁粉快速倒在石棉网上,纳米铁粉立刻发生自燃并产生火星,上层为红棕色粉末,下层为黑色粉末,上层红棕色物质为
(3)活性炭负载纳米铁可高效去除含铬强酸性废水中的六价铬(以Cr2O
 表示),其原理为在强酸性条件下Cr2O
表示),其原理为在强酸性条件下Cr2O 首先被Fe2+还原为Cr3+,随溶液pH上升(pH始终小于7)再形成CrxFe1-x(OH)3沉淀而除去。上述两步反应的离子方程式分别是
首先被Fe2+还原为Cr3+,随溶液pH上升(pH始终小于7)再形成CrxFe1-x(OH)3沉淀而除去。上述两步反应的离子方程式分别是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有以下物质:①NaCl晶体 ②液态SO3 ③铁(Fe) ④BaSO4固体 ⑤纯蔗糖(C12H22O11) ⑥熔化的KNO3。
请回答下列问题(用序号)
(1)以上物质中能导电的是________ 。
(2)以上物质中属于电解质的是________ 。
(3)以上物质中属于非电解质的是________ 。
(4)以上物质中溶于水后形成的水溶液能导电的是________ 。
请回答下列问题(用序号)
(1)以上物质中能导电的是
(2)以上物质中属于电解质的是
(3)以上物质中属于非电解质的是
(4)以上物质中溶于水后形成的水溶液能导电的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】以下有10种物质:①铜 ②硫酸溶液 ③氯化氢 ④氨气 ⑤空气 ⑥冰醋酸 ⑦酒精 ⑧氯化钠 ⑨硫酸钡 ⑩氢氧化钾。按照表中提示的信息,把符合左栏条件的物质的序号填入右栏相应的位置。
符号 | 符合的条件 | 物质的对应序号 |
(1) | 混合物 | |
(2) | 电解质,但熔融状态下并不导电 | |
(3) | 属于盐的强电解质 | |
(4) | 非电解质 | |
(5) | 既不是电解质,也不是非电解质,但本身能导电 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)现有以下物质①NaCl溶液② CO2③铜④ BaSO4固体⑤蔗糖⑥酒精⑦熔融的 KNO3,其中属于电解质的是 ________ (填上序号,下同), 属于非电解质的是 ________ ,能够导电的是__________ 。
(2)写出下列反应的离子方程式:
①碳酸钠溶液与盐酸混合________________________
②硫酸铜溶液和氢氧化钡溶液混合________________________
(3)写出一个与离子方程式2H++CaCO3 =Ca2+ +CO2↑+H2O 相对应的反应化学方程式:__________________________________________
(2)写出下列反应的离子方程式:
①碳酸钠溶液与盐酸混合
②硫酸铜溶液和氢氧化钡溶液混合
(3)写出一个与离子方程式2H++CaCO3 =Ca2+ +CO2↑+H2O 相对应的反应化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求回答下列问题:
(1)下列几种物质:①铜丝②液态HCl③SO3④Ba(OH)2溶液⑤氨水⑥硫酸⑦NaHSO4固体⑧熔融KNO3⑨蔗糖⑩CuSO4·5H2O晶体。
根据要求回答下列问题:
以上物质中能导电的是_______ (填序号,下同);属于电解质的是__________ ;写出物质⑦在水溶液中的电离方程式_________ 。
(2)下列微粒:在S2-、Fe2+、Al3+、HCl、Cu、I-、H+在化学反应中只能被氧化的是_____ ,只有氧化性的是________ ,既有氧化性又有还原性的是_________ 。
(1)下列几种物质:①铜丝②液态HCl③SO3④Ba(OH)2溶液⑤氨水⑥硫酸⑦NaHSO4固体⑧熔融KNO3⑨蔗糖⑩CuSO4·5H2O晶体。
根据要求回答下列问题:
以上物质中能导电的是
(2)下列微粒:在S2-、Fe2+、Al3+、HCl、Cu、I-、H+在化学反应中只能被氧化的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下表是生活生产中常见的物质:
(1)分别写出③、⑥的电离方程式__________ ;__________ 。
(2)③与⑥反应的离子方程式:__________ 。
(3)检验⑤的溶液中含有 的方法是:
的方法是:__________ ,有关的离子方程式为__________ 。
(4)常温下,将 通入②中,可以得到一种漂白液,该漂白液的有效成分为
通入②中,可以得到一种漂白液,该漂白液的有效成分为__________ (填名称),检验中②阳离子的方法是__________ (填名称)。
编号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
名称 | Na |
|
| 酒精 |
|
|
(2)③与⑥反应的离子方程式:
(3)检验⑤的溶液中含有
 的方法是:
的方法是:(4)常温下,将
 通入②中,可以得到一种漂白液,该漂白液的有效成分为
通入②中,可以得到一种漂白液,该漂白液的有效成分为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】如图是氮元素的几种价态与物质类别的对应关系。请回答下列问题:
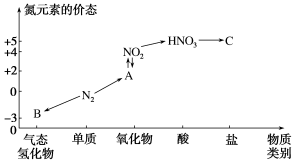
(1)写出N2的一种用途:_______ 。
(2)硝酸一般盛放在棕色试剂瓶中,请用化学方程式说明其原因:_______ 。
(3)HNO3与图中的物质C常用于检验Cl-的存在,则C的化学式为_______ 。
(4)实验室物质B的催化氧化是工业制硝酸的基础,其化学方程式为_______ 。
(5)从N元素化合价角度分析,图中涉及的六种物质只有还原性的是_______ (填化学式,下同),既有氧化性又有还原性的是_______ 。

(1)写出N2的一种用途:
(2)硝酸一般盛放在棕色试剂瓶中,请用化学方程式说明其原因:
(3)HNO3与图中的物质C常用于检验Cl-的存在,则C的化学式为
(4)实验室物质B的催化氧化是工业制硝酸的基础,其化学方程式为
(5)从N元素化合价角度分析,图中涉及的六种物质只有还原性的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】NaCl是一种化工原料,可以制备多种物质,如图所示。请回答下列问题:

(1)工业上制取NaOH主要采用反应①,而不采用反应⑦的方法,主要原因是___________ 。
(2)NaClO是“84消毒液”的有效成分,在抗击新冠肺炎疫情中发挥了重要作用。“84消毒液”不能与“洁厕灵(主要成分是HCl)”混合使用,否则会产生黄绿色的有毒气体引起安全事故,其反应的离子方程式是___________ 。
(3)反应③和⑧是工业制备纯碱的原理,我国化学工业科学家侯德榜提出了将氨碱法(又称索尔维法)制取碳酸钠和合成氨联合的改进工艺,这就是联合制碱法,也称侯氏制碱法。侯氏制碱法提高了食盐的转化率,缩短了生产流程,减少了对环境的污染,将制碱技术发展到了一个新的水平,赢得了国际化工界的高度评价。以下是这两种制碱法的工艺流程图:
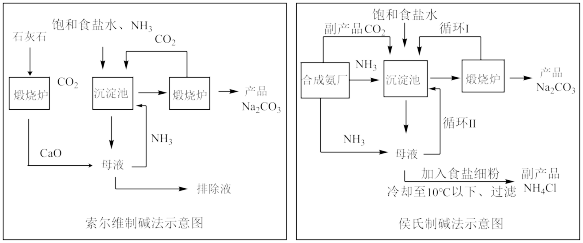
下列说法正确的是___________ (填序号)。
A.用NaCl制取纯碱的过程中,利用了物质溶解度的差异
B.沉淀池中NH3与CO2的通入顺序为先通入CO2,再通入NH3
C.索尔维制碱法所得“排出液”的主要成分为CaCl2
D.侯氏制碱法循环利用的物质主要是CO2和NH3
E.侯氏制碱法从母液中经过循环Ⅱ进入沉淀池的主要有NH3·H2O、NH4Cl、Na2CO3,从而使原料NaCl的利用率大大提升
F.侯氏制碱法在母液中加入食盐细粉目的是提高Na+的浓度,促进碳酸氢钠结晶析出
G.检验产品Na2CO3中是否含有NaCl的操作方法是取少量试样溶于水,加入过量的稀硝酸,再滴加硝酸银溶液,观察是否有白色沉淀生成

(1)工业上制取NaOH主要采用反应①,而不采用反应⑦的方法,主要原因是
(2)NaClO是“84消毒液”的有效成分,在抗击新冠肺炎疫情中发挥了重要作用。“84消毒液”不能与“洁厕灵(主要成分是HCl)”混合使用,否则会产生黄绿色的有毒气体引起安全事故,其反应的离子方程式是
(3)反应③和⑧是工业制备纯碱的原理,我国化学工业科学家侯德榜提出了将氨碱法(又称索尔维法)制取碳酸钠和合成氨联合的改进工艺,这就是联合制碱法,也称侯氏制碱法。侯氏制碱法提高了食盐的转化率,缩短了生产流程,减少了对环境的污染,将制碱技术发展到了一个新的水平,赢得了国际化工界的高度评价。以下是这两种制碱法的工艺流程图:

下列说法正确的是
A.用NaCl制取纯碱的过程中,利用了物质溶解度的差异
B.沉淀池中NH3与CO2的通入顺序为先通入CO2,再通入NH3
C.索尔维制碱法所得“排出液”的主要成分为CaCl2
D.侯氏制碱法循环利用的物质主要是CO2和NH3
E.侯氏制碱法从母液中经过循环Ⅱ进入沉淀池的主要有NH3·H2O、NH4Cl、Na2CO3,从而使原料NaCl的利用率大大提升
F.侯氏制碱法在母液中加入食盐细粉目的是提高Na+的浓度,促进碳酸氢钠结晶析出
G.检验产品Na2CO3中是否含有NaCl的操作方法是取少量试样溶于水,加入过量的稀硝酸,再滴加硝酸银溶液,观察是否有白色沉淀生成
您最近一年使用:0次

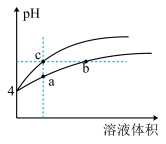

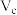 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。





