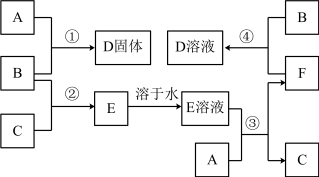
A-F 为中学化学常见物质,它们的焰色试验均为黄色。其中 A 为单质, B 与 C的组成元素相同,且 B 为淡黄色固体; D、 E、 F 的溶液均显碱性,其中 E 和 F 属于盐且相同物质的量浓度的溶液, E溶液的碱性更强。它们之间的相互转化关系如下图。(“ ”表示进一步反应即可转化,部分反应物、生成物和反应条件已略去)
”表示进一步反应即可转化,部分反应物、生成物和反应条件已略去)
请回答下列问题:
(1)写出下列物质的化学式: B___ , C___ , E___ 。
(2)A D 的化学方程式是
D 的化学方程式是_______________________ 。
(3)B D 的化学方程式是
D 的化学方程式是_______________________ 。
(4)区分 E 和 F 两种固体的方法是:分别取等量的 E 和 F 两种固体少许于试管中,具体的操作现象和结论是_________________________ 。
 ”表示进一步反应即可转化,部分反应物、生成物和反应条件已略去)
”表示进一步反应即可转化,部分反应物、生成物和反应条件已略去)
请回答下列问题:
(1)写出下列物质的化学式: B
(2)A
 D 的化学方程式是
D 的化学方程式是(3)B
 D 的化学方程式是
D 的化学方程式是(4)区分 E 和 F 两种固体的方法是:分别取等量的 E 和 F 两种固体少许于试管中,具体的操作现象和结论是
更新时间:2019-12-17 16:42:15
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色。

请填写下列空白:
(1)写出下列化学式:A________ ,B________ ,D_______ 。
(2)以上反应中,属于氧化还原反应的有______ (填写编号)。
(3)写出A→C反应的离子方程式:________ ,E→D的化学方程式:________ 。
(4)反应④中,若有标准状况下3.36L的氧气生成,则反应的CO2的质量为_____ ,此时反应中转移的电子的物质的量为_____ 。

请填写下列空白:
(1)写出下列化学式:A
(2)以上反应中,属于氧化还原反应的有
(3)写出A→C反应的离子方程式:
(4)反应④中,若有标准状况下3.36L的氧气生成,则反应的CO2的质量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
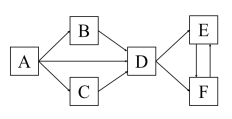
【推荐2】A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如图所示(反应条件及其他物质已经略去)。请回答下列问题:

(1)若A在常温下为固体单质,B是能使品红溶液褪色的有刺激性气味的无色气体。写出B→C的化学方程式___________ 。
(2)若A在常温下为气体单质,C是红棕色气体。
①写出化学反应方程式:A→B___________ ;B→C__________ ;
②用充满C气体(标准状态下)的圆底烧瓶做喷泉实验,实验结束时,烧瓶内硝酸的物质的量浓度为___________ mol/L。
(3)若A在常温下为非金属气态氢化物,C是红棕色气体。
①写出实验室制取A气体的化学方程式___________ 。
②写出A→B的化学方程式___________ 。
(4)若A是一种非金属单质,C是一种无色无味且能使澄清石灰水变浑浊的气体。
①写出A与 反应的化学方程式
反应的化学方程式___________ 。
②写出A与浓硫酸反应的化学方程式___________ 。

(1)若A在常温下为固体单质,B是能使品红溶液褪色的有刺激性气味的无色气体。写出B→C的化学方程式
(2)若A在常温下为气体单质,C是红棕色气体。
①写出化学反应方程式:A→B
②用充满C气体(标准状态下)的圆底烧瓶做喷泉实验,实验结束时,烧瓶内硝酸的物质的量浓度为
(3)若A在常温下为非金属气态氢化物,C是红棕色气体。
①写出实验室制取A气体的化学方程式
②写出A→B的化学方程式
(4)若A是一种非金属单质,C是一种无色无味且能使澄清石灰水变浑浊的气体。
①写出A与
 反应的化学方程式
反应的化学方程式②写出A与浓硫酸反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。

请回答下列问题:
(1)写出下列物质的化学式:B_____________ , C_______________ ,F_____________ , 乙_______________ ,
(2)写出下列反应的离子方程式:反应①____________________ ;反应⑤____________________ ;

请回答下列问题:
(1)写出下列物质的化学式:B
(2)写出下列反应的离子方程式:反应①
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知有以下物质相互转化

试回答:(1)写出B的化学式__________ ,D的化学式____________ 。
(2)写出由E转变成F的化学方程式__________________________ 。
(3)写出用KSCN鉴别G溶液的实验现象是__________ ;向G溶液加入A的有关离子反应方程式________________ 。

试回答:(1)写出B的化学式
(2)写出由E转变成F的化学方程式
(3)写出用KSCN鉴别G溶液的实验现象是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下图所涉及的物质均为中学化学中的常见物质,其中:①C、D、E、F都为单质,其余为化合物;②C、D、E在常温下为气体,其它物质为固体或液体;③A、I两种化合物的焰色反应分别为紫色和黄色;④反应①、②中的一些生成物已经略去,有些反应的条件未列出,它们存在如下转化关系。

(1)写出有关物质的化学式:A_______ ,D________ ,F_______ ,I________ 。
(2)指出MnO2在相关反应中的作用:反应①中是_______ 剂,反应②中是_______ 剂。
(3)写出B与MnO2共热获得D的化学方程式__________________________________ 。

(1)写出有关物质的化学式:A
(2)指出MnO2在相关反应中的作用:反应①中是
(3)写出B与MnO2共热获得D的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】(一)A、B、C、D、E、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。
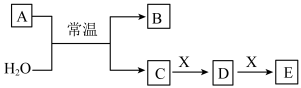
(1)若A为常见的金属单质,且其焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:___ 。
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,则X可能为__ (填字母)。
a.NaHCO3 b.Na2CO3 c.Al(OH)3 d.NaAlO2
(3)若A为淡黄色粉末,则A的电子式为___ 。若X为一种最常见的造成温室效应的气体。则鉴别等浓度的D、E两种溶液,可选择的试剂为___ 。(填字母)
a.盐酸 b.CaCl2溶液 c.氨水 d.澄清石灰水
(二)工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度均为0.1mol L-1。
L-1。
某同学欲探究该废水的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
Ⅱ.取少量溶液,加入KSCN溶液无明显变化。
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
Ⅳ.向Ⅲ 中所得溶液中加入BaCl2溶液,有白色沉淀生成。
请回答下列问题:
(1)甲同学最终确定原溶液中所含阳离子有___ ,阴离子是有___ 。(写离子符号)
(2)Ⅲ中加入少量盐酸生成无色气体的离子方程式为___ 。
(3)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体的质量为__ g。

(1)若A为常见的金属单质,且其焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,则X可能为
a.NaHCO3 b.Na2CO3 c.Al(OH)3 d.NaAlO2
(3)若A为淡黄色粉末,则A的电子式为
a.盐酸 b.CaCl2溶液 c.氨水 d.澄清石灰水
(二)工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度均为0.1mol
 L-1。
L-1。| 阳离子 | K+、Cu2+、Fe3+、Al3+、Fe2+ |
| 阴离子 | Cl-、CO32-、NO3-、SO42-、SiO32- |
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
Ⅱ.取少量溶液,加入KSCN溶液无明显变化。
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
Ⅳ.向Ⅲ 中所得溶液中加入BaCl2溶液,有白色沉淀生成。
请回答下列问题:
(1)甲同学最终确定原溶液中所含阳离子有
(2)Ⅲ中加入少量盐酸生成无色气体的离子方程式为
(3)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体的质量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】一无色气体,可能由CO2、HCl、NH3、NO2、NO、H2中的一种或几种组成。将此无色气体通过盛有浓H2SO4的洗气瓶,发现气体体积减少。继续通过装有固体Na2O2的干燥管,发现从出气管出来的气体颜色显红棕色,再将该气体全部通入盛满水倒立于水槽中的试管内,发现最后试管里仍然为一满试管液体。由此可推知:①原气体中一定含有_____________ ,一定不会有 ____________ ;②最终结果可知原气体中_______ 与________ 气体的体积比为________ 。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有A、B两种氧化物,焰色试验均为黄色,其转化关系如下图所示(其他物质均已略去)。请回答下列问题:
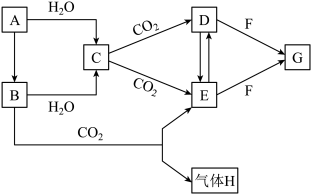
(1)写出A的化学式:___________ 。
(2)写出B→C的化学方程式:___________ 。
(3)B可与 反应生成E与气体H,该反应在生活中可用于
反应生成E与气体H,该反应在生活中可用于___________ 。
(4)有同学提议可用 溶液鉴别D与E,你认为该方案
溶液鉴别D与E,你认为该方案___________ (填“可行”或“不可行”),原因是___________ 。
(5)D与E可互相转化,请写出E→D的化学方程式:___________ 。
(6)若F为人体胃液中的主要成分,则G为___________ 。

(1)写出A的化学式:
(2)写出B→C的化学方程式:
(3)B可与
 反应生成E与气体H,该反应在生活中可用于
反应生成E与气体H,该反应在生活中可用于(4)有同学提议可用
 溶液鉴别D与E,你认为该方案
溶液鉴别D与E,你认为该方案(5)D与E可互相转化,请写出E→D的化学方程式:
(6)若F为人体胃液中的主要成分,则G为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献。下图为联合制碱法的主要过程(部分物质已略去)。
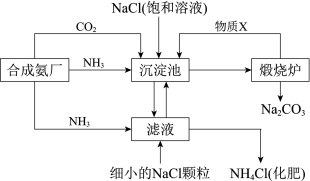
已知:i. 溶于水生成碱,与酸反应生成盐,如
溶于水生成碱,与酸反应生成盐,如 。
。
ⅱ.有关物质的溶解度(20℃)
(1)煅烧炉中反应的化学方程式为_______ ,物质X是_______ 。沉淀池中发生反应的化学方程式为_______ 。
(2)下列说法正确的是_______ (填字母)。
A.沉淀池中有 析出,因为一定条件下
析出,因为一定条件下 的溶解度最小
的溶解度最小
B.滤液中主要含有NaCl、 和
和
C.设计循环的目的是提高原料的利用率
(3)工业可用纯碱代替烧碱生产某些化工产品,如用饱和纯碱溶液与 反应可制得一种在生产生活中常用于漂白、消毒的物质,同时有
反应可制得一种在生产生活中常用于漂白、消毒的物质,同时有 生成,该反应的化学方程式是
生成,该反应的化学方程式是_______ 。

已知:i.
 溶于水生成碱,与酸反应生成盐,如
溶于水生成碱,与酸反应生成盐,如 。
。ⅱ.有关物质的溶解度(20℃)
| 物质 | NaCl |  |  |  |
| 溶解度/g | 36.0 | 21.7 | 9.6 | 37.2 |
(2)下列说法正确的是
A.沉淀池中有
 析出,因为一定条件下
析出,因为一定条件下 的溶解度最小
的溶解度最小B.滤液中主要含有NaCl、
 和
和
C.设计循环的目的是提高原料的利用率
(3)工业可用纯碱代替烧碱生产某些化工产品,如用饱和纯碱溶液与
 反应可制得一种在生产生活中常用于漂白、消毒的物质,同时有
反应可制得一种在生产生活中常用于漂白、消毒的物质,同时有 生成,该反应的化学方程式是
生成,该反应的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】小组同学探究 的性质及工业制法。
的性质及工业制法。
(1)用 固体配制
固体配制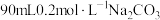 溶液。
溶液。
①用到的仪器有:托盘天平、药匙、量筒、烧杯、玻璃棒、_______ 。
②计算:需用托盘天平称量 固体
固体_______ g。
③下列情况中,会使所配溶液浓度偏低的是_______ (填字母)。
a.容量瓶中有水
b.定容时,眼睛仰视刻度线
c.定容摇匀后,发现液面低于刻度线,继续加水至液面与刻度线相切
(2)探究 与
与 的性质。完成下列填空。
的性质。完成下列填空。
(3)我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献。下图为联合制碱法的主要过程(部分物质已略去)。
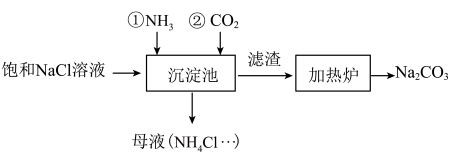
①沉淀池中发生反应的离子方程式:_______ 。
②沉淀池通入 和
和 顺序一定不能颠倒的原因:
顺序一定不能颠倒的原因:_______ 。
 的性质及工业制法。
的性质及工业制法。(1)用
 固体配制
固体配制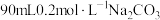 溶液。
溶液。①用到的仪器有:托盘天平、药匙、量筒、烧杯、玻璃棒、
②计算:需用托盘天平称量
 固体
固体③下列情况中,会使所配溶液浓度偏低的是
a.容量瓶中有水
b.定容时,眼睛仰视刻度线
c.定容摇匀后,发现液面低于刻度线,继续加水至液面与刻度线相切
(2)探究
 与
与 的性质。完成下列填空。
的性质。完成下列填空。| 实验装置及操作 | 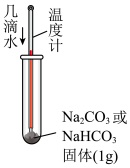 |  |  |
| 实验现象 | 盛有 | 盛有 的试管中固体完全溶解;盛有 的试管中固体完全溶解;盛有 的试管中固体有剩余 的试管中固体有剩余 | 盛有 溶液的试管中立即有气泡产生;盛有 溶液的试管中立即有气泡产生;盛有 溶液的试管中 溶液的试管中 |
| 实验结论或解释 | 略 | 相同温度下,溶解度:  (填“>”“<”或“=”) (填“>”“<”或“=”) | 略 |

①沉淀池中发生反应的离子方程式:
②沉淀池通入
 和
和 顺序一定不能颠倒的原因:
顺序一定不能颠倒的原因:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】碳酸钠和碳酸氢钠广泛的应用于我们的生产和生活中。请回答下列问题。
(1)NaHCO3是膨松剂必不可少的成分,受热时能使面胚在焙烧过程中变得松软、多孔。写出受热时NaHCO3发生反应的化学方程式_______ 。
(2)如图是某兴趣学习小组设计的验证Na2CO3比NaHCO3热稳定性强的实验装置。
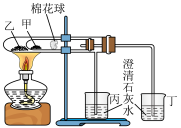
①乙处盛放固体药品的化学式是_______ ;
②变浑浊的是_______ 烧杯中的澄清石灰水。
(3)兴趣学习小组为研究膨松剂在加热情况下放出气体的量,即:根据单位质量膨松剂产生CO2气体的量来判定其膨胀效果,设计了以下实验,并按如图装置连接(气密性良好,各装置中试剂均过量)。已知:浓硫酸常用于吸收水蒸气;碱石灰是固体氢氧化钠和氧化钙的混合物。回答下列问题:

①装置A的作用为_______ 。
②如果去掉装置C,该实验会造成测定结果_______ 。(“偏大”、“不变”、“偏小”)
③加热前先通入一段时间的空气,再连接D装置,目的是_______
(1)NaHCO3是膨松剂必不可少的成分,受热时能使面胚在焙烧过程中变得松软、多孔。写出受热时NaHCO3发生反应的化学方程式
(2)如图是某兴趣学习小组设计的验证Na2CO3比NaHCO3热稳定性强的实验装置。

①乙处盛放固体药品的化学式是
②变浑浊的是
(3)兴趣学习小组为研究膨松剂在加热情况下放出气体的量,即:根据单位质量膨松剂产生CO2气体的量来判定其膨胀效果,设计了以下实验,并按如图装置连接(气密性良好,各装置中试剂均过量)。已知:浓硫酸常用于吸收水蒸气;碱石灰是固体氢氧化钠和氧化钙的混合物。回答下列问题:

①装置A的作用为
②如果去掉装置C,该实验会造成测定结果
③加热前先通入一段时间的空气,再连接D装置,目的是
您最近一年使用:0次