在人类社会的发展进程中,金属起着重要的作用。
(1)以下有关金属单质的叙述正确的是_______ 。
A.金属钠非常活泼,在实验室中保存在石蜡油或煤油中
B.用坩埚钳夹住一小块铝箔,在酒精灯上加热,可观察到铝箔熔化,并有熔融物滴下
C.铁单质与水蒸气反应的化学方程式为2Fe+3H2O(g)=Fe2O3+3H2
(2)把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16 g白色沉淀,在所得的浊液中逐滴加入1 mol·L-1 HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如下图所示,试回答:
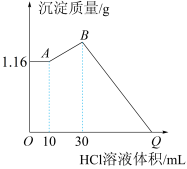
①A点的沉淀物的化学式为________ ;B点的沉淀物的化学式为________________________ ;写出A→B段发生反应的离子方程式_____________________________ 。
②原混合物中MgCl2的质量是________ g,AlCl3的质量是________ g,NaOH的质量是________ g。
③Q点HCl溶液加入量是________ mL。
(1)以下有关金属单质的叙述正确的是
A.金属钠非常活泼,在实验室中保存在石蜡油或煤油中
B.用坩埚钳夹住一小块铝箔,在酒精灯上加热,可观察到铝箔熔化,并有熔融物滴下
C.铁单质与水蒸气反应的化学方程式为2Fe+3H2O(g)=Fe2O3+3H2
(2)把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16 g白色沉淀,在所得的浊液中逐滴加入1 mol·L-1 HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如下图所示,试回答:

①A点的沉淀物的化学式为
②原混合物中MgCl2的质量是
③Q点HCl溶液加入量是
更新时间:2019-12-23 13:34:50
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】现有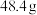 碱式碳酸镁样品(化学式:
碱式碳酸镁样品(化学式: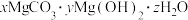 ,
, 、
、 、
、 为正整数),将其分为二等份,一份样品充分灼烧至恒重进行热重分析,结果如图所示。另一份投入
为正整数),将其分为二等份,一份样品充分灼烧至恒重进行热重分析,结果如图所示。另一份投入 某浓度的盐酸中,充分反应后生成
某浓度的盐酸中,充分反应后生成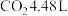 (已换算成标准状况下),测得溶液的
(已换算成标准状况下),测得溶液的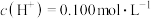 。(忽略溶液前后体积变化)
。(忽略溶液前后体积变化)

按要求回答下列问题:
(1)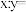
_______________ 。
(2)盐酸的物质的量浓度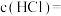
____________  。
。
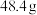 碱式碳酸镁样品(化学式:
碱式碳酸镁样品(化学式: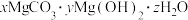 ,
, 、
、 、
、 为正整数),将其分为二等份,一份样品充分灼烧至恒重进行热重分析,结果如图所示。另一份投入
为正整数),将其分为二等份,一份样品充分灼烧至恒重进行热重分析,结果如图所示。另一份投入 某浓度的盐酸中,充分反应后生成
某浓度的盐酸中,充分反应后生成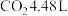 (已换算成标准状况下),测得溶液的
(已换算成标准状况下),测得溶液的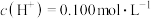 。(忽略溶液前后体积变化)
。(忽略溶液前后体积变化)
按要求回答下列问题:
(1)
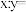
(2)盐酸的物质的量浓度
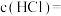
 。
。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的浊液中逐滴加入1mol•L﹣1 HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如图所示,试回答:

(1)写出混合物溶于水时发生反应的离子方程式________________________________________________ 。
(2)写出AB段反应的离子方程式__________________ 。B点的沉淀物的化学式为______________ 。
(3)求原混合物中AlCl3的物质的量____________ ,NaOH的质量________________ 。
(4)求Q点加入的HCl溶液体积.______________________ 。

(1)写出混合物溶于水时发生反应的离子方程式
(2)写出AB段反应的离子方程式
(3)求原混合物中AlCl3的物质的量
(4)求Q点加入的HCl溶液体积.
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐3】在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如下图所示。
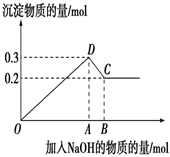
(1)写出代表下列线段发生的反应的离子方程式:
DC段________________________________________________ 。
(2)原溶液中Mg2+、Al3+的物质的量之比为_____________ 。
(3)图中B点时所加入溶液中含NaOH为________ mol
(4)若向50 mL 2 mol·L-1的AlCl3溶液中加入100 mL KOH溶液,充分反应后得到3.12g沉淀。则KOH的物质的量浓度可能为________________________________ 。

(1)写出代表下列线段发生的反应的离子方程式:
DC段
(2)原溶液中Mg2+、Al3+的物质的量之比为
(3)图中B点时所加入溶液中含NaOH为
(4)若向50 mL 2 mol·L-1的AlCl3溶液中加入100 mL KOH溶液,充分反应后得到3.12g沉淀。则KOH的物质的量浓度可能为
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】小苏打、胃舒平、达喜都是常用的中和胃酸的药物。
(1)小苏打片每片含0.42 gNaHCO3,2片小苏打片和胃酸完全中和,被中和的氢离子是
_______ mol。
(2)胃舒平每片含0.135 g Al(OH)3。中和胃酸时,6片小苏打片相当于胃舒平_____ 片。
(3)达喜的化学成分是铝和镁的碱式碳酸盐。
①取该碱式碳酸盐2.20g,加入2.0 mol·L-1盐酸使其溶解,当加入盐酸30 mL时开始产生CO2,加入盐酸至35 mL时正好反应完全,计算该碱式盐样品中氢氧根与碳酸根的物质的量之比_________ 。
②在上述碱式盐溶于盐酸后的溶液中加入过量氢氧化钠,过滤,沉淀物进行干燥后重1.16g,试推测该碱式盐的化学式_________ 。
(1)小苏打片每片含0.42 gNaHCO3,2片小苏打片和胃酸完全中和,被中和的氢离子是
(2)胃舒平每片含0.135 g Al(OH)3。中和胃酸时,6片小苏打片相当于胃舒平
(3)达喜的化学成分是铝和镁的碱式碳酸盐。
①取该碱式碳酸盐2.20g,加入2.0 mol·L-1盐酸使其溶解,当加入盐酸30 mL时开始产生CO2,加入盐酸至35 mL时正好反应完全,计算该碱式盐样品中氢氧根与碳酸根的物质的量之比
②在上述碱式盐溶于盐酸后的溶液中加入过量氢氧化钠,过滤,沉淀物进行干燥后重1.16g,试推测该碱式盐的化学式
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】NaOH、MgCl2、AlCl3的混合物溶于H2O后,加入0.5mol/L的稀盐酸溶液,变化如图,求:
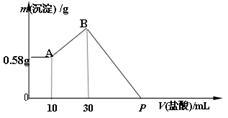
(1)混合物中NaOH的质量是_________ g。
(2)P点所表示盐酸加入体积为________ mL。

(1)混合物中NaOH的质量是
(2)P点所表示盐酸加入体积为
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】实验室中有甲﹑乙两瓶丢失标签的无色溶液,其中一瓶是盐酸,另一瓶是碳酸钠溶液。为确定甲﹑乙两瓶溶液的成分及其物质的量浓度,现操作如下:
①量取25.00mL甲溶液,向其中缓缓滴加乙溶液15.00mL,共收集到CO2气体224mL﹙标况﹚。②量取15.00mL乙溶液,向其中缓缓滴加甲溶液25.00mL,共收集到CO2气体112mL﹙标况﹚。
请回答:
(1)根据上述两种不同操作过程及实验数据可判断甲溶液是________________ (填名称)
(2)甲溶液的物质的量浓度为________________ mol﹒L-1 ,乙溶液的物质的量浓度为________________ mol﹒L-1 ﹙忽略CO2在溶液中的少量溶解﹚。
(3)若用类似上述“互滴”的方式。
①将100 mL 3mol/L的NaAlO2溶液逐滴加到50mL12mol/L的HCl溶液中,充分反应。写出发生反应的总反应离子方程式_____________________________________ 。
②将50mL12mol/L的HCl溶液逐滴加入100 mL 3mol/L的NaAlO2溶液中,充分反应。两种混合方式生成沉淀的量是否相等________________ (填“相等”或“不相等”)
①量取25.00mL甲溶液,向其中缓缓滴加乙溶液15.00mL,共收集到CO2气体224mL﹙标况﹚。②量取15.00mL乙溶液,向其中缓缓滴加甲溶液25.00mL,共收集到CO2气体112mL﹙标况﹚。
请回答:
(1)根据上述两种不同操作过程及实验数据可判断甲溶液是
(2)甲溶液的物质的量浓度为
(3)若用类似上述“互滴”的方式。
①将100 mL 3mol/L的NaAlO2溶液逐滴加到50mL12mol/L的HCl溶液中,充分反应。写出发生反应的总反应离子方程式
②将50mL12mol/L的HCl溶液逐滴加入100 mL 3mol/L的NaAlO2溶液中,充分反应。两种混合方式生成沉淀的量是否相等
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】硅酸盐材料具有硬度高、难溶于水、耐高温等特点。硅酸盐中常含有Al、K等元素,如钾长石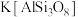 和钠长石
和钠长石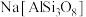 等。回答下列问题:
等。回答下列问题:
(1)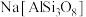 用氧化物形式表示为
用氧化物形式表示为_______ 。
(2)我国科学家发现在200℃熔盐体系中,采用金属Al还原钾长石等制备纳米硅材料的方法,将该材料应用于锂离子电池负极材料,展示出优异的电化学性能。配平下列方程式:_______ 。
______Al+______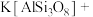 ______
______ →______Si+_____AlOCl+_____
→______Si+_____AlOCl+_____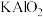 。
。
(3)将钾长石或钠长石用足量稀盐酸处理后,所得固体为_______ (填化学式)。
(4)将一定质量的铝粉和铁粉的混合物加入到一定量很稀的硝酸溶液中,充分反应,反应过程中无气体放出。向反应结束后的溶液中,逐滴加入5mol∙L-1的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量(n)关系如图所示:
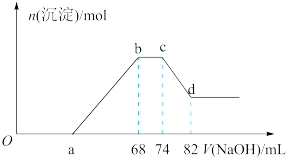
①根据关系图,写出Fe与稀硝酸反应的离子方程式:_______ 。
②样品中铝粉和铁粉的物质的量之比为_______ 。
③a点对应NaOH溶液的体积为_______ 。
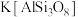 和钠长石
和钠长石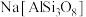 等。回答下列问题:
等。回答下列问题:(1)
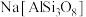 用氧化物形式表示为
用氧化物形式表示为(2)我国科学家发现在200℃熔盐体系中,采用金属Al还原钾长石等制备纳米硅材料的方法,将该材料应用于锂离子电池负极材料,展示出优异的电化学性能。配平下列方程式:
______Al+______
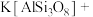 ______
______ →______Si+_____AlOCl+_____
→______Si+_____AlOCl+_____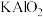 。
。(3)将钾长石或钠长石用足量稀盐酸处理后,所得固体为
(4)将一定质量的铝粉和铁粉的混合物加入到一定量很稀的硝酸溶液中,充分反应,反应过程中无气体放出。向反应结束后的溶液中,逐滴加入5mol∙L-1的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量(n)关系如图所示:

①根据关系图,写出Fe与稀硝酸反应的离子方程式:
②样品中铝粉和铁粉的物质的量之比为
③a点对应NaOH溶液的体积为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】某同学取一定质量的铁铝合金与100 mLxmol/L稀硝酸充分反应,反应过程中没有气体放出。在反应结束后的溶液中,逐滴加入2 mol/L NaOH溶液,所加 NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)的关系如图所示:

(1)写出EF段发生反应的离子方程式____________
(2)C点对应的溶液中含有的阳离子除Na+外,还含有_______ 。
(3)x =________ 。
(4)铁铝合金中铝的物质的量分数为_________ 。

(1)写出EF段发生反应的离子方程式
(2)C点对应的溶液中含有的阳离子除Na+外,还含有
(3)x =
(4)铁铝合金中铝的物质的量分数为
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐3】在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如下图所示。

(1)写出代表下列线段发生的反应的离子方程式:
DC段________________________________________________ 。
(2)原溶液中Mg2+、Al3+的物质的量之比为_____________ 。
(3)图中B点时所加入溶液中含NaOH为________ mol
(4)若向50 mL 2 mol·L-1的AlCl3溶液中加入100 mL KOH溶液,充分反应后得到3.12g沉淀。则KOH的物质的量浓度可能为________________________________ 。

(1)写出代表下列线段发生的反应的离子方程式:
DC段
(2)原溶液中Mg2+、Al3+的物质的量之比为
(3)图中B点时所加入溶液中含NaOH为
(4)若向50 mL 2 mol·L-1的AlCl3溶液中加入100 mL KOH溶液,充分反应后得到3.12g沉淀。则KOH的物质的量浓度可能为
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐1】如图是向MgCl2、AlCl3混合溶液中,开始滴加试剂A,之后改滴试剂B,所得沉淀ymol 与试剂体积V(mL)间的关系。请回答

(1)写出c~d段发生反应的离子方程式______________________________________
(2)原溶液中Mg2+、Al3+、Cl−的物质的量浓度之比为:_______________________
(3)如果A和B为一元强酸或一元强碱,则c(A):c(B)=_____________________
(4)图中e点处V=_______________ (填数字)

(1)写出c~d段发生反应的离子方程式
(2)原溶液中Mg2+、Al3+、Cl−的物质的量浓度之比为:
(3)如果A和B为一元强酸或一元强碱,则c(A):c(B)=
(4)图中e点处V=
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】把由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水中,有0.58g白色难溶物析出,向所得溶液中逐滴加入0.5mol·L−1的盐酸,加入盐酸的体积和生成沉淀的质量如图所示:
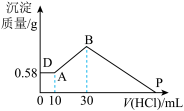
请计算:
(1)混合物中MgCl2的质量__________ g;
(2)P点表示盐酸加入的体积_________ ml。

请计算:
(1)混合物中MgCl2的质量
(2)P点表示盐酸加入的体积
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】实验室中有甲﹑乙两瓶丢失标签的无色溶液,其中一瓶是盐酸,另一瓶是碳酸钠溶液。为确定甲﹑乙两瓶溶液的成分及其物质的量浓度,现操作如下:
①量取25.00mL甲溶液,向其中缓缓滴加乙溶液15.00mL,共收集到CO2气体224mL﹙标况﹚。②量取15.00mL乙溶液,向其中缓缓滴加甲溶液25.00mL,共收集到CO2气体112mL﹙标况﹚。
请回答:
(1)根据上述两种不同操作过程及实验数据可判断甲溶液是________________ (填名称)
(2)甲溶液的物质的量浓度为________________ mol﹒L-1 ,乙溶液的物质的量浓度为________________ mol﹒L-1 ﹙忽略CO2在溶液中的少量溶解﹚。
(3)若用类似上述“互滴”的方式。
①将100 mL 3mol/L的NaAlO2溶液逐滴加到50mL12mol/L的HCl溶液中,充分反应。写出发生反应的总反应离子方程式_____________________________________ 。
②将50mL12mol/L的HCl溶液逐滴加入100 mL 3mol/L的NaAlO2溶液中,充分反应。两种混合方式生成沉淀的量是否相等________________ (填“相等”或“不相等”)
①量取25.00mL甲溶液,向其中缓缓滴加乙溶液15.00mL,共收集到CO2气体224mL﹙标况﹚。②量取15.00mL乙溶液,向其中缓缓滴加甲溶液25.00mL,共收集到CO2气体112mL﹙标况﹚。
请回答:
(1)根据上述两种不同操作过程及实验数据可判断甲溶液是
(2)甲溶液的物质的量浓度为
(3)若用类似上述“互滴”的方式。
①将100 mL 3mol/L的NaAlO2溶液逐滴加到50mL12mol/L的HCl溶液中,充分反应。写出发生反应的总反应离子方程式
②将50mL12mol/L的HCl溶液逐滴加入100 mL 3mol/L的NaAlO2溶液中,充分反应。两种混合方式生成沉淀的量是否相等
您最近一年使用:0次



