有一学生在实验室测某溶液的pH。实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测。
(1)该学生的操作是________ (填“正确”或“错误”),其理由是______________ 。
(2)若用此法分别测定c(H+)相等的盐酸与醋酸溶液的pH,误差较大是__________ ,其理由是__________ 。
(3)用湿润的pH试纸测定下列溶液的pH,测定结果不变的是__________ 。
A HCl溶液 B NaOH溶液 C Na2SO4溶液 D 氨水
(1)该学生的操作是
(2)若用此法分别测定c(H+)相等的盐酸与醋酸溶液的pH,误差较大是
(3)用湿润的pH试纸测定下列溶液的pH,测定结果不变的是
A HCl溶液 B NaOH溶液 C Na2SO4溶液 D 氨水
更新时间:2020-01-01 19:57:03
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.现有pH=2的醋酸溶液甲和pH=2的盐酸乙,请根据下列操作回答问题:
(1)取10 mL的甲溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中 的比值将
的比值将____________ (填“增大”、“减小”或“无法确定”)。
(2)相同条件下,取等体积的甲、乙两溶液,各稀释100倍。稀释后的溶液,其pH大小关系为:pH甲________ pH乙(填“大于”、“小于”或“等于”)。
(3)各取25 mL的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和至pH=7,则消耗的NaOH溶液的体积大小关系为: V甲_____ V乙(填“大于”、“小于”或“等于”)。
Ⅱ.有一学生在实验室测某溶液的pH。实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测。
(1)该学生的操作是______________ (填“正确的”或“不正确的”)。
(2)若用此法分别测定c (H+)相等的盐酸和醋酸溶液的pH,误差较大的是___________ 。
(1)取10 mL的甲溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中
 的比值将
的比值将(2)相同条件下,取等体积的甲、乙两溶液,各稀释100倍。稀释后的溶液,其pH大小关系为:pH甲
(3)各取25 mL的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和至pH=7,则消耗的NaOH溶液的体积大小关系为: V甲
Ⅱ.有一学生在实验室测某溶液的pH。实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测。
(1)该学生的操作是
(2)若用此法分别测定c (H+)相等的盐酸和醋酸溶液的pH,误差较大的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】金属表面处理、皮革鞣制、印染等都可能造成铬污染。六价铬比三价铬毒性高,更易被人体吸收且在体内蓄积。根据要求,回答下列问题:
(1)工业上处理含 的酸性废水的方法如下:
的酸性废水的方法如下:
①向含 的酸性废水中加入
的酸性废水中加入 溶液,使
溶液,使 全部转化为
全部转化为 ,反应的离子方程式为
,反应的离子方程式为_______ 。
②调节溶液的 ,使
,使 完全沉淀。实验室粗略测定溶液的
完全沉淀。实验室粗略测定溶液的 的方法为
的方法为_______ 。
(2)铬元素总浓度的测定:准确移取 含
含 和
和 的酸性废水,向其中加入足量的
的酸性废水,向其中加入足量的 溶液将
溶液将 氧化成
氧化成 ,煮沸除去过量的
,煮沸除去过量的 ;上述溶液中加入过量的
;上述溶液中加入过量的 溶液,充分反应后,以淀粉溶液为指示剂,向其中滴加
溶液,充分反应后,以淀粉溶液为指示剂,向其中滴加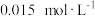 的
的 标准溶液,终点时消耗
标准溶液,终点时消耗 溶液
溶液 。废水中铬元素的总浓度为
。废水中铬元素的总浓度为_______ 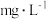 。已知测定过程中发生的反应如下:
。已知测定过程中发生的反应如下:
①
②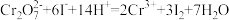
③
(1)工业上处理含
 的酸性废水的方法如下:
的酸性废水的方法如下:①向含
 的酸性废水中加入
的酸性废水中加入 溶液,使
溶液,使 全部转化为
全部转化为 ,反应的离子方程式为
,反应的离子方程式为②调节溶液的
 ,使
,使 完全沉淀。实验室粗略测定溶液的
完全沉淀。实验室粗略测定溶液的 的方法为
的方法为(2)铬元素总浓度的测定:准确移取
 含
含 和
和 的酸性废水,向其中加入足量的
的酸性废水,向其中加入足量的 溶液将
溶液将 氧化成
氧化成 ,煮沸除去过量的
,煮沸除去过量的 ;上述溶液中加入过量的
;上述溶液中加入过量的 溶液,充分反应后,以淀粉溶液为指示剂,向其中滴加
溶液,充分反应后,以淀粉溶液为指示剂,向其中滴加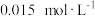 的
的 标准溶液,终点时消耗
标准溶液,终点时消耗 溶液
溶液 。废水中铬元素的总浓度为
。废水中铬元素的总浓度为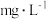 。已知测定过程中发生的反应如下:
。已知测定过程中发生的反应如下:①

②
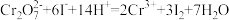
③

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某研究性学习小组为了证明某酸HmA是强酸还是弱酸,设计了如下实验方案,请回答有关问题:
⑴当m=1时,测定0.1mol/L HA的pH值,若0.1mol/L HA的pH>1,说明HA为____ 酸(填“强”、 “弱”)。测定0.1mol/L HA的值时,pH试纸预先_________ 用蒸馏水湿润(填“能”、“不能”)。
⑵取少量NamA固体溶于蒸馏水,再向得到的溶液中滴加2滴石蕊,若溶液由无色变成蓝色,证明HmA是________ 酸(填“强”、 “弱”)。若某浓度的NamA溶液pH=9,则该溶液中,水电离的c(H+)=___________ mol/L;
⑶室温下,将pH=2的酸HmA和pH=12的B(OH)n等体积混合,测得混合液的pH=8。
①写出生成正盐的化学方程式____________________ ;
②若该盐中只有一种能水解的离子,则HmA为______ 酸(填“强”、 “弱”), 离子水解的方程式为_____________________ ;
⑷现有某浓度的HmA溶液,蒸馏水,常见指示剂(如:石蕊、酚酞),pH试纸以及常用实验仪器,请你设计一种简单可行的实验方案,证明HmA是强酸还是弱酸。简述实验过程、现象、结论:_________________________ 。
⑴当m=1时,测定0.1mol/L HA的pH值,若0.1mol/L HA的pH>1,说明HA为
⑵取少量NamA固体溶于蒸馏水,再向得到的溶液中滴加2滴石蕊,若溶液由无色变成蓝色,证明HmA是
⑶室温下,将pH=2的酸HmA和pH=12的B(OH)n等体积混合,测得混合液的pH=8。
①写出生成正盐的化学方程式
②若该盐中只有一种能水解的离子,则HmA为
⑷现有某浓度的HmA溶液,蒸馏水,常见指示剂(如:石蕊、酚酞),pH试纸以及常用实验仪器,请你设计一种简单可行的实验方案,证明HmA是强酸还是弱酸。简述实验过程、现象、结论:
您最近一年使用:0次



