按要求回答下列问题。
(1)磷酸钠(Na3PO4)在水溶液中的电离方程式为__ 。
(2)镁条在氮气中燃烧的化学方程式为___ 。
(3)过氧化钠与水反应的化学方程式为___ 。该反应中,氧化剂是___ ,还原剂是___ 。
(4)浓硫酸和碳在加热条件下反应的化学方程式为___ 。
(1)磷酸钠(Na3PO4)在水溶液中的电离方程式为
(2)镁条在氮气中燃烧的化学方程式为
(3)过氧化钠与水反应的化学方程式为
(4)浓硫酸和碳在加热条件下反应的化学方程式为
更新时间:2020-01-11 14:02:15
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】现有下列十种物质①碳酸氢钠粉末②酒精③氨水④HCl气体⑤Fe⑥稀硫酸⑦熔融NaCl⑧KOH溶液⑨CO2气体⑩CuSO4·5H2O晶体
(1)属于电解质的是___________ (填序号),属于非电解质的是___________ (填序号)。
(2)上述状态下能导电的是___________ (填序号)。
(3)写出①在水溶液中的电离方程式:___________ ;
(4)①的溶液与⑧反应的离子方程式为:___________ 。
(1)属于电解质的是
(2)上述状态下能导电的是
(3)写出①在水溶液中的电离方程式:
(4)①的溶液与⑧反应的离子方程式为:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】化学与生活密切相关,回答下列问题:
(1)豆浆中加入适量胆水(含 等)能形成豆腐,是因为胶体遇电解质发生
等)能形成豆腐,是因为胶体遇电解质发生_______ 。
(2)铁与水难反应,但在高温条件下与水蒸气反应,生成的固体物质为_______ (写化学式)。
(3)明矾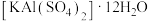 是一种常用净水剂。写出
是一种常用净水剂。写出 溶于水的电离方程式
溶于水的电离方程式_______ 。
(4)“84”消毒液与洁厕灵(主要成分为 )混用会生成有毒的氯气,反应方程式为
)混用会生成有毒的氯气,反应方程式为 。该反应中还原剂是
。该反应中还原剂是_______ ,用双线桥表示该反应中电子转移方向和数目_______ 。
(5)硅胶常用作袋装食品的干燥剂,原因是_______ (用适当的文字描述)。
(1)豆浆中加入适量胆水(含
 等)能形成豆腐,是因为胶体遇电解质发生
等)能形成豆腐,是因为胶体遇电解质发生(2)铁与水难反应,但在高温条件下与水蒸气反应,生成的固体物质为
(3)明矾
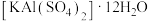 是一种常用净水剂。写出
是一种常用净水剂。写出 溶于水的电离方程式
溶于水的电离方程式(4)“84”消毒液与洁厕灵(主要成分为
 )混用会生成有毒的氯气,反应方程式为
)混用会生成有毒的氯气,反应方程式为 。该反应中还原剂是
。该反应中还原剂是(5)硅胶常用作袋装食品的干燥剂,原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】按要求写出下列反应的方程式:
(1)氯气和水反应的离子方程式:_______ ;
(2)过量铁粉在氯气中燃烧的化学方程式:_______ ;
(3)工业制漂白粉的化学方程式:_______ ;
(4)漂白粉工作原理的化学方程式:_______ ;
(5)Ca(OH)2溶液与足量的NaHCO3溶液反应的离子方程式:_______ ;
(6)碳酸氢钠的电离方程式:_______ ;
(7)氢氧化铜的电离方程式:_______ ;
(8)Na与水反应的离子方程式:_______ ;
(9)Na2O2与二氧化碳反应的化学方程式:_______ ;
(10)Na2CO3溶液与少量盐酸反应的离子方程式:_______ 。
(1)氯气和水反应的离子方程式:
(2)过量铁粉在氯气中燃烧的化学方程式:
(3)工业制漂白粉的化学方程式:
(4)漂白粉工作原理的化学方程式:
(5)Ca(OH)2溶液与足量的NaHCO3溶液反应的离子方程式:
(6)碳酸氢钠的电离方程式:
(7)氢氧化铜的电离方程式:
(8)Na与水反应的离子方程式:
(9)Na2O2与二氧化碳反应的化学方程式:
(10)Na2CO3溶液与少量盐酸反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】硫及其化合物广泛存在于自然界中,硫的部分化合物相互转化关系如图所示。回答下列问题: 与NaOH溶液反应可实现转化
与NaOH溶液反应可实现转化______ (填图中的序号),由该反应推断。 属于
属于______ (填“酸性”或“碱性”)氧化物。
(2)在转化②中,硫元素的化合价由+4价变成+6价,这表明 具有
具有______ (填“氧化性”或“还原性”)。
(3) 还具有氧化性,
还具有氧化性, 与
与 反应可生成
反应可生成______ (填化学式)和 ,该反应可发生在火山口附近的大气中,这是自然界中硫单质存在于火山口附近的原因之一。
,该反应可发生在火山口附近的大气中,这是自然界中硫单质存在于火山口附近的原因之一。
(4)在加热条件下,Cu与浓硫酸反应可实现转化③,该反应中 被Cu
被Cu______ (填“氧化”或“还原”)成 。
。 能使
能使______ (填试剂名称)溶液褪色,说明 具有漂白性,因此可用作草帽、纸张等的漂白剂。
具有漂白性,因此可用作草帽、纸张等的漂白剂。
(5)为检验Cu与浓硫酸反应后溶液中的 ,取少量稀释后的溶液,加入少量稀盐酸,再滴加几滴
,取少量稀释后的溶液,加入少量稀盐酸,再滴加几滴______ (填化学式)溶液,振荡,生成______ 色沉淀,则证明溶液中含有 ,生成该沉淀的离子反应方程式为
,生成该沉淀的离子反应方程式为______ 。
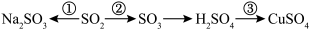
 与NaOH溶液反应可实现转化
与NaOH溶液反应可实现转化 属于
属于(2)在转化②中,硫元素的化合价由+4价变成+6价,这表明
 具有
具有(3)
 还具有氧化性,
还具有氧化性, 与
与 反应可生成
反应可生成 ,该反应可发生在火山口附近的大气中,这是自然界中硫单质存在于火山口附近的原因之一。
,该反应可发生在火山口附近的大气中,这是自然界中硫单质存在于火山口附近的原因之一。(4)在加热条件下,Cu与浓硫酸反应可实现转化③,该反应中
 被Cu
被Cu 。
。 能使
能使 具有漂白性,因此可用作草帽、纸张等的漂白剂。
具有漂白性,因此可用作草帽、纸张等的漂白剂。(5)为检验Cu与浓硫酸反应后溶液中的
 ,取少量稀释后的溶液,加入少量稀盐酸,再滴加几滴
,取少量稀释后的溶液,加入少量稀盐酸,再滴加几滴 ,生成该沉淀的离子反应方程式为
,生成该沉淀的离子反应方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】现有物质:① ②
② ③
③ ④
④ 胶体 ⑤酒精 ⑥
胶体 ⑤酒精 ⑥ ⑦
⑦ 。回答下列问题:
。回答下列问题:
(1)其中属于非电解质的是___________ (填序号)。
(2)②与⑦的浓溶液反应会产生大量气体,气体的主要成分有___________ (填化学式)。
(3)写出③的电离方程式:___________ 。
(4)提纯④的方法为___________ (填名称)。
(5)在实验室中检验气体⑥常用的试剂是___________ 。
 ②
② ③
③ ④
④ 胶体 ⑤酒精 ⑥
胶体 ⑤酒精 ⑥ ⑦
⑦ 。回答下列问题:
。回答下列问题:(1)其中属于非电解质的是
(2)②与⑦的浓溶液反应会产生大量气体,气体的主要成分有
(3)写出③的电离方程式:
(4)提纯④的方法为
(5)在实验室中检验气体⑥常用的试剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】硫酸和硝酸都是重要的化工原料,也是化学实验室里必备的重要试剂。
(1)常温下,可用铁或者铝制的容器盛放浓硝酸,说明浓硝酸具有________ 性
A.酸性 B.强氧化性 C.吸水性 D.脱水性
(2)浓H2SO4能够用于干燥某些气体,是由于它具有_____ 性;下列气体能用浓硫酸来进行干燥的是_____
①Cl2 ②H2S ③CO2 ④NH3 ⑤SO2
(3)浓H2SO4能使纸片变黑,是由于它具有____ 性;
(4)在加热条件下铜与浓硫酸反应,浓硫酸表现性质为________
(1)常温下,可用铁或者铝制的容器盛放浓硝酸,说明浓硝酸具有
A.酸性 B.强氧化性 C.吸水性 D.脱水性
(2)浓H2SO4能够用于干燥某些气体,是由于它具有
①Cl2 ②H2S ③CO2 ④NH3 ⑤SO2
(3)浓H2SO4能使纸片变黑,是由于它具有
(4)在加热条件下铜与浓硫酸反应,浓硫酸表现性质为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】填空。
(1)写出氢氧化钠与氯气反应的离子方程式___________
(2)写出氢氧化钙与氯气反应的化学方程式___________
(3)写出过氧化钠与水反应的化学方程式___________
(1)写出氢氧化钠与氯气反应的离子方程式
(2)写出氢氧化钙与氯气反应的化学方程式
(3)写出过氧化钠与水反应的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】将物质的用途选项填在表格下对应的位置。
用途:a.自来水消毒剂 b.呼吸面具中氧气的来源 c.红色油漆和涂料 d.生产硫酸
用途:a.自来水消毒剂 b.呼吸面具中氧气的来源 c.红色油漆和涂料 d.生产硫酸
| 物质 | 氧化铁 | 过氧化钠 | 二氧化氯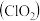 | 三氧化硫 |
| 用途 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】钠、氯及其化合物有如下转化关系,请按要求填空:
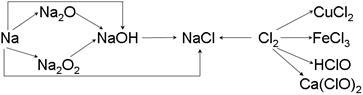
(1)金属钠的密度比水____________ ,实验室中金属钠通常保存在__________ 中。一小块金属钠投入水中的反应方程式是_____________________ 。
(2)Na2O2 是____________ 色的固体,Na2O2 的重要用途是________________ ,有关反应的化学方程式为_____________________ 。
(3)通常情况下,为了防止污染环境,在做完实验后,多余的氯气应用NaOH溶液吸收,其化学方程式为__________________ 。
(4)漂白粉的有效成分是________ (填化学式),漂白粉溶于水后,受空气中的CO2作用,产生有漂白、杀菌作用的次氯酸,化学方程式为_______________________ 。

(1)金属钠的密度比水
(2)Na2O2 是
(3)通常情况下,为了防止污染环境,在做完实验后,多余的氯气应用NaOH溶液吸收,其化学方程式为
(4)漂白粉的有效成分是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】a(g)镁和足量稀硫酸反应,镁完全反应后,测得氢气在常温时的体积为V(L),则常温下l mol氢气的体积为_________________ L。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】在标准状况下进行甲、乙、丙三组实验,三组实验均各取30mL同浓度的盐酸,加入同一种镁铝合金粉末,产生气体,有关数据见表:
(1)甲组实验中,盐酸_____ (填“过量”、“适量”或“不足量”),理由是_____ ;
(2)丙组实验中,盐酸_____ (填“过量”、“适量”或“不足量”),理由是_____ 。
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/m g | 255 | 385 | 459 |
| 生成气体体积/mL | 280 | 336 | 336 |
(1)甲组实验中,盐酸
(2)丙组实验中,盐酸
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】钛(Ti)因为具有神奇的性能越来越引起人们的关注。常温下,钛不和非金属、强酸反应;红热时,却可与常见的非金属单质反应。钛是航空、军工、电力等方面的必需原料。地壳中含钛矿石之一称金红石(TiO2)目前大规模生产钛的方法是:
第一步:金红石、碳粉混合,在高温条件下通入氯气制得TiCl4和一种可燃性气体。该反应的化学方程式是______ ,该反应的还原剂是______ 。
第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛。
(1)此反应的化学方程式是______ 。
(2)简述由上述所得产物中获取金属钛的步骤______ 。
第一步:金红石、碳粉混合,在高温条件下通入氯气制得TiCl4和一种可燃性气体。该反应的化学方程式是
第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛。
(1)此反应的化学方程式是
(2)简述由上述所得产物中获取金属钛的步骤
您最近一年使用:0次



