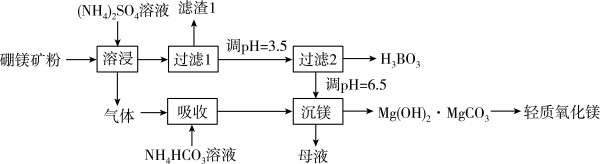
钛(Ti)因为具有神奇的性能越来越引起人们的关注。常温下,钛不和非金属、强酸反应;红热时,却可与常见的非金属单质反应。钛是航空、军工、电力等方面的必需原料。地壳中含钛矿石之一称金红石(TiO2)目前大规模生产钛的方法是:
第一步:金红石、碳粉混合,在高温条件下通入氯气制得TiCl4和一种可燃性气体。该反应的化学方程式是______ ,该反应的还原剂是______ 。
第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛。
(1)此反应的化学方程式是______ 。
(2)简述由上述所得产物中获取金属钛的步骤______ 。
第一步:金红石、碳粉混合,在高温条件下通入氯气制得TiCl4和一种可燃性气体。该反应的化学方程式是
第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛。
(1)此反应的化学方程式是
(2)简述由上述所得产物中获取金属钛的步骤
13-14高一·全国·课时练习 查看更多[2]
更新时间:2016-12-08 21:36:35
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】用分类思想研究一类物质的通性和特殊性是学习化学的一种重要方法。下图是依据一定的分类标准,对某些物质与水反应情况进行分类的分类图。已知: ;
;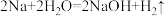 ;
; 。请根据你所学的知识,按要求填空:
。请根据你所学的知识,按要求填空:
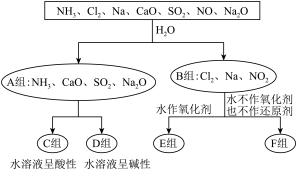
(1)上述第一级分类标准(分成A、B组的依据)是___________ 。
(2)F组物质中除了Cl2外还有___________ (填化学式,下同)。
(3)A组中属于电解质的是___________ 。
(4)已知Cl2可发生如下反应: 。
。
①该反应中氧化剂是___________ ,氧化产物是___________ 。
②用双线桥法标出电子转移的数目和方向:___________ 。
(5)氯化铵溶液常用于焊接。在焊接铜器时可用氯化铵除去铜器表面的氧化铜以便焊接,其反应如下:
___________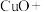 ___________
___________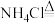 ___________
___________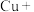 ___________
___________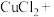 ___________
___________ ___________
___________
配平此氧化还原反应的化学方程式。___________
 ;
;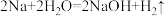 ;
; 。请根据你所学的知识,按要求填空:
。请根据你所学的知识,按要求填空:
(1)上述第一级分类标准(分成A、B组的依据)是
(2)F组物质中除了Cl2外还有
(3)A组中属于电解质的是
(4)已知Cl2可发生如下反应:
 。
。①该反应中氧化剂是
②用双线桥法标出电子转移的数目和方向:
(5)氯化铵溶液常用于焊接。在焊接铜器时可用氯化铵除去铜器表面的氧化铜以便焊接,其反应如下:
___________
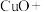 ___________
___________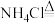 ___________
___________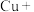 ___________
___________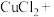 ___________
___________ ___________
___________
配平此氧化还原反应的化学方程式。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】现有以下物质:① 溶液,②液氮,③
溶液,②液氮,③ 固体,④熔融
固体,④熔融 ,⑤
,⑤ 胶体,⑥
胶体,⑥ ,⑦
,⑦ ,⑧
,⑧ 。
。
(1)以上物质中属于混合物的是___________ (填序号),以上物质中属于非电解质的是___________ (填序号),⑤和①的本质区别是___________ 。
(2)写出①和⑧的水溶液反应的离子方程式___________
(3)写出④的电离方程式___________
(4)在足量④的水溶液中加入少量③,发生反应的离子方程式为___________
(5)写出⑥与水反应的离子反应方程式为___________ ,此反应的氧化剂为___________ 。
 溶液,②液氮,③
溶液,②液氮,③ 固体,④熔融
固体,④熔融 ,⑤
,⑤ 胶体,⑥
胶体,⑥ ,⑦
,⑦ ,⑧
,⑧ 。
。(1)以上物质中属于混合物的是
(2)写出①和⑧的水溶液反应的离子方程式
(3)写出④的电离方程式
(4)在足量④的水溶液中加入少量③,发生反应的离子方程式为
(5)写出⑥与水反应的离子反应方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】按要求回答下列问题。
(1)磷酸钠(Na3PO4)在水溶液中的电离方程式为__ 。
(2)镁条在氮气中燃烧的化学方程式为___ 。
(3)过氧化钠与水反应的化学方程式为___ 。该反应中,氧化剂是___ ,还原剂是___ 。
(4)浓硫酸和碳在加热条件下反应的化学方程式为___ 。
(1)磷酸钠(Na3PO4)在水溶液中的电离方程式为
(2)镁条在氮气中燃烧的化学方程式为
(3)过氧化钠与水反应的化学方程式为
(4)浓硫酸和碳在加热条件下反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】方程式书写:
(1)镁条在二氧化碳中燃烧的反应:___________________________
(2)小块钠投入到水中的离子反应:___________________________
(1)镁条在二氧化碳中燃烧的反应:
(2)小块钠投入到水中的离子反应:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】聚合铝(PAC)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理。用铝灰、铝土矿、铝渣等为原料(主要成分为Al、Al2O3)可制取聚合铝。实验步骤如下:

(1)写出铝、氧化铝分别与盐酸反应的离子方程式:________________ ;________________ ;
(2)用36.5%的盐酸配制20%的盐酸,操作步骤是____________________ ;(依次写出),配制过程中所需的定量仪器是________________ ;
(3)聚合铝(PAC)的分子式为[Al2(OH)aClb]m,聚合铝中OH-与Al3+的比值对净水效果有很大影响,定义盐基度B=n(OH-)/3n(Al3+),当B=2/3时,b=________________ ;(填入合适数字).
(4)聚合过程主要利用了Al3+的性质是________________ ;
(5)要测定1mol聚合铝中a的值
①测定时所需的试剂是________________ (填代号);
(a) NaOH(b)AgNO3(c) pH试纸(d) HNO3
②需要直接测定的物理量是________________ (用文字表示);若该物理量的数值用β表示,试写出聚合铝中a值的表达式________________ ;
③测定过程中所需的基本操作是________________ (按操作先后顺序的代号列出,可重复选择),
(a) 洗涤(b) 过滤(c) 称量 (d) 干燥(e) 冷却。

(1)写出铝、氧化铝分别与盐酸反应的离子方程式:
(2)用36.5%的盐酸配制20%的盐酸,操作步骤是
(3)聚合铝(PAC)的分子式为[Al2(OH)aClb]m,聚合铝中OH-与Al3+的比值对净水效果有很大影响,定义盐基度B=n(OH-)/3n(Al3+),当B=2/3时,b=
(4)聚合过程主要利用了Al3+的性质是
(5)要测定1mol聚合铝中a的值
①测定时所需的试剂是
(a) NaOH(b)AgNO3(c) pH试纸(d) HNO3
②需要直接测定的物理量是
③测定过程中所需的基本操作是
(a) 洗涤(b) 过滤(c) 称量 (d) 干燥(e) 冷却。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】铝土矿(主要成分为Al2O3,还有少量杂质)是提取铝的原料。提取铝的工艺流程如下:
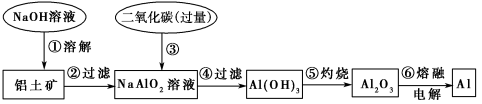
(1)请用离子方程式表示以上工艺流程中第①步反应:________________ 。
(2)写出以上工艺流程中第③步反应的离子方程式:________________ 。
(3)写出实验室制取Al(OH)3的离子方程式:________________ 。

(1)请用离子方程式表示以上工艺流程中第①步反应:
(2)写出以上工艺流程中第③步反应的离子方程式:
(3)写出实验室制取Al(OH)3的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】国家主席习近平在9月22日召开的联合国大会上表示:“中国将争取在2060年前实现碳中和”。
(1)CO2甲烷化反应是由法国化学家Paul Sabatier提出的,CO2催化氢化制甲烷的研究过程如下:
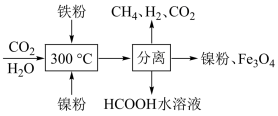
①上述过程中,加入铁粉的作用是____ 。
②HCOOH是CO2转化为CH4的中间体:CO2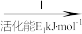 HCOOH
HCOOH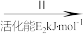 CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,原因是
CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,原因是____ 。
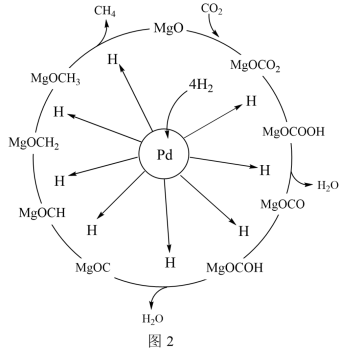
(2)一定条件下,Pd-Mg/SiO2催化剂可使CO2甲烷化从而变废为宝,其反应机理如图2所示,该反应的化学方程式为____ ,反应过程中碳元素的化合价为-2价的中间体是____ 。
(3)CO2一定条件可转化为CH3OH,CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH<0。
CH3OH(g)+H2O(g) ΔH<0。
①某温度下恒容密闭容器中,CO2和H2起始浓度分别为2mol/L和4mol/L,反应达平衡时,CO2转化率为50%,该温度下反应的平衡常数K=____ 。
②恒压下,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜时甲醇的产率随温度的变化如图3 所示,分子筛膜能选择性分离出H2O。P点甲醇产率高于T点的原因为____ 。

(1)CO2甲烷化反应是由法国化学家Paul Sabatier提出的,CO2催化氢化制甲烷的研究过程如下:

①上述过程中,加入铁粉的作用是
②HCOOH是CO2转化为CH4的中间体:CO2
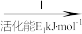 HCOOH
HCOOH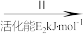 CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,原因是
CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,原因是(2)一定条件下,Pd-Mg/SiO2催化剂可使CO2甲烷化从而变废为宝,其反应机理如图2所示,该反应的化学方程式为

(3)CO2一定条件可转化为CH3OH,CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH<0。
CH3OH(g)+H2O(g) ΔH<0。①某温度下恒容密闭容器中,CO2和H2起始浓度分别为2mol/L和4mol/L,反应达平衡时,CO2转化率为50%,该温度下反应的平衡常数K=
②恒压下,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜时甲醇的产率随温度的变化如图3 所示,分子筛膜能选择性分离出H2O。P点甲醇产率高于T点的原因为

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】铁是一种重要的金属材料,它的单质及化合物在生产生活中应用广泛。
Ⅰ.
(1)生铁含有C、Si、Mn、S、P等元素,其中属于金属元素的除Fe外,还有_____ 元素。
(2)铁元素有三种常见的氧化物,分别是FeO、 、
、 。其中具有磁性的是
。其中具有磁性的是_____ ,可作红色颜料的是_____ 。
(3)某补铁口服液中含有 ,为检验其是否被氧化变质,可取少量该口服液,向其中滴加KSCN溶液,若溶液变为
,为检验其是否被氧化变质,可取少量该口服液,向其中滴加KSCN溶液,若溶液变为_____ 色,则说明其已变质。向该口服液中加入维生素C可防止其被氧化变质,此过程中利用了维生素C的_____ 性。
(4) 可作为铜电路板的腐蚀液,其反应原理为Cu与
可作为铜电路板的腐蚀液,其反应原理为Cu与 溶液反应生成
溶液反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为_____ 。向反应后的溶液中加入_____ ,可回收Cu,并得到 溶液。
溶液。
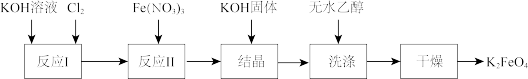
Ⅱ.高铁酸钾( )是一种新型、高效、多功能水处理剂。工业上制备高铁酸钾的流程如下图所示:
)是一种新型、高效、多功能水处理剂。工业上制备高铁酸钾的流程如下图所示:
(5)下列说法错误的是_____。
(6)用电解饱和食盐水获得原料氯气的过程中有2mol电子发生转移,试计算理论上最多可制得氯气的体积(标准状况)是_____ L。
Ⅰ.
(1)生铁含有C、Si、Mn、S、P等元素,其中属于金属元素的除Fe外,还有
(2)铁元素有三种常见的氧化物,分别是FeO、
 、
、 。其中具有磁性的是
。其中具有磁性的是(3)某补铁口服液中含有
 ,为检验其是否被氧化变质,可取少量该口服液,向其中滴加KSCN溶液,若溶液变为
,为检验其是否被氧化变质,可取少量该口服液,向其中滴加KSCN溶液,若溶液变为(4)
 可作为铜电路板的腐蚀液,其反应原理为Cu与
可作为铜电路板的腐蚀液,其反应原理为Cu与 溶液反应生成
溶液反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为 溶液。
溶液。Ⅱ.高铁酸钾(
 )是一种新型、高效、多功能水处理剂。工业上制备高铁酸钾的流程如下图所示:
)是一种新型、高效、多功能水处理剂。工业上制备高铁酸钾的流程如下图所示:
(5)下列说法错误的是_____。
A. 中铁元素的化合价为+6价 中铁元素的化合价为+6价 |
| B.用无水乙醇洗涤可以减少产品的损耗 |
C.反应Ⅱ中的氧化剂是 |
| D.高铁酸根离子具有强氧化性,能杀菌消毒 |
您最近一年使用:0次

 溶液可以除去铁锈,利用了
溶液可以除去铁锈,利用了
 ,转化为无污染的
,转化为无污染的 和NaCl,该反应的化学反应方程式为
和NaCl,该反应的化学反应方程式为