聚合铝(PAC)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理。用铝灰、铝土矿、铝渣等为原料(主要成分为Al、Al2O3)可制取聚合铝。实验步骤如下:

(1)写出铝、氧化铝分别与盐酸反应的离子方程式:________________ ;________________ ;
(2)用36.5%的盐酸配制20%的盐酸,操作步骤是____________________ ;(依次写出),配制过程中所需的定量仪器是________________ ;
(3)聚合铝(PAC)的分子式为[Al2(OH)aClb]m,聚合铝中OH-与Al3+的比值对净水效果有很大影响,定义盐基度B=n(OH-)/3n(Al3+),当B=2/3时,b=________________ ;(填入合适数字).
(4)聚合过程主要利用了Al3+的性质是________________ ;
(5)要测定1mol聚合铝中a的值
①测定时所需的试剂是________________ (填代号);
(a) NaOH(b)AgNO3(c) pH试纸(d) HNO3
②需要直接测定的物理量是________________ (用文字表示);若该物理量的数值用β表示,试写出聚合铝中a值的表达式________________ ;
③测定过程中所需的基本操作是________________ (按操作先后顺序的代号列出,可重复选择),
(a) 洗涤(b) 过滤(c) 称量 (d) 干燥(e) 冷却。

(1)写出铝、氧化铝分别与盐酸反应的离子方程式:
(2)用36.5%的盐酸配制20%的盐酸,操作步骤是
(3)聚合铝(PAC)的分子式为[Al2(OH)aClb]m,聚合铝中OH-与Al3+的比值对净水效果有很大影响,定义盐基度B=n(OH-)/3n(Al3+),当B=2/3时,b=
(4)聚合过程主要利用了Al3+的性质是
(5)要测定1mol聚合铝中a的值
①测定时所需的试剂是
(a) NaOH(b)AgNO3(c) pH试纸(d) HNO3
②需要直接测定的物理量是
③测定过程中所需的基本操作是
(a) 洗涤(b) 过滤(c) 称量 (d) 干燥(e) 冷却。
12-13高二上·上海松江·期末 查看更多[1]
(已下线)2011-2012学年上海市松江二中高二上学期期末考试化学试卷
更新时间:2012-02-23 22:36:41
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】化学物质丰富多彩,化学反应精彩纷呈,在生活和生产中应用广泛。
(1)盛放氢氧化钠的玻璃试剂瓶不用玻璃塞,请用化学方程式表示其中的原因:___ ;
(2)工业上制备粗硅的化学方程式为:___ ;
(3)可用氢氧化钠溶解铝土矿(主要成分Al2O3);其反应方程式为:___ ;
(4)铁锈(主要成分氧化铁)与稀盐酸反应___ ;
(5)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液呈中性___ 。
(1)盛放氢氧化钠的玻璃试剂瓶不用玻璃塞,请用化学方程式表示其中的原因:
(2)工业上制备粗硅的化学方程式为:
(3)可用氢氧化钠溶解铝土矿(主要成分Al2O3);其反应方程式为:
(4)铁锈(主要成分氧化铁)与稀盐酸反应
(5)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液呈中性
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】铝土矿(主要成分为Al2O3,还有少量杂质)是提取铝的原料。提取铝的工艺流程如下:
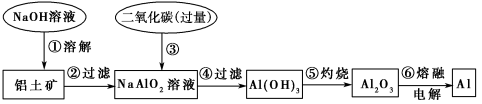
(1)请用离子方程式表示以上工艺流程中第①步反应:________________ 。
(2)写出以上工艺流程中第③步反应的离子方程式:________________ 。
(3)写出实验室制取Al(OH)3的离子方程式:________________ 。

(1)请用离子方程式表示以上工艺流程中第①步反应:
(2)写出以上工艺流程中第③步反应的离子方程式:
(3)写出实验室制取Al(OH)3的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】钛(Ti)因为具有神奇的性能越来越引起人们的关注。常温下,钛不和非金属、强酸反应;红热时,却可与常见的非金属单质反应。钛是航空、军工、电力等方面的必需原料。地壳中含钛矿石之一称金红石(TiO2)目前大规模生产钛的方法是:
第一步:金红石、碳粉混合,在高温条件下通入氯气制得TiCl4和一种可燃性气体。该反应的化学方程式是______ ,该反应的还原剂是______ 。
第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛。
(1)此反应的化学方程式是______ 。
(2)简述由上述所得产物中获取金属钛的步骤______ 。
第一步:金红石、碳粉混合,在高温条件下通入氯气制得TiCl4和一种可燃性气体。该反应的化学方程式是
第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛。
(1)此反应的化学方程式是
(2)简述由上述所得产物中获取金属钛的步骤
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】欲除去下表中固体物质中的杂质(括号内物质为杂质),请选择下面提供的试剂和操作,并将序号填在表内。
供选试剂:A.盐酸;B.烧碱溶液;C.水;D.不用其他试剂。
供选操作:①加热;②过滤;③蒸发结晶。
供选试剂:A.盐酸;B.烧碱溶液;C.水;D.不用其他试剂。
供选操作:①加热;②过滤;③蒸发结晶。
| 含杂质的物质 | 所加试剂 | 主要操作 |
| SiO2(CaCO3) | ||
| Fe2O3(Al2O3) | ||
| NaCl(SiO2) |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】某铝合金中含有元素铝、镁、铜、硅,为了测定该合金中铝的含量,设计了如下实验,请回答有关问题:
(1)称取样品ag(精确到0.1g),称量时通常使用的主要仪器的名称是_______ 。
(2)样品溶解于足量的稀盐酸,过滤并洗涤滤渣。滤渣为_______ ,溶解、过滤用到的玻璃仪器是_______ 。
(3)向滤液中加过量的氢氧化钠溶液,过滤并洗涤滤渣。有关的离子方程式是_______ 、_______ 、_______ 。
(4)向步骤(3)的滤液中通入足量的二氧化碳气体,过滤并洗涤滤渣。有关的离子方程式是_______ 、_______ 。
(5)将步骤(4)中所得的滤渣烘干并灼烧至恒重、冷却后称量,其质量为bg。有关反应的化学方程式是_______ 。原样品中铝的质量分数是_______ 。
(1)称取样品ag(精确到0.1g),称量时通常使用的主要仪器的名称是
(2)样品溶解于足量的稀盐酸,过滤并洗涤滤渣。滤渣为
(3)向滤液中加过量的氢氧化钠溶液,过滤并洗涤滤渣。有关的离子方程式是
(4)向步骤(3)的滤液中通入足量的二氧化碳气体,过滤并洗涤滤渣。有关的离子方程式是
(5)将步骤(4)中所得的滤渣烘干并灼烧至恒重、冷却后称量,其质量为bg。有关反应的化学方程式是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】粗盐中除含有不溶性的泥沙外,还含有可溶性的CaCl2、MgCl2、硫酸钠等,我们可以通过分离、提纯等方法制取纯净的氯化钠。

(1)怎样除去粗盐中不溶性的泥沙:__________ 。
(2)实验过程中为了将可溶性杂质除净,应该怎样操作?这样操作有什么弊端:__________ 。
(3)设计除去杂质的实验方案时,除了要考虑所加试剂的种类,还要考虑哪些问题:__________ 。
(4)在粗盐的提纯实验中,为何氯化钡溶液要在碳酸钠溶液之前加入:__________ ,加入碳酸钠溶液的目的是:__________ 。

(1)怎样除去粗盐中不溶性的泥沙:
(2)实验过程中为了将可溶性杂质除净,应该怎样操作?这样操作有什么弊端:
(3)设计除去杂质的实验方案时,除了要考虑所加试剂的种类,还要考虑哪些问题:
(4)在粗盐的提纯实验中,为何氯化钡溶液要在碳酸钠溶液之前加入:
您最近一年使用:0次



