名校
1 . 草酸钴在化学中应用广泛,可用于制备催化剂等。以钻矿[主要成分为 、
、 、
、 ,含少量的
,含少量的 、
、 、
、 、
、 、
、 等]为原料制取草酸钴晶体
等]为原料制取草酸钴晶体 的工艺流程如图所示。
的工艺流程如图所示。
(1) 位于元素周期表中第
位于元素周期表中第___________ 周期第___________ 族。
(2)浸出渣的主要成分是___________ (填化学式)。“浸取”时 发生反应的化学方程式为
发生反应的化学方程式为___________ 。
(3)“氧化”过程中消耗 的量明显偏高的原因是
的量明显偏高的原因是___________ (用化学方程式表示)。
(4)取“调节 ”后所得滤液,将
”后所得滤液,将 调至9.4,可得到
调至9.4,可得到 沉淀,在空气中
沉淀,在空气中 煅烧该沉淀得到
煅烧该沉淀得到 的化学方程式为
的化学方程式为___________ 。
(5)“提纯”分为萃取和反萃取两步进行。向除杂后的溶液中加入某有机酸萃取剂 发生反应
发生反应 当溶液
当溶液 处于一定范围内时,测得
处于一定范围内时,测得 萃取率随溶液
萃取率随溶液 的增大而增大,其原因是
的增大而增大,其原因是___________ 。反萃取时,应加入___________ 。
(6)取 草酸钴晶体,在空气中加热至恒重,得到
草酸钴晶体,在空气中加热至恒重,得到 和
和 的混合物
的混合物 ,则该混合物中
,则该混合物中 的质量为
的质量为___________  。
。
 、
、 、
、 ,含少量的
,含少量的 、
、 、
、 、
、 、
、 等]为原料制取草酸钴晶体
等]为原料制取草酸钴晶体 的工艺流程如图所示。
的工艺流程如图所示。
(1)
 位于元素周期表中第
位于元素周期表中第(2)浸出渣的主要成分是
 发生反应的化学方程式为
发生反应的化学方程式为(3)“氧化”过程中消耗
 的量明显偏高的原因是
的量明显偏高的原因是(4)取“调节
 ”后所得滤液,将
”后所得滤液,将 调至9.4,可得到
调至9.4,可得到 沉淀,在空气中
沉淀,在空气中 煅烧该沉淀得到
煅烧该沉淀得到 的化学方程式为
的化学方程式为(5)“提纯”分为萃取和反萃取两步进行。向除杂后的溶液中加入某有机酸萃取剂
 发生反应
发生反应 当溶液
当溶液 处于一定范围内时,测得
处于一定范围内时,测得 萃取率随溶液
萃取率随溶液 的增大而增大,其原因是
的增大而增大,其原因是(6)取
 草酸钴晶体,在空气中加热至恒重,得到
草酸钴晶体,在空气中加热至恒重,得到 和
和 的混合物
的混合物 ,则该混合物中
,则该混合物中 的质量为
的质量为 。
。
您最近一年使用:0次
2 . 以黄铁矿(主要成分 )为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。
)为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。
(1)由炉渣制备还原铁粉的化学方程式为_______ 。
(2)欲得到更纯的 ,反应①应通入
,反应①应通入_______ (填“过量”或“不足量”)的 气体。
气体。
(3)因为 具有
具有_______ 性(填“氧化”或“还原”),导致商品 中不可避免地存在
中不可避免地存在 。检验其中含有
。检验其中含有 的方法是
的方法是_______ 。
(4)一般用 滴定分析法测定还原铁粉纯度。实验步骤:称取一定量样品,用过量稀硫酸溶解,用标准
滴定分析法测定还原铁粉纯度。实验步骤:称取一定量样品,用过量稀硫酸溶解,用标准 溶液滴定其中的
溶液滴定其中的 。反应式:
。反应式: 某次实验称取0.2800g样品,滴定时消耗浓度为0.03000
某次实验称取0.2800g样品,滴定时消耗浓度为0.03000 的
的 溶液25.10mL,则样品中铁含量为
溶液25.10mL,则样品中铁含量为_______ %。
 )为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。
)为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。
(1)由炉渣制备还原铁粉的化学方程式为
(2)欲得到更纯的
 ,反应①应通入
,反应①应通入 气体。
气体。(3)因为
 具有
具有 中不可避免地存在
中不可避免地存在 。检验其中含有
。检验其中含有 的方法是
的方法是(4)一般用
 滴定分析法测定还原铁粉纯度。实验步骤:称取一定量样品,用过量稀硫酸溶解,用标准
滴定分析法测定还原铁粉纯度。实验步骤:称取一定量样品,用过量稀硫酸溶解,用标准 溶液滴定其中的
溶液滴定其中的 。反应式:
。反应式: 某次实验称取0.2800g样品,滴定时消耗浓度为0.03000
某次实验称取0.2800g样品,滴定时消耗浓度为0.03000 的
的 溶液25.10mL,则样品中铁含量为
溶液25.10mL,则样品中铁含量为
您最近一年使用:0次
名校
解题方法
3 . Li2CO3可用于制备锂电池的正极材料LiCoO2,以某锂云母矿石(主要成分为Li2O,还有Al2O3、Fe2O3、MnO、MgF2等杂质)制备Li2CO3。
已知:①有关沉淀数据如下表(“完全沉淀”时金属离子浓度≤1.0×10-5mol·L-1)。
②部分物质的溶解度曲线见下图。
(1)酸浸,向锂云母矿石中加入50%硫酸,加热至90℃,装置如图所示。烧杯中试剂的作用是___________ 。___________ 。分两次调节pH的主要原因是___________ 。
(3)沉锂,将已经除杂的溶液蒸发浓缩,向浓缩后的滤液中加入稍过量饱和Na2CO3溶液,加热煮沸,趁热过滤,将滤渣洗涤烘干,得Li2CO3固体。浓缩液中离子浓度过大将在产品中引入___________ 杂质(填化学式)。
(4)Li2CO3和Co3O4混合后,在空气中高温加热可以制备锂电池的正极材料LiCoO2,写出反应方程式:___________ 。
(5)CoC2O4·2H2O热分解可制备Co3O4。请补充完整由含c(Co2+)=0.1mol·L-1的浸出液(含有杂质Al3+、Fe3+、Fe2+)制备纯净的CoC2O4·2H2O实验方案:___________ ,干燥,得到CoC2O4·2H2O晶体。(须使用的试剂:NaClO3,NaOH,AgNO3溶液,(NH4)2C2O4,蒸馏水)
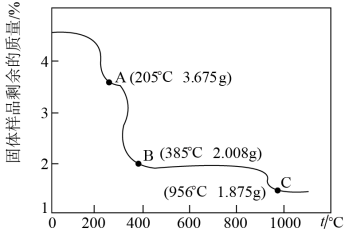
(6)为确定由CoC2O4·2H2O获得Co3O4的最佳煅烧温度,准确称取4.575g的CoC2O4·2H2O样品,在空气中加热,固体样品的剩余质量随温度的变化如图所示(已知385℃以上残留固体均为金属氧化物)经测定,205~385℃的煅烧过程中,产生的气体为CO2,计算AB段消耗O2在标准状况下的体积___________ 。(写出计算过程,结果保留2位有效数字)
已知:①有关沉淀数据如下表(“完全沉淀”时金属离子浓度≤1.0×10-5mol·L-1)。
| 沉淀 | Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Co(OH)2 | Mn(OH)2 | Mg(OH)2 |
| 恰好完全沉淀时pH | 5.2 | 8.8 | 3.2 | 9.4 | 9.8 | 11.1 |

(1)酸浸,向锂云母矿石中加入50%硫酸,加热至90℃,装置如图所示。烧杯中试剂的作用是

(3)沉锂,将已经除杂的溶液蒸发浓缩,向浓缩后的滤液中加入稍过量饱和Na2CO3溶液,加热煮沸,趁热过滤,将滤渣洗涤烘干,得Li2CO3固体。浓缩液中离子浓度过大将在产品中引入
(4)Li2CO3和Co3O4混合后,在空气中高温加热可以制备锂电池的正极材料LiCoO2,写出反应方程式:
(5)CoC2O4·2H2O热分解可制备Co3O4。请补充完整由含c(Co2+)=0.1mol·L-1的浸出液(含有杂质Al3+、Fe3+、Fe2+)制备纯净的CoC2O4·2H2O实验方案:
(6)为确定由CoC2O4·2H2O获得Co3O4的最佳煅烧温度,准确称取4.575g的CoC2O4·2H2O样品,在空气中加热,固体样品的剩余质量随温度的变化如图所示(已知385℃以上残留固体均为金属氧化物)经测定,205~385℃的煅烧过程中,产生的气体为CO2,计算AB段消耗O2在标准状况下的体积
您最近一年使用:0次
名校
解题方法
4 . 由废弃锌锰干电池中 制取
制取 晶体的实验原理与装置能达到实验目的的是
晶体的实验原理与装置能达到实验目的的是
 制取
制取 晶体的实验原理与装置能达到实验目的的是
晶体的实验原理与装置能达到实验目的的是
A.用装置甲实现 与 与 、 、 的分离 的分离 |
B.用装置乙灼烧 、KOH和 、KOH和 固体制取 固体制取 |
C.用装置丙通入 气体实现 气体实现 转化为 转化为 |
D.用装置丁蒸干 溶液获取 溶液获取 晶体 晶体 |
您最近一年使用:0次
5 . 锰是生产各种合金的重要元素。工业上以含锰矿石(主要成分为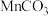 ,还含有铁钴、铜等的碳酸盐杂质)为原料生产金属锰的工艺流程如下:
,还含有铁钴、铜等的碳酸盐杂质)为原料生产金属锰的工艺流程如下:
回答下列问题:
(1)用硫酸浸取含锰矿石时,提高浸取速率的方法有_______ (写两种)。
(2)“氧化”步骤发生反应的离子方程式为_______ 。
(3)滤渣1的主要成分是___ ,实验室中为了加快固液混合物的分离,常采用的操作是___ 。
(4)当溶液中可溶组分浓度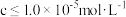 时,可认为已除尽。“除杂2”步骤需要控制溶液的pH至少为
时,可认为已除尽。“除杂2”步骤需要控制溶液的pH至少为____ (已知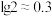 )。
)。
(5)“除杂3”步骤所得溶液中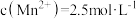 ,则其
,则其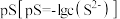 的范围是
的范围是____ 。
(6)电解废液中还含有少量 ,向其中加入饱和
,向其中加入饱和 溶液,有沉淀和气体生成,该反应的离子方程式为
溶液,有沉淀和气体生成,该反应的离子方程式为_______ 。
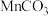 ,还含有铁钴、铜等的碳酸盐杂质)为原料生产金属锰的工艺流程如下:
,还含有铁钴、铜等的碳酸盐杂质)为原料生产金属锰的工艺流程如下: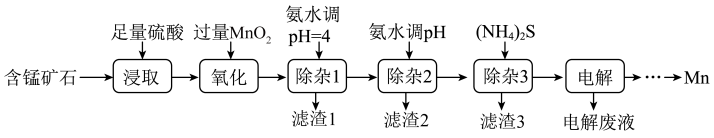
| 物质 |  |  |  | MnS | CoS |
 |  |  |  | 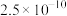 | 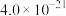 |
(1)用硫酸浸取含锰矿石时,提高浸取速率的方法有
(2)“氧化”步骤发生反应的离子方程式为
(3)滤渣1的主要成分是
(4)当溶液中可溶组分浓度
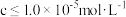 时,可认为已除尽。“除杂2”步骤需要控制溶液的pH至少为
时,可认为已除尽。“除杂2”步骤需要控制溶液的pH至少为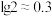 )。
)。(5)“除杂3”步骤所得溶液中
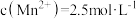 ,则其
,则其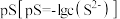 的范围是
的范围是(6)电解废液中还含有少量
 ,向其中加入饱和
,向其中加入饱和 溶液,有沉淀和气体生成,该反应的离子方程式为
溶液,有沉淀和气体生成,该反应的离子方程式为
您最近一年使用:0次
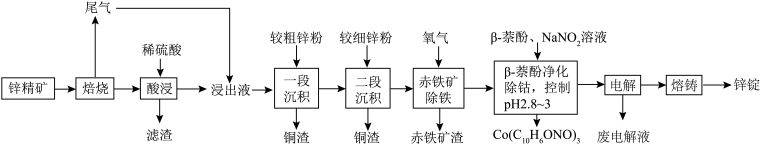
6 . 湿法炼锌具有能耗低,生成产品纯度高等特点,其主要原料为锌精矿(主要成分为硫化锌,还含有铁、钴、铜、镉、铅等元素的杂质),获得较纯锌锭的工艺流程如图:
(1)铜原子的价层电子排布图为_____ 。
(2)“酸浸”中滤渣主要成分为_____ 。
(3)“一段沉积”和“二段沉积”刚开始加入锌粉时,反应速率较小,然后反应速率显著增大,请解释产生此现象的原因:_____ 。
(4)“β—萘酚净化除钴”先是NaNO2把Co2+氧化成Co3+,并生成NO,Co3+与有机物发生化学反应生成红褐色稳定鳌合物沉淀。写出Co2+被氧化的离子方程式:_____ 。
(5)纯净的硫化锌是半导体锂离子电池负极材料。在充电过程中,发生合金化反应生成LiZn(合金相),同时负极材料晶胞的组成变化如图所示。_____ (x和y用具体数字表示)。
②若Li2S的晶胞参数为ann,则EF间的距离为_____ nm。
(1)铜原子的价层电子排布图为
(2)“酸浸”中滤渣主要成分为
(3)“一段沉积”和“二段沉积”刚开始加入锌粉时,反应速率较小,然后反应速率显著增大,请解释产生此现象的原因:
(4)“β—萘酚净化除钴”先是NaNO2把Co2+氧化成Co3+,并生成NO,Co3+与有机物发生化学反应生成红褐色稳定鳌合物沉淀。写出Co2+被氧化的离子方程式:
(5)纯净的硫化锌是半导体锂离子电池负极材料。在充电过程中,发生合金化反应生成LiZn(合金相),同时负极材料晶胞的组成变化如图所示。
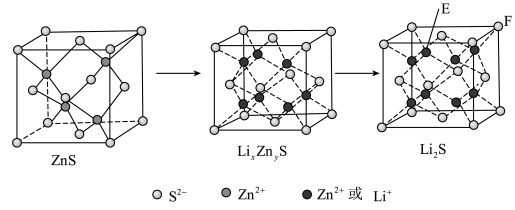
②若Li2S的晶胞参数为ann,则EF间的距离为
您最近一年使用:0次
7日内更新
|
84次组卷
|
2卷引用:黑龙江省大庆市实验中学实验二部2023-2024学年高三下学期得分训练化学试题(五)
7 . 2024年新春,万米载人潜水器“奋斗者”号全面升级,“中国深度”再次刷新。下列关于“奋斗者”号的说法中正确的是
| A.实验舱使用的导热石墨烯属于新型无机非金属材料 |
| B.载人舱壳所用新型钛合金材料中钛元素属于ⅣA族元素 |
| C.动力舱配置锂离子电池作为动力电池工作时,锂离子移向负极 |
D.浮力材料中的空心玻璃微球主要成分是 ,与金刚砂的组成相同 ,与金刚砂的组成相同 |
您最近一年使用:0次
8 . 锰可用于制造特种钢材,在汽车电池、高端装备制造、新材料等领域有广泛应用。二氧化锰广泛应用于电池、电子工业。以主要成分为 的某锰矿(杂质为
的某锰矿(杂质为 、
、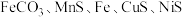 等)为原料制备单质锰的一种流程如图所示:
等)为原料制备单质锰的一种流程如图所示: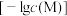 与溶液
与溶液 的关系如图所示:
的关系如图所示:
(1)滤液中的溶质为 、
、___________ (填化学式),“氧化除硫”过程中有红褐色固体生成,则 参与反应的化学方程式为
参与反应的化学方程式为___________ 。
(2)“酸浸氧化”过程 被氧化的离子方程式为
被氧化的离子方程式为___________ 。
(3)为何不通过调 的方法将
的方法将 除去:
除去: ___________ ;已知若溶液中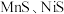 同时沉淀完全时,溶液中
同时沉淀完全时,溶液中 ,则相同温度下,
,则相同温度下,
___________ 。
(4)通过控制适当的反应条件,电解 溶液时,既可得到
溶液时,既可得到 也可得到
也可得到 ,则生成单质时,
,则生成单质时, 应在
应在___________ (填“阳极”或“阴极”)上放电;写出生成 时的电极反应式:
时的电极反应式:___________ 。
(5)已知单质锰的立方晶胞结构如图所示:___________ ;若锰原子半径为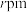 ,阿伏加德罗常数值为
,阿伏加德罗常数值为 ,则单质锰的密度为
,则单质锰的密度为___________  (用含
(用含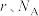 的代数式表示)。
的代数式表示)。
 的某锰矿(杂质为
的某锰矿(杂质为 、
、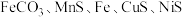 等)为原料制备单质锰的一种流程如图所示:
等)为原料制备单质锰的一种流程如图所示:
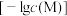 与溶液
与溶液 的关系如图所示:
的关系如图所示: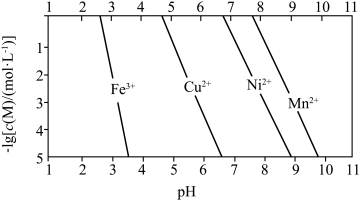
(1)滤液中的溶质为
 、
、 参与反应的化学方程式为
参与反应的化学方程式为(2)“酸浸氧化”过程
 被氧化的离子方程式为
被氧化的离子方程式为(3)为何不通过调
 的方法将
的方法将 除去:
除去: 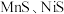 同时沉淀完全时,溶液中
同时沉淀完全时,溶液中 ,则相同温度下,
,则相同温度下,
(4)通过控制适当的反应条件,电解
 溶液时,既可得到
溶液时,既可得到 也可得到
也可得到 ,则生成单质时,
,则生成单质时, 应在
应在 时的电极反应式:
时的电极反应式:(5)已知单质锰的立方晶胞结构如图所示:

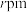 ,阿伏加德罗常数值为
,阿伏加德罗常数值为 ,则单质锰的密度为
,则单质锰的密度为 (用含
(用含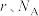 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解题方法
9 . 某地区原生钴矿,杂质主要含铁、硫、砷、碳等元素及石英。近年我国科技工作者提出一种用该矿石制备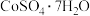 的新方法,该方法具有回收率高、污染小、成本低等优点。其工艺流程如下:
的新方法,该方法具有回收率高、污染小、成本低等优点。其工艺流程如下: 具有强氧化性,在水溶液中易转化为
具有强氧化性,在水溶液中易转化为 ;
;
②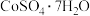 易溶于水,难溶于乙醇。
易溶于水,难溶于乙醇。
回答下列问题:
(1)“磨细”的目的是____________________ 。
(2)“焙烧”时加入石灰石,以防止产生的硫、砷氧化物气体污染环境。写出该过程中 与石灰石反应的化学方程式
与石灰石反应的化学方程式____________________ 。
(3)“酸浸”时,钴的浸出率受酸度、温度的影响,结合生产实际分析图1和图2,最佳条件是酸度为__________ %;温度为__________ ,原因是______________________________ 。 形式存在。
形式存在。 溶于盐酸的离子方程式
溶于盐酸的离子方程式____________________ 。
(5)“滤渣2”的化学式__________ ,
(6)“一系列操作”为蒸馏浓缩、冷却结晶、过滤、洗涤、干燥。选用酒精作洗涤剂的优点____________________ 。
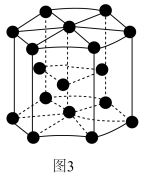
(7)钴的晶胞结构如图,该晶胞中原子个数为__________ 。
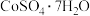 的新方法,该方法具有回收率高、污染小、成本低等优点。其工艺流程如下:
的新方法,该方法具有回收率高、污染小、成本低等优点。其工艺流程如下: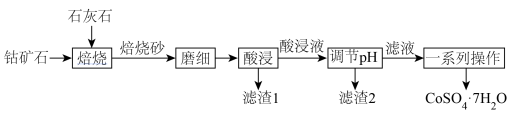
 具有强氧化性,在水溶液中易转化为
具有强氧化性,在水溶液中易转化为 ;
;②
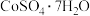 易溶于水,难溶于乙醇。
易溶于水,难溶于乙醇。回答下列问题:
(1)“磨细”的目的是
(2)“焙烧”时加入石灰石,以防止产生的硫、砷氧化物气体污染环境。写出该过程中
 与石灰石反应的化学方程式
与石灰石反应的化学方程式(3)“酸浸”时,钴的浸出率受酸度、温度的影响,结合生产实际分析图1和图2,最佳条件是酸度为

 形式存在。
形式存在。 溶于盐酸的离子方程式
溶于盐酸的离子方程式(5)“滤渣2”的化学式
(6)“一系列操作”为蒸馏浓缩、冷却结晶、过滤、洗涤、干燥。选用酒精作洗涤剂的优点
(7)钴的晶胞结构如图,该晶胞中原子个数为
您最近一年使用:0次
10 . 利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中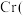 Ⅲ
Ⅲ 的处理工艺流程如下:
的处理工艺流程如下: ,其次是
,其次是 、
、 、
、 和
和 。
。
(1)酸浸时,为了提高浸取率可采取的措施有______ 、_______  答出两点
答出两点 。
。
(2) 的作用是将滤液 Ⅰ中的
的作用是将滤液 Ⅰ中的 转化为Cr2O
转化为Cr2O ,则此反应中氧化剂和还原剂物质的量之比为
,则此反应中氧化剂和还原剂物质的量之比为_____ 。
(3)常温下,部分阳离子以氢氧化物形式沉淀时溶液的 如下:
如下:
①用 调节溶液的
调节溶液的 不能超过
不能超过 ,其理由是
,其理由是_______ 。
②当 时,
时, 是否开始沉淀
是否开始沉淀 溶液中镁离子浓度不超过
溶液中镁离子浓度不超过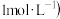 。
。____  填“是”或“否”
填“是”或“否”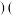 已知
已知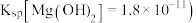 。并说明理由
。并说明理由_____ 。
(4)上述流程中,加入 溶液后,溶液呈碱性,
溶液后,溶液呈碱性, 转化为
转化为 ,写出上述流程中用
,写出上述流程中用 进行还原时发生反应的离子方程式:
进行还原时发生反应的离子方程式:________ 。
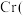 Ⅲ
Ⅲ 的处理工艺流程如下:
的处理工艺流程如下:
 ,其次是
,其次是 、
、 、
、 和
和 。
。(1)酸浸时,为了提高浸取率可采取的措施有
 答出两点
答出两点 。
。(2)
 的作用是将滤液 Ⅰ中的
的作用是将滤液 Ⅰ中的 转化为Cr2O
转化为Cr2O ,则此反应中氧化剂和还原剂物质的量之比为
,则此反应中氧化剂和还原剂物质的量之比为(3)常温下,部分阳离子以氢氧化物形式沉淀时溶液的
 如下:
如下:| 阳离子 |  |  |  |
开始沉淀时的 |  |  |  |
沉淀完全时的 | 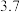 | 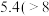 溶解 溶解 | 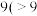 溶解 溶解 |
 调节溶液的
调节溶液的 不能超过
不能超过 ,其理由是
,其理由是②当
 时,
时, 是否开始沉淀
是否开始沉淀 溶液中镁离子浓度不超过
溶液中镁离子浓度不超过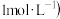 。
。 填“是”或“否”
填“是”或“否”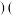 已知
已知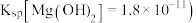 。并说明理由
。并说明理由(4)上述流程中,加入
 溶液后,溶液呈碱性,
溶液后,溶液呈碱性, 转化为
转化为 ,写出上述流程中用
,写出上述流程中用 进行还原时发生反应的离子方程式:
进行还原时发生反应的离子方程式:
您最近一年使用:0次
2024-05-16更新
|
162次组卷
|
2卷引用:江苏省无锡市江阴市三校联考2023-2024学年高二下学期4月期中联考化学试题



