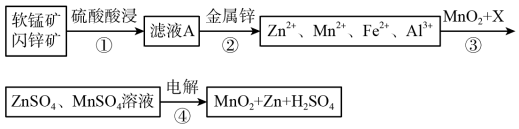
现有以下物质:① 溶液,②液氮,③
溶液,②液氮,③ 固体,④熔融
固体,④熔融 ,⑤
,⑤ 胶体,⑥
胶体,⑥ ,⑦
,⑦ ,⑧
,⑧ 。
。
(1)以上物质中属于混合物的是___________ (填序号),以上物质中属于非电解质的是___________ (填序号),⑤和①的本质区别是___________ 。
(2)写出①和⑧的水溶液反应的离子方程式___________
(3)写出④的电离方程式___________
(4)在足量④的水溶液中加入少量③,发生反应的离子方程式为___________
(5)写出⑥与水反应的离子反应方程式为___________ ,此反应的氧化剂为___________ 。
 溶液,②液氮,③
溶液,②液氮,③ 固体,④熔融
固体,④熔融 ,⑤
,⑤ 胶体,⑥
胶体,⑥ ,⑦
,⑦ ,⑧
,⑧ 。
。(1)以上物质中属于混合物的是
(2)写出①和⑧的水溶液反应的离子方程式
(3)写出④的电离方程式
(4)在足量④的水溶液中加入少量③,发生反应的离子方程式为
(5)写出⑥与水反应的离子反应方程式为
更新时间:2021-11-09 10:08:33
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】下列物质属于电解质的是______ ;能导电的是_____ ;属于弱电解质的是______ (均填写序号)。
①醋酸溶液②乙醇③胆矾④熔融氯化钠⑤二氧化硫⑥氨水⑦硫酸钡⑧蔗糖⑨氢氧化铁⑩浓盐酸
①醋酸溶液②乙醇③胆矾④熔融氯化钠⑤二氧化硫⑥氨水⑦硫酸钡⑧蔗糖⑨氢氧化铁⑩浓盐酸
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】从物质类别和元素化合价两个角度研究物质的性质,是一种行之有效的方法。某研究小组对下列物质展开研究:
①用饱和FeCl3溶液制得的胶体 ②乙醇 ③Al2O3 ④Na2CO3·10H2O ⑤FeCl3溶液 ⑥CO2 ⑦液氯 ⑧烧碱溶液 ⑨熔融的K2SO4 ⑩NaHSO4溶液 ⑪Fe
请回答:
(1)某同学采用分类的方法进行研究。他将①⑤⑧⑩归为一类,其分类依据为_______ ;此外,他还认为可将_______ (填物质编号)归为电解质。
(2)可证明③是两性氧化物的实验证据为_______ (用离子方程式表示)。
(3)NaHSO4虽属于盐类物质,但其溶液呈酸性,依据为______ (用电离方程式表示)。向⑩中滴加Ba(OH)2溶液至不再产生沉淀,反应的离子方程式为_______ ,检验反应后所得溶液中是否含有 的实验方法为
的实验方法为________ 。
(4)某同学欲探究 的氧化性,向⑤中加入足量
的氧化性,向⑤中加入足量________ (填物质编号)后过滤,随即向所得的滤液中加入足量 溶液,可观察到的现象为
溶液,可观察到的现象为________ 。
①用饱和FeCl3溶液制得的胶体 ②乙醇 ③Al2O3 ④Na2CO3·10H2O ⑤FeCl3溶液 ⑥CO2 ⑦液氯 ⑧烧碱溶液 ⑨熔融的K2SO4 ⑩NaHSO4溶液 ⑪Fe
请回答:
(1)某同学采用分类的方法进行研究。他将①⑤⑧⑩归为一类,其分类依据为
(2)可证明③是两性氧化物的实验证据为
(3)NaHSO4虽属于盐类物质,但其溶液呈酸性,依据为
 的实验方法为
的实验方法为(4)某同学欲探究
 的氧化性,向⑤中加入足量
的氧化性,向⑤中加入足量 溶液,可观察到的现象为
溶液,可观察到的现象为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】酒后驾车是马路上的第一大杀手。已知酒精(C2H5OH)能与K2Cr2O7和H2SO4的混合溶液在一定条件下发生如下反应:2K2Cr2O7+3C2H5OH+8H2SO4=2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O,且知Cr2O 和Cr3+在溶液中分别显橙色和绿色,回答下列问题:
和Cr3+在溶液中分别显橙色和绿色,回答下列问题:
(1)该反应___________ (填“是”或“不是”)离子反应。
(2)写出Cr2(SO4)3的电离方程式:___________ 。
(3)你认为能否用这一反应来检测司机是否酒后驾车?___________ (填“能”或“不能”),简述其原理___________ 。
 和Cr3+在溶液中分别显橙色和绿色,回答下列问题:
和Cr3+在溶液中分别显橙色和绿色,回答下列问题:(1)该反应
(2)写出Cr2(SO4)3的电离方程式:
(3)你认为能否用这一反应来检测司机是否酒后驾车?
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾、次氯酸等还强。工业上制取高铁酸钠的化学方程式是(未配平):
Fe(NO3)3+ NaOH + Cl2→ Na2FeO4+ NaNO3+ NaCl + H2O
(1)高铁酸钠中,铁元素的化合价是______ ;上述制取高铁酸钠的反应中,铁元素被________ (填“还原”或“氧化”)。
(2)高铁酸钠溶解于水,立即与水发生剧烈反应,放出氧气,正是这些在水中新产生出的氧原子发挥其极强的氧化能力给水杀菌消毒的。高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂原因铁元素转化为Fe(OH)3胶体,使水中悬浮物沉聚, Fe(OH)3胶体微粒直径的范围是__________ nm,高铁酸钠的电离方程式是____________________________ 。
Fe(NO3)3+ NaOH + Cl2→ Na2FeO4+ NaNO3+ NaCl + H2O
(1)高铁酸钠中,铁元素的化合价是
(2)高铁酸钠溶解于水,立即与水发生剧烈反应,放出氧气,正是这些在水中新产生出的氧原子发挥其极强的氧化能力给水杀菌消毒的。高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂原因铁元素转化为Fe(OH)3胶体,使水中悬浮物沉聚, Fe(OH)3胶体微粒直径的范围是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】请按要求完成下列方程式的书写。
(1) 在溶液中的电离方程式:
在溶液中的电离方程式:______ 。
(2)氧化镁与稀盐酸混合,反应的离子方程式:______ 。
(3) 与酸性
与酸性 溶液混合,反应的离子方程式:
溶液混合,反应的离子方程式:______ 。
(4)酸性条件下, 可发生反应生成
可发生反应生成 并释放出
并释放出 ,反应的离子方程式:
,反应的离子方程式:______ 。
(5)完成该反应的配平,并用单线桥标出电子转移的方向和数目:______ 。
______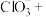 ______
______ ______=______
______=______ ______
______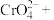 ______
______
(1)
 在溶液中的电离方程式:
在溶液中的电离方程式:(2)氧化镁与稀盐酸混合,反应的离子方程式:
(3)
 与酸性
与酸性 溶液混合,反应的离子方程式:
溶液混合,反应的离子方程式:(4)酸性条件下,
 可发生反应生成
可发生反应生成 并释放出
并释放出 ,反应的离子方程式:
,反应的离子方程式:(5)完成该反应的配平,并用单线桥标出电子转移的方向和数目:
______
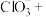 ______
______ ______=______
______=______ ______
______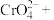 ______
______
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】有下列物质:①Ba(OH)2固体;②熔融的KHSO4;③HNO3;④稀硫酸;⑤CO2;⑥铜;⑦氨水;⑧蔗糖晶体;⑨FeCl3固体;⑩CH3COOH。请用序号填空
(1)上述状态下的物质可导电的是_______ (请用序号填空)。
(2)属于非电解质的是_______ (请用序号填空)。
(3)写出⑩的电离方程式_______ 。写出KHSO4水溶液中的电离方程式_______ 。
(4)写出少量的①的溶液与②的溶液反应的离子方程式_______ 。
(1)上述状态下的物质可导电的是
(2)属于非电解质的是
(3)写出⑩的电离方程式
(4)写出少量的①的溶液与②的溶液反应的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】有下列物质:①Na2CO3•10H2O晶体 ②铜 ③硫酸溶液 ④CO2 ⑤NaHSO4 固体
⑥Ba(OH)2 固体 ⑦蔗糖 ⑧氨水 ⑨稀硝酸 ⑩Al2(SO4)3 固体。
(1)上述物质属于电解质的有_____________ ,属于非电解质的有____________ ,能导电的物质有__________ (填编号)。
(2)上述物质中有两种物质之间可发生离子反应: H++OH-=H2O,写出该离子反应对应的化学方程式_____________________________________________ 。
(3)写出固体⑤溶解时的电离方程式____________________________________ 。
(4)当⑤与⑥1:1混合后,写出该离子方程式______________________________ 。
⑥Ba(OH)2 固体 ⑦蔗糖 ⑧氨水 ⑨稀硝酸 ⑩Al2(SO4)3 固体。
(1)上述物质属于电解质的有
(2)上述物质中有两种物质之间可发生离子反应: H++OH-=H2O,写出该离子反应对应的化学方程式
(3)写出固体⑤溶解时的电离方程式
(4)当⑤与⑥1:1混合后,写出该离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3-+4H++3e-= NO+2H2O
KMnO4、Na2CO3、FeO、Al(OH)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出该氧化还原反应的方程式(不需配平):_____________________________ ;
(2)反应中,氧化剂是_________ ,被氧化的元素是_____________ ;
(3)如反应转移了0.6mole-,则产生的气体在标准状况下体积为___ L。
KMnO4、Na2CO3、FeO、Al(OH)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出该氧化还原反应的方程式(不需配平):
(2)反应中,氧化剂是
(3)如反应转移了0.6mole-,则产生的气体在标准状况下体积为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】(1)难溶物PbSO4溶于CH3COONH4溶液可制得易溶于水的(CH3COO)2Pb,发生的反应为PbSO4+2CH3COONH4=(CH3COO)2Pb+(NH4)2SO4,说明(CH3COO)2Pb是________ (填“强”或“弱”)电解质。
(2)已知次磷酸(H3PO2)与足量的氢氧化钠溶液反应生成NaH2PO2和H2O,则次磷酸是_____ 元酸(填“一”、“二”或“三”)。
(3)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下面离子方程式,并用双线桥法标出电子转移方向及数目______ 。
____Fe(OH)3+____ClO-+____OH-=__FeO +___Cl-+______
+___Cl-+______
(4)在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,氧化剂是___________ ;当有2mol H3PO4生成,转移的电子数目为____ e-
(2)已知次磷酸(H3PO2)与足量的氢氧化钠溶液反应生成NaH2PO2和H2O,则次磷酸是
(3)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下面离子方程式,并用双线桥法标出电子转移方向及数目
____Fe(OH)3+____ClO-+____OH-=__FeO
 +___Cl-+______
+___Cl-+______(4)在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,氧化剂是
您最近一年使用:0次