用分类思想研究一类物质的通性和特殊性是学习化学的一种重要方法。下图是依据一定的分类标准,对某些物质与水反应情况进行分类的分类图。已知: ;
;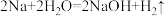 ;
; 。请根据你所学的知识,按要求填空:
。请根据你所学的知识,按要求填空:
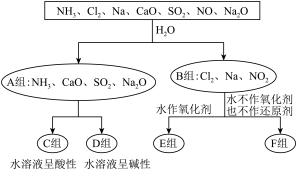
(1)上述第一级分类标准(分成A、B组的依据)是___________ 。
(2)F组物质中除了Cl2外还有___________ (填化学式,下同)。
(3)A组中属于电解质的是___________ 。
(4)已知Cl2可发生如下反应: 。
。
①该反应中氧化剂是___________ ,氧化产物是___________ 。
②用双线桥法标出电子转移的数目和方向:___________ 。
(5)氯化铵溶液常用于焊接。在焊接铜器时可用氯化铵除去铜器表面的氧化铜以便焊接,其反应如下:
___________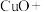 ___________
___________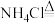 ___________
___________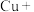 ___________
___________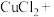 ___________
___________ ___________
___________
配平此氧化还原反应的化学方程式。___________
 ;
;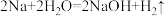 ;
; 。请根据你所学的知识,按要求填空:
。请根据你所学的知识,按要求填空:
(1)上述第一级分类标准(分成A、B组的依据)是
(2)F组物质中除了Cl2外还有
(3)A组中属于电解质的是
(4)已知Cl2可发生如下反应:
 。
。①该反应中氧化剂是
②用双线桥法标出电子转移的数目和方向:
(5)氯化铵溶液常用于焊接。在焊接铜器时可用氯化铵除去铜器表面的氧化铜以便焊接,其反应如下:
___________
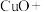 ___________
___________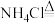 ___________
___________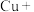 ___________
___________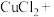 ___________
___________ ___________
___________
配平此氧化还原反应的化学方程式。
更新时间:2023-11-10 11:33:37
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】现有下列物质:①K2SO4晶体;②液态SO3;③硫酸溶液;④铜;⑤小苏打;⑥蔗糖;⑦乙醇;⑧熔融的氯化钠;⑨NaOH溶液;⑩干冰;其中:属于氧化物的是___________ (填序号,下同);属于盐的是___________ ;能导电的是___________ (填序号,下同);属于电解质的是___________ ;属于非电解质的是___________ ;
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】现有10种物质:①Cu②稀硫酸③HCl④NH3⑤空气⑥CO2⑦Hg⑧NaCl⑨CaCO3⑩Cl2,按照表中提示的信息,把符合左栏条件的物质的序号填入右栏相应的位置。
| 序号 | 符合的条件 | 物质的序号 |
| (1) | 混合物 | |
| (2) | 电解质,但难溶于水 | |
| (3) | 非电解质 | |
| (4) | 既不是电解质,也不是非电解质,但本身能导电 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】回答下列问题:
(一)下列物质中:①铜,②稀硫酸,③氯化氢,④氨气,⑤空气,⑥二氧化碳,⑦金属汞(俗称水银),⑧氯化钾,⑨碳酸钙,⑩液氯。
(1)属于混合物的是___________ (填序号)。
(2)属于电解质的是___________ (填序号)。
(3)能导电的是___________ (填序号)。
(二)写出下列物质在水溶液中的电离方程式:
(4)Ba(OH)2:___________ ;
(5)NaHCO3:___________ 。
(三)
(6)由以下一些微粒: 、
、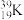 、
、 、
、 、
、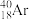 。其中互为同位素的是
。其中互为同位素的是_______ 。
(7)某元素的核素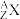 ,1.11g该核素的氯化物XCl2配成的溶液需用20mL1mol·L-1的AgNO3溶液才能把Cl-完全沉淀下来,已知此核素中质子数与中子数相等,则:
,1.11g该核素的氯化物XCl2配成的溶液需用20mL1mol·L-1的AgNO3溶液才能把Cl-完全沉淀下来,已知此核素中质子数与中子数相等,则:
①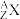 的质量数A是
的质量数A是___________ 。
②22.2gXCl2中所含Cl-的物质的量为___________ 。
(一)下列物质中:①铜,②稀硫酸,③氯化氢,④氨气,⑤空气,⑥二氧化碳,⑦金属汞(俗称水银),⑧氯化钾,⑨碳酸钙,⑩液氯。
(1)属于混合物的是
(2)属于电解质的是
(3)能导电的是
(二)写出下列物质在水溶液中的电离方程式:
(4)Ba(OH)2:
(5)NaHCO3:
(三)
(6)由以下一些微粒:
 、
、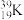 、
、 、
、 、
、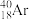 。其中互为同位素的是
。其中互为同位素的是(7)某元素的核素
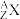 ,1.11g该核素的氯化物XCl2配成的溶液需用20mL1mol·L-1的AgNO3溶液才能把Cl-完全沉淀下来,已知此核素中质子数与中子数相等,则:
,1.11g该核素的氯化物XCl2配成的溶液需用20mL1mol·L-1的AgNO3溶液才能把Cl-完全沉淀下来,已知此核素中质子数与中子数相等,则:①
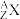 的质量数A是
的质量数A是②22.2gXCl2中所含Cl-的物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】“化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。根据所学知识,回答下列问题:
(1)沾有水的铁锅在高温火焰上灼烧会发黑,该反应的化学方程式为___________ 。
(2)食用加碘食盐能消除碘缺乏病的困扰,碘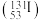 的质量数是
的质量数是___________ 。
(3)臭氧、“84”消毒液、二氧化氯、高铁酸钠等都是生活中常见的消毒剂。
①臭氧和氧气互为___________ (填“同位素”或“同素异形体”)。
②生活中“84”消毒液和洁厕灵(主要成分是稀盐酸)不能混合使用,原因是___________ 。
③ 是一种新型含氯消毒剂,在自来水消毒领域已经开始使用。实验室可通过反应
是一种新型含氯消毒剂,在自来水消毒领域已经开始使用。实验室可通过反应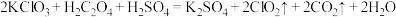 制得
制得 。该反应中产生
。该反应中产生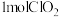 时,转移的电子的物质的量为
时,转移的电子的物质的量为___________ 。
④高铁酸钠 还是一种新型的净水剂。其净水过程中所发生的化学反应主要为
还是一种新型的净水剂。其净水过程中所发生的化学反应主要为 (胶体)
(胶体)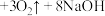 ,证明有
,证明有 胶体生成的实验操作为
胶体生成的实验操作为___________ 。
(4)汽车安全气囊弹出时发生反应: ,该反应中被氧化的N与被还原的N的物质的量之比为
,该反应中被氧化的N与被还原的N的物质的量之比为___________ 。
(5)铝制器具不宜盛放碱性食物,请写出铝与 溶液反应的离子方程式:
溶液反应的离子方程式:___________ 。
(1)沾有水的铁锅在高温火焰上灼烧会发黑,该反应的化学方程式为
(2)食用加碘食盐能消除碘缺乏病的困扰,碘
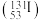 的质量数是
的质量数是(3)臭氧、“84”消毒液、二氧化氯、高铁酸钠等都是生活中常见的消毒剂。
①臭氧和氧气互为
②生活中“84”消毒液和洁厕灵(主要成分是稀盐酸)不能混合使用,原因是
③
 是一种新型含氯消毒剂,在自来水消毒领域已经开始使用。实验室可通过反应
是一种新型含氯消毒剂,在自来水消毒领域已经开始使用。实验室可通过反应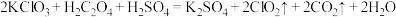 制得
制得 。该反应中产生
。该反应中产生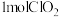 时,转移的电子的物质的量为
时,转移的电子的物质的量为④高铁酸钠
 还是一种新型的净水剂。其净水过程中所发生的化学反应主要为
还是一种新型的净水剂。其净水过程中所发生的化学反应主要为 (胶体)
(胶体)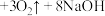 ,证明有
,证明有 胶体生成的实验操作为
胶体生成的实验操作为(4)汽车安全气囊弹出时发生反应:
 ,该反应中被氧化的N与被还原的N的物质的量之比为
,该反应中被氧化的N与被还原的N的物质的量之比为(5)铝制器具不宜盛放碱性食物,请写出铝与
 溶液反应的离子方程式:
溶液反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:
2KNO3+3C+S=K2S+N2↑+3CO2↑。其中被还原的元素是_______ ,被氧化的元素是_______ ,氧化剂是_______ ,用双线桥表示出电子转移的方向和数目_______ 。(在方程式中直接标出)
2KNO3+3C+S=K2S+N2↑+3CO2↑。其中被还原的元素是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】硫酸是一种重要的工业原料,可用于制造肥料、药物、洗涤剂、蓄电池等。工业上生产硫酸常以硫磺或黄铁矿为原料,制备硫酸的尾气中含有硫的氧化物等。
(1)除去试管壁上沾有的硫磺,可用的化学试剂是___________ (填名称)。
(2)二氧化硫可以用氯化铁溶液吸收,生成氯化亚铁和两种强酸,该反应的离子方程式为___________ 。
(3)二氧化硫与硝酸钠溶液的反应为3SO2+2NaNO3+2H2O=Na2SO4+2NO+2H2SO4。
①该反应体现SO2的性质是___________ 。
②SO2经催化氧化可转化为SO3,该转化的化学方程式是___________ 。
(4)黄铁矿主要成分是FeS2,写出用黄铁矿制备硫酸的第一步反应的化学方程式:_______ 。
(1)除去试管壁上沾有的硫磺,可用的化学试剂是
(2)二氧化硫可以用氯化铁溶液吸收,生成氯化亚铁和两种强酸,该反应的离子方程式为
(3)二氧化硫与硝酸钠溶液的反应为3SO2+2NaNO3+2H2O=Na2SO4+2NO+2H2SO4。
①该反应体现SO2的性质是
②SO2经催化氧化可转化为SO3,该转化的化学方程式是
(4)黄铁矿主要成分是FeS2,写出用黄铁矿制备硫酸的第一步反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】有四种物质:①铝②稀硫酸③碳酸氢钠④氢氧化钠
(1)属于盐的物质是______ (填序号,下同)。
(2)溶液显碱性的是_______ 。
(3)分析①与②反应,i表示的内容为__________ 。
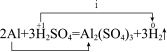
a.得到e-×6,化合价升高,被还原
b.得到e-×6,化合价降低,被还原
c.失去e-×6,化合价升高,被氧化
(4)①与④发生反应的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,还原剂是______ 。
(5)写出③与④反应的离子方程式________ 。
(1)属于盐的物质是
(2)溶液显碱性的是
(3)分析①与②反应,i表示的内容为
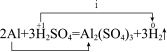
a.得到e-×6,化合价升高,被还原
b.得到e-×6,化合价降低,被还原
c.失去e-×6,化合价升高,被氧化
(4)①与④发生反应的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,还原剂是
(5)写出③与④反应的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】Ⅰ、已知乙醇( )能与
)能与 和
和 的混合溶液在一定条件下发生反应:
的混合溶液在一定条件下发生反应: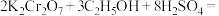
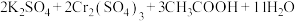 。
。 和
和 在溶液中分别显橙色和绿色,回答下列问题:
在溶液中分别显橙色和绿色,回答下列问题:
(1)写出 的电离方程式
的电离方程式___________ 。
(2)你认为能否用这一反应来检测司机是否酒后驾车___________ (填“能”或“不能”),简述其原理___________ 。
Ⅱ、某一反应体系有反应物和生成物共五种物质: 、
、 、
、 、
、 、
、 。已知该反应中
。已知该反应中 只发生如下过程:
只发生如下过程: 。
。
(3)该反应中的还原剂是___________ 。
(4)该反应中,发生还原反应的过程是___________ →___________ 。
(5)写出该反应的化学方程式,用双线桥标出电子转移的方向和数目___________ 。
 )能与
)能与 和
和 的混合溶液在一定条件下发生反应:
的混合溶液在一定条件下发生反应: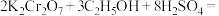
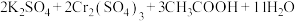 。
。 和
和 在溶液中分别显橙色和绿色,回答下列问题:
在溶液中分别显橙色和绿色,回答下列问题:(1)写出
 的电离方程式
的电离方程式(2)你认为能否用这一反应来检测司机是否酒后驾车
Ⅱ、某一反应体系有反应物和生成物共五种物质:
 、
、 、
、 、
、 、
、 。已知该反应中
。已知该反应中 只发生如下过程:
只发生如下过程: 。
。(3)该反应中的还原剂是
(4)该反应中,发生还原反应的过程是
(5)写出该反应的化学方程式,用双线桥标出电子转移的方向和数目
您最近一年使用:0次
【推荐1】已知某一反应体系有反应物和生成物共三种物质:FeCl3、FeCl2、Fe。完成下列问题:
(1)该反应中的还原产物的化学式是________ ,氧化产物的化学式是________ 。
(2)该反应的离子方程式为____________________________________________ 。
(3)标出该反应中电子转移的方向和数目________________________________ 。
(4)如反应转移了0.3 mol电子,则________ (填“溶解”或“生成”)的铁的质量为________ 。
(1)该反应中的还原产物的化学式是
(2)该反应的离子方程式为
(3)标出该反应中电子转移的方向和数目
(4)如反应转移了0.3 mol电子,则
您最近一年使用:0次
【推荐2】高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用化学方程式表示为:3NaClO + 2Fe(OH)3 + 4NaOH = 2Na2FeO4 + 3NaCl + 5H2O
(1)请用双线桥表示该氧化还原反应中电子转移的方向和数目_______ ;
(2)该反应中氧化剂是_______ ;氧化产物是_______ ;
(3)反应中当有3mol电子转移时,生成高铁酸钠的质量为_______ g;
(4)将高铁酸钠溶液滴入稀硫酸中,会放出O2,并生成Na2SO4和Fe2(SO4)3,请写出并配平化学方程式_______ 。
(1)请用双线桥表示该氧化还原反应中电子转移的方向和数目
(2)该反应中氧化剂是
(3)反应中当有3mol电子转移时,生成高铁酸钠的质量为
(4)将高铁酸钠溶液滴入稀硫酸中,会放出O2,并生成Na2SO4和Fe2(SO4)3,请写出并配平化学方程式
您最近一年使用:0次
【推荐3】请配平以下化学方程式,并回答下列问题:
(1)配平氧化还原反应方程式:_____________ 。
_____KClO3+_____HCl=______Cl2↑+_____KCl+_______H2O
(2)发生氧化反应的物质是___________ ,被还原的元素是___________ 。
(3)反应中1mol氧化剂___________ (填“得到”或“失去”)___________ mol电子。
(4)氧化产物与还原产物的物质的量之比为___________ 。
(1)配平氧化还原反应方程式:
_____KClO3+_____HCl=______Cl2↑+_____KCl+_______H2O
(2)发生氧化反应的物质是
(3)反应中1mol氧化剂
(4)氧化产物与还原产物的物质的量之比为
您最近一年使用:0次



