(1)有①分液漏斗②量筒③容量瓶,使用前需检查是否漏液的是___ (填序号)
(2)___ molH2O中含有的氧原子数与1.5molCO2中含有的氧原子数相等。
(3)标准状况下的四种气体:①6.72LCH4②3.01×1023个HCl分子③13.6gH2S④0.2molNH3,密度最大的是___ (填序号)
(4)10mL的CaCl2溶液里含2gCa2+,从中取出一半的溶液中Cl-的物质的量浓度是___ 。
(5)在Na2SO4和K2SO4的混合溶液中c(Na+)=0.2mol/L,c(SO42-)= amol/L,c(K+)=bmol/L时,a和b的关系是___ 。
(6)某物质A加热时按化学方程式2A=2B+C+3D分解,产物均为气体,测得由生成物组成的混合气体对H2的相对密度为20,则反应物A的摩尔质量为___ 。
(7)下列物质中:①铜 ②碳酸钙 ③氨气 ④氯气 ⑤空气 ⑥二氧化碳 ⑦氯化钠晶体 ⑧熔融硫酸钠。
属于电解质的是___ , 非电解质的是___ 。
(2)
(3)标准状况下的四种气体:①6.72LCH4②3.01×1023个HCl分子③13.6gH2S④0.2molNH3,密度最大的是
(4)10mL的CaCl2溶液里含2gCa2+,从中取出一半的溶液中Cl-的物质的量浓度是
(5)在Na2SO4和K2SO4的混合溶液中c(Na+)=0.2mol/L,c(SO42-)= amol/L,c(K+)=bmol/L时,a和b的关系是
(6)某物质A加热时按化学方程式2A=2B+C+3D分解,产物均为气体,测得由生成物组成的混合气体对H2的相对密度为20,则反应物A的摩尔质量为
(7)下列物质中:①铜 ②碳酸钙 ③氨气 ④氯气 ⑤空气 ⑥二氧化碳 ⑦氯化钠晶体 ⑧熔融硫酸钠。
属于电解质的是
更新时间:2020-01-09 17:15:47
|
【知识点】 物质的量有关计算
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】称取58.7克Ba(OH)2和BaCl2固体混合物,配成500mL溶液,把该溶液分成5等份后分别加入相同浓度不同体积的NaHCO3溶液,生成沉淀的质量如下表。已知加入NaHCO3溶液体积为80.0mL时,反应后溶液呈中性。
(1)NaHCO3溶液中溶质的物质的量浓度______________________ 。
(2)原固体混合物中Ba(OH)2和BaCl2的物质的量之比__________________________ 。
| 实验序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ |
| NaHCO3溶液(mL) | 20.0 | 40.0 | 60.0 | 80.0 | 100.0 |
| 沉淀的质量(g) | 1.97 | 3.94 | 5.91 | 7.88 | 7.88 |
(1)NaHCO3溶液中溶质的物质的量浓度
(2)原固体混合物中Ba(OH)2和BaCl2的物质的量之比
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐2】在标准状况下,0.5 mol的HCl占有的体积是_______ ,33.6L的H2的物质的量为________ ,16g O2的体积是________ 。
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐3】根据要求,回答下列问题:
(1)0.2 L0.5 mol/LFeCl3溶液中的Cl-的物质的量浓度为_____ 。
(2)同质量的 和
和 中所含
中所含 原子个数比为
原子个数比为_____ 。
(3)现有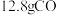 和
和 的混合气体,在标准状况下所占的体积约为
的混合气体,在标准状况下所占的体积约为 。
。
Ⅰ.该混合气体的平均摩尔质量为_____ 。
Ⅱ.混合气体中碳原子的个数为_____ (用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
Ⅲ.将混合气体依次通过如图装置,最后收集在气球中。
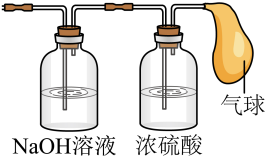
①气球中收集到的气体的质量为_____ ;
②气球中收集到的气体在标准状况下的体积为_____ ;
③气球中收集到的气体的电子总数为_____ (用NA表示阿伏加德罗常数的值)。
(1)0.2 L0.5 mol/LFeCl3溶液中的Cl-的物质的量浓度为
(2)同质量的
 和
和 中所含
中所含 原子个数比为
原子个数比为(3)现有
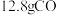 和
和 的混合气体,在标准状况下所占的体积约为
的混合气体,在标准状况下所占的体积约为 。
。Ⅰ.该混合气体的平均摩尔质量为
Ⅱ.混合气体中碳原子的个数为
 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。Ⅲ.将混合气体依次通过如图装置,最后收集在气球中。

①气球中收集到的气体的质量为
②气球中收集到的气体在标准状况下的体积为
③气球中收集到的气体的电子总数为
您最近半年使用:0次



