某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol/L 的溶液。在FeCl2溶液中需加入少量铁屑,其目的是_____ 。
(2)甲组同学取2mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的化学方程式为_______________ 。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,你认为上述方案应如何改进______ 。
(4)现向一支装有FeCl2溶液的试管中滴加氢氧化钠溶液,可观察到的现象是白色沉淀迅速转变成灰绿色,最后变成红褐色。其中涉及的氧化还原反应方程式为__________ 。
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol/L 的溶液。在FeCl2溶液中需加入少量铁屑,其目的是
(2)甲组同学取2mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的化学方程式为
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,你认为上述方案应如何改进
(4)现向一支装有FeCl2溶液的试管中滴加氢氧化钠溶液,可观察到的现象是白色沉淀迅速转变成灰绿色,最后变成红褐色。其中涉及的氧化还原反应方程式为
19-20高一上·江西南昌·期末 查看更多[2]
更新时间:2020-01-16 01:44:08
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】酒后驾车是马路第一杀手。已知酒精(C2H5OH)能与K2Cr2O7和H2SO4的混合溶液在一定条件下发生反应: 2K2Cr2O7+ 3C2H5OH+ 8H2SO4=2K2SO4+ 2Cr2(SO4)3+ 3CH3COOH+ 11H2O, 且知 和Cr3+在溶液中分别显橙色和绿色。回答下列问题:
和Cr3+在溶液中分别显橙色和绿色。回答下列问题:
(1)该反应__________________ (填 “是”或“不是”)离子反应。.
(2)将上述化学方程式改写成离子方程式__________ 。
(3)该反应________________ (填“是”或“不是”)氧化还原反应,判断的依据是______________ 。
(4)能否用这一反应来检测司机是否酒后驾车________ (填“能” 或“否”),理由是_______________________ 。
 和Cr3+在溶液中分别显橙色和绿色。回答下列问题:
和Cr3+在溶液中分别显橙色和绿色。回答下列问题:(1)该反应
(2)将上述化学方程式改写成离子方程式
(3)该反应
(4)能否用这一反应来检测司机是否酒后驾车
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】无机化合物按照组成和性质可进行如下分类。其中②、③、⑥均由Na、K、H、N、O、S中的三种元素组成。
(1)图中 可以代表的物质类别
可以代表的物质类别_____________________ ;
(2)③水溶液呈碱性,写出电离方程式_______________________________ ;(写一种即可)
(3)②与④在水溶液中发生反应的离子方程式_________________________ ;(无沉淀生成)
(4)④与少量的⑦在水溶液中发生反应的离子方程式_______________________________________ ;
(5)④与⑥在水溶液中发生反应的离子方程式_______________________________________ 。
| 强酸 | 强碱 | 可溶性盐 |  |
| ①HCl | ③ | ⑤Na2CO3 | ⑦CO2 |
| ② | ④Ba(OH)2 | ⑥ | ⑧SO3 |
(1)图中
 可以代表的物质类别
可以代表的物质类别(2)③水溶液呈碱性,写出电离方程式
(3)②与④在水溶液中发生反应的离子方程式
(4)④与少量的⑦在水溶液中发生反应的离子方程式
(5)④与⑥在水溶液中发生反应的离子方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)以下为中学化学中常见的几种物质:
①氯化钠晶体②干冰③HCl气体④铜⑤硫酸钡晶体⑥酒精⑦熔融的硝酸钾
能导电的是_______ ;(填序号,下同)属于电解质的是_______ ;属于非电解质的是__________ ;属于氧化物的是:________ 。
(2)按要求写出方程式:
①Fe2(SO4)3电离方程式________________________________ 。
②硫酸氢钠在水溶液中的电离方程式______________________ 。
(3)如图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是________ (填字母)。

①氯化钠晶体②干冰③HCl气体④铜⑤硫酸钡晶体⑥酒精⑦熔融的硝酸钾
能导电的是
(2)按要求写出方程式:
①Fe2(SO4)3电离方程式
②硫酸氢钠在水溶液中的电离方程式
(3)如图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】已知A和B两支试管的溶液中共含有K+、Ag+、Mg2+、Cl﹣、OH﹣、NO3﹣六种离子,向试管A的溶液中滴入酚酞试液呈红色.请回答下列问题:
(1)试管A的溶液中所含上述离子共有____ 种.
(2)若向某试管中滴入稀盐酸产生沉淀,则该试管为_____ (填“A”或“B”).
(3)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是_____ (填化学式).
(4)若向由试管A的溶液中阳离子组成的硫酸氢盐溶液中,滴入 Ba(OH)2溶液至溶液显中性,则发生反应的离子方程式为___________________________ .
(1)试管A的溶液中所含上述离子共有
(2)若向某试管中滴入稀盐酸产生沉淀,则该试管为
(3)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是
(4)若向由试管A的溶液中阳离子组成的硫酸氢盐溶液中,滴入 Ba(OH)2溶液至溶液显中性,则发生反应的离子方程式为
您最近半年使用:0次
【推荐2】(1)难溶物PbSO4溶于CH3COONH4溶液可制得易溶于水的(CH3COO)2Pb,发生的反应为PbSO4+2CH3COONH4=(CH3COO)2Pb+(NH4)2SO4,说明(CH3COO)2Pb是________ (填“强”或“弱”)电解质。
(2)已知次磷酸(H3PO2)与足量的氢氧化钠溶液反应生成NaH2PO2和H2O,则次磷酸是_____ 元酸(填“一”、“二”或“三”)。
(3)一个完整的氧化还原反应方程式可以拆开写成两个“半反应式”,一个是“氧化反应”式,一个是“还原反应”式。如2Fe3++Cu=2Fe2++Cu2+的拆写结果是:氧化反应为:Cu-2e−=Cu2+;还原反应为:2Fe3++2e−=2Fe2+。请据此将反应:Fe+2H+=Fe2++H2↑拆写成两个“半反应式”:氧化反应为____________________ ;还原反应为____________________ 。
(4)某同学写出以下三个化学方程式(未配平)
①NO+HNO3→N2O3+H2O
②NH3+NO→HNO2+H2O
③N2O4+H2O→HNO3+HNO2
其中你认为一定不可能实现的是________ (填序号)。
(2)已知次磷酸(H3PO2)与足量的氢氧化钠溶液反应生成NaH2PO2和H2O,则次磷酸是
(3)一个完整的氧化还原反应方程式可以拆开写成两个“半反应式”,一个是“氧化反应”式,一个是“还原反应”式。如2Fe3++Cu=2Fe2++Cu2+的拆写结果是:氧化反应为:Cu-2e−=Cu2+;还原反应为:2Fe3++2e−=2Fe2+。请据此将反应:Fe+2H+=Fe2++H2↑拆写成两个“半反应式”:氧化反应为
(4)某同学写出以下三个化学方程式(未配平)
①NO+HNO3→N2O3+H2O
②NH3+NO→HNO2+H2O
③N2O4+H2O→HNO3+HNO2
其中你认为一定不可能实现的是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】某同学为了检验家中的两种补铁药(成分均为FeSO4)是否变质,查阅了有关资料,得知SCN-、Fe2+能被酸性KMnO4溶液氧化而使酸性KMnO4溶液褪色,并结合已学的知识设计了如下实验:
①将药片除去糖衣研细后溶解、过滤。
②取滤液分别加入两支试管中,在一支试管中加入酸性KMnO4溶液,在另一支试管中加入KSCN溶液。
请回答下列问题:
(1)若滴入酸性KMnO4溶液后褪色,滴入KSCN溶液后不变红,结论是_______ 。
(2)若滴入酸性KMnO4溶液后不褪色,滴入KSCN溶液变红,结论是_________ 。
(3)若滴入酸性KMnO4溶液后褪色,滴入KSCN溶液变红,结论是________ 。
(4)________ (填“能”或“不能”)将酸性KMnO4溶液和KSCN溶液滴入同一支试管中进行验证,原因是_________________ 。
①将药片除去糖衣研细后溶解、过滤。
②取滤液分别加入两支试管中,在一支试管中加入酸性KMnO4溶液,在另一支试管中加入KSCN溶液。
请回答下列问题:
(1)若滴入酸性KMnO4溶液后褪色,滴入KSCN溶液后不变红,结论是
(2)若滴入酸性KMnO4溶液后不褪色,滴入KSCN溶液变红,结论是
(3)若滴入酸性KMnO4溶液后褪色,滴入KSCN溶液变红,结论是
(4)
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铁器时代是人类发展史中一个极为重要的时代,铁及其化合物在人类的生产、生活中都起了巨大的作用。
(1)长期放置的FeSO4溶液易被氧化而变质,实验室用绿矾FeSO4•xH2O配制FeSO4溶液时为了防止FeSO4溶液变质,采取的方法是________ (用离子方程式表示)。
(2)利用部分变质的FeSO4溶液制备Fe2O3:
溶液部分变质的FeSO4溶液 溶液Ⅰ
溶液Ⅰ 沉淀Ⅱ
沉淀Ⅱ Fe2O3
Fe2O3
①FeSO4溶液与H2O2溶液反应,H2O2的作用为_______ 。
②写出由“溶液Ⅰ”到“沉淀Ⅱ”反应的离子方程式_______ 。
(3)电子工业中,常用FeCl3溶液腐蚀铜,其反应的离子方程式为_______ ,检验反应后的溶液中存在Fe3+的试剂是________ 溶液(填试剂化学式)。
(1)长期放置的FeSO4溶液易被氧化而变质,实验室用绿矾FeSO4•xH2O配制FeSO4溶液时为了防止FeSO4溶液变质,采取的方法是
(2)利用部分变质的FeSO4溶液制备Fe2O3:
溶液部分变质的FeSO4溶液
 溶液Ⅰ
溶液Ⅰ 沉淀Ⅱ
沉淀Ⅱ Fe2O3
Fe2O3①FeSO4溶液与H2O2溶液反应,H2O2的作用为
②写出由“溶液Ⅰ”到“沉淀Ⅱ”反应的离子方程式
(3)电子工业中,常用FeCl3溶液腐蚀铜,其反应的离子方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】铁器时代是人类发展史中⼀个极为重要的时代,铁及其化合物在人类的生产、生活中都起了巨大的作用。
(1)长期放置的 溶液易被氧化而变质,实验室⽤绿矾
溶液易被氧化而变质,实验室⽤绿矾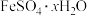 配制
配制 溶液时为了防止
溶液时为了防止 溶液变质,经常向其中加入
溶液变质,经常向其中加入________ ,其原因是______________________ (用离子方程式表示)。
(2)利用部分变质的 溶液制备
溶液制备 :
:
部分变质的 溶液
溶液 溶液I
溶液I 沉淀II
沉淀II

① 溶液作用的离子方程式为
溶液作用的离子方程式为_____________________________________ 。
②写出由“溶液I”到“沉淀II”反应的离子方程式:_______________________________ 。
(3)电子工业中,常用 溶液腐蚀铜,其反应的离子方程式为
溶液腐蚀铜,其反应的离子方程式为________________________ 。
(1)长期放置的
 溶液易被氧化而变质,实验室⽤绿矾
溶液易被氧化而变质,实验室⽤绿矾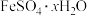 配制
配制 溶液时为了防止
溶液时为了防止 溶液变质,经常向其中加入
溶液变质,经常向其中加入(2)利用部分变质的
 溶液制备
溶液制备 :
:部分变质的
 溶液
溶液 溶液I
溶液I 沉淀II
沉淀II

①
 溶液作用的离子方程式为
溶液作用的离子方程式为②写出由“溶液I”到“沉淀II”反应的离子方程式:
(3)电子工业中,常用
 溶液腐蚀铜,其反应的离子方程式为
溶液腐蚀铜,其反应的离子方程式为
您最近半年使用:0次



