有7种短周期元素的原子序数按A、B、C、D、E、F、G 的顺序依次增大;B元素一种原子的含量常用于判定古生物遗体的年代,A和C元素的原子能形成4核10电子的微粒;D和E可形成离子化合物E2D,E2D中所有微粒的电子数相同,且电子总数为30;E、F、G的最高价氧化物对应的水化物之间可以相互反应;G和D同主族。试回答下列问题:
(1)C元素的原子结构示意图________________ 。
(2)A和D可形成化合物的化学式为______________ 。
(3)B元素在周期表中的位置为________________ ;过量的B元素的最高价氧化物与氢氧化钠溶液反应的离子方程式为__________________ 。
(4)D、E、F、G的离子半径由大到小顺序为(用离子符号表示)______________________ 。
(5)F的单质与E元素的最高价氧化物对应的水化物反应的离子方程式为__________________ 。
(6)上述元素形成的二元化合物中,能够用于漂白的气体物质中含有的化学键类型为__________ ,能够用于漂白的固体物质中阴、阳离子个数比为____________ 。
(7)写出D元素原子形成的10电子微粒X与G元素原子形成的18电子微粒Y反应的离子方程式:________________________ 。
(1)C元素的原子结构示意图
(2)A和D可形成化合物的化学式为
(3)B元素在周期表中的位置为
(4)D、E、F、G的离子半径由大到小顺序为(用离子符号表示)
(5)F的单质与E元素的最高价氧化物对应的水化物反应的离子方程式为
(6)上述元素形成的二元化合物中,能够用于漂白的气体物质中含有的化学键类型为
(7)写出D元素原子形成的10电子微粒X与G元素原子形成的18电子微粒Y反应的离子方程式:
更新时间:2020/02/12 19:48:02
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】元素是组成我们生活的世界中一切物质的“原材料”。
(1)1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,到20世纪初,门捷列夫在周期表中为未知元素留下的空位逐渐被填满。而且,随着原子结构的逐渐揭秘,科学家们发现了元素性质不是随着相对原子质量的递增呈现周期性变化,而是随着原子序数(核电荷数)的递增呈现周期性变化。其本质原因是_______ (填标号)。
A.随着核电荷数递增,原子核外电子排布呈现周期性变化
B.随着核电荷数递增,原子半径呈现周期性变化
C.随着核电荷数递增,元素最高正化合价呈现周期性变化
(2)有A、B、D、E、X、Y六种短周期元素。X与Y处于同一周期,Y的最高价氧化物对应的水化物与强酸、强碱均能反应。其余元素的信息如图所示:
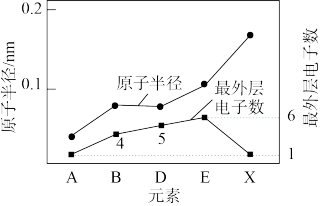
①上述六种元素中,处于第2周期的有_______ (填元素符号),X在周期表中的位置是_______ 。
②E的原子结构示意图为_______ 。
③Y与X的最高价氧化物对应水化物反应的离子方程式为_______ 。
④B和D的最高价氧化物对应水化物的化学式分别为_______ 、_______ ,二者酸性前者_______ (填“强于”或“弱于”)后者,原因是B和D的非金属性有差异,利用原子结构解释产生差异的原因:_______ 。
(1)1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,到20世纪初,门捷列夫在周期表中为未知元素留下的空位逐渐被填满。而且,随着原子结构的逐渐揭秘,科学家们发现了元素性质不是随着相对原子质量的递增呈现周期性变化,而是随着原子序数(核电荷数)的递增呈现周期性变化。其本质原因是
A.随着核电荷数递增,原子核外电子排布呈现周期性变化
B.随着核电荷数递增,原子半径呈现周期性变化
C.随着核电荷数递增,元素最高正化合价呈现周期性变化
(2)有A、B、D、E、X、Y六种短周期元素。X与Y处于同一周期,Y的最高价氧化物对应的水化物与强酸、强碱均能反应。其余元素的信息如图所示:

①上述六种元素中,处于第2周期的有
②E的原子结构示意图为
③Y与X的最高价氧化物对应水化物反应的离子方程式为
④B和D的最高价氧化物对应水化物的化学式分别为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E都是短周期的主族元素,原子序数依次增大,A、B处于同周期,C、D、E同处另一周期,C、A可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙,D是地壳中含量最高的金属元素,E的最高价氧化物对应的水化物是酸性最强的含氧酸。回答下列问题:
(1)B和E分别对应的氢化物的化学式为HB、HE,氢化物的沸点HB_______ HE(填“>”、“<”、“=”,下同),氢化物的稳定性HB_______ HE。
(2)物质乙的电子式为_______ ;物质乙可用于呼吸面具作供氧剂,写出乙与CO2反应的化学方程式:_______ 。
(3)1mol单质B的气体与1molC的氢氧化物在一定条件下恰好完全反应,生成一种盐、水及另一种气体,则所得气体的化学式为:_______ 。
(1)B和E分别对应的氢化物的化学式为HB、HE,氢化物的沸点HB
(2)物质乙的电子式为
(3)1mol单质B的气体与1molC的氢氧化物在一定条件下恰好完全反应,生成一种盐、水及另一种气体,则所得气体的化学式为:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】已知短周期元素M、N、X、Y、Z分布在三个周期,N、X最外层电子数相同,物质A由原子序数依次增大的元素X、Y、Z组成,其中Z的简单离子半径在同周期中最小,X、Y、Z简单离子的核外电子排布相同,物质A的结构式如下图所示:
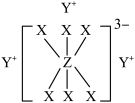
回答下列问题:
(1)请写出YM的电子式:_______ 。
(2)N、X、Y、Z简单离子的半径由大到小的顺序(用对应离子符号表示):_______ 。
(3)在YZO2与YX的混合液中,通入足量CO2,是工业制取A的一种方法,写出该反应的化学方程式:_______ 。
(4)镓(31Ga)与Z为同主族元素,氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。下列有关说法正确的是_______ 。
a. Ga位于元素周期表第四周期IVA族
b. GaN为新型无机非金属材料
c. Ga的最高价氧化物对应水化物的碱性比Z元素最高价氧化物对应水化物的碱性强
d. 酸性:H3AsO4>H3PO4>HNO3
(5)YZM4是有机合成的重要还原剂,其合成路线如图所示

利用YZM4遇水反应生成的氢气的体积测定YZM4样品纯度。
①其反应的化学方程式为_______ 。
②现设计如图四种装置测定YZM4样品的纯度(假设杂质不参与反应)。
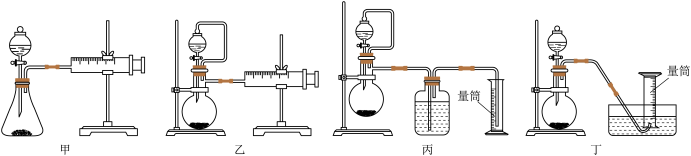
从简约性、准确性考虑,最适宜的方案是_______ (填编号)。
③取样品ag,若实验测得氢气的体积为V L(标准状态),则YZM4样品纯度为_______ (用代数式表示)。

回答下列问题:
(1)请写出YM的电子式:
(2)N、X、Y、Z简单离子的半径由大到小的顺序(用对应离子符号表示):
(3)在YZO2与YX的混合液中,通入足量CO2,是工业制取A的一种方法,写出该反应的化学方程式:
(4)镓(31Ga)与Z为同主族元素,氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。下列有关说法正确的是
a. Ga位于元素周期表第四周期IVA族
b. GaN为新型无机非金属材料
c. Ga的最高价氧化物对应水化物的碱性比Z元素最高价氧化物对应水化物的碱性强
d. 酸性:H3AsO4>H3PO4>HNO3
(5)YZM4是有机合成的重要还原剂,其合成路线如图所示

利用YZM4遇水反应生成的氢气的体积测定YZM4样品纯度。
①其反应的化学方程式为
②现设计如图四种装置测定YZM4样品的纯度(假设杂质不参与反应)。

从简约性、准确性考虑,最适宜的方案是
③取样品ag,若实验测得氢气的体积为V L(标准状态),则YZM4样品纯度为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】下表是部分短周期元素的原子半径及主要化合价:
试回答下列问题:
(1)五种元素中原子半径最大的元素在周期表中位置是 。
(2)Y的氢化物比Q的氢化物沸点高的原因是 。
(3)X或与R按1∶1的原子个数比形成化合物甲,甲中存在的化学键有 ;X可与W组成含18e-的化合物乙,则乙的电子式为 ;X可与Z组成一种有恶臭味的气体丙,丙分子中各原子最外层均满足8e-结构,且含有非极性键。1 mol
丙气体可与2 mol氧气完全反应,生成一种气体,且反应前后气体的总体积不变,该生成物能使澄清石灰水变浑浊,请写出丙分子的结构式 。
| 元素代号 | W | R | X | Y | Z | Q |
| 原子半径/nm | 0.037 | 0.186 | 0.074 | 0.075 | 0.077 | 0.110 |
| 主要化合价 | +1 | +1 | -2 | -3,+5 | +2、+4 | -3、+5 |
(1)五种元素中原子半径最大的元素在周期表中位置是 。
(2)Y的氢化物比Q的氢化物沸点高的原因是 。
(3)X或与R按1∶1的原子个数比形成化合物甲,甲中存在的化学键有 ;X可与W组成含18e-的化合物乙,则乙的电子式为 ;X可与Z组成一种有恶臭味的气体丙,丙分子中各原子最外层均满足8e-结构,且含有非极性键。1 mol
丙气体可与2 mol氧气完全反应,生成一种气体,且反应前后气体的总体积不变,该生成物能使澄清石灰水变浑浊,请写出丙分子的结构式 。
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的原子半径最小;B元素的最高价氧化物对应水化物与其氢化物能生成盐;D与A同主族,且与E同周期;E元素原子的最外层电子数比次外层电子数少2;A、B、D、E这四种元素,每一种与C元素都能形成原子个数比不相同的若干种化合物。请回答:
(1)C和E两种元素相比较,原子得电子能力较强的是(填元素名称)__________ ,以下三种说法中,可以验证该结论的是(填写编号)__________ ;
A.比较这两种元素的常见单质的沸点
B.二者形成的化合物中,C元素的原子显负价
C.比较这两种元素的气态氢化物的稳定性
(2)A、B、C、E可形成两种酸式盐(均含有该四种元素),这两种酸式盐在水溶液中相互反应的离子方程式为__________________________________ 。
(3)C与D形成的某种化合物可作潜水面具中的供氧剂,每生成标准状况下11.2LO2,消耗该化合物的质量为___________ 。
(4)B2A4是一种可燃性液体,B2A4—空气燃料电池是一种碱性燃料电池,B2A4的氧化产物为B2。用该燃料电池电解足量的饱和食盐水,如下图所示,电解装置内发生反应的离子方程式为__________________________________________ ;检验Y极产物的方法是___________________________________________________ ;每生成0.1mol该产物,燃料电池中消耗B2A4的物质的量为___________ 。
(1)C和E两种元素相比较,原子得电子能力较强的是(填元素名称)
A.比较这两种元素的常见单质的沸点
B.二者形成的化合物中,C元素的原子显负价
C.比较这两种元素的气态氢化物的稳定性
(2)A、B、C、E可形成两种酸式盐(均含有该四种元素),这两种酸式盐在水溶液中相互反应的离子方程式为
(3)C与D形成的某种化合物可作潜水面具中的供氧剂,每生成标准状况下11.2LO2,消耗该化合物的质量为
(4)B2A4是一种可燃性液体,B2A4—空气燃料电池是一种碱性燃料电池,B2A4的氧化产物为B2。用该燃料电池电解足量的饱和食盐水,如下图所示,电解装置内发生反应的离子方程式为

您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、J、Q五种短周期主族元素,原子序数依次增大。Z是地壳中含量最高的元素,J的焰色反应呈黄色,Q的最外层电子数与其电子总数之比为3∶8,X能与J形成离子化合物JX,含Y的氧化物是光化学烟雾的主要污染物。
(1)Q在元素周期表中的位置是_______ 。
(2)用电子式表示JX的形成过程:_______ 。
(3)将这五种元素的原子半径从大到小排列,排在第三位的元素是_______ (填元素符号)。
(4)元素的非金属性:Z_______ (填“>”或“<”)Q,下列不能说明这一结论的事实是_______ (填字母)。
A.Q的氢化物的水溶液放置在空气中会变浑浊
B.化合物 中,Z显负价,Q显正价
中,Z显负价,Q显正价
C.常温常压下,Z的单质为气体,Q的单质为固体
D.简单气态氢化物的热稳定性:Z>Q
(5)Q的氢化物可与它的 价氧化物相互反应,该反应的化学方程式为
价氧化物相互反应,该反应的化学方程式为_______ 。
(6)X与Y可形成阳离子B,该阳离子的电子数为10,写出B的电子式:_______ 。
(1)Q在元素周期表中的位置是
(2)用电子式表示JX的形成过程:
(3)将这五种元素的原子半径从大到小排列,排在第三位的元素是
(4)元素的非金属性:Z
A.Q的氢化物的水溶液放置在空气中会变浑浊
B.化合物
 中,Z显负价,Q显正价
中,Z显负价,Q显正价C.常温常压下,Z的单质为气体,Q的单质为固体
D.简单气态氢化物的热稳定性:Z>Q
(5)Q的氢化物可与它的
 价氧化物相互反应,该反应的化学方程式为
价氧化物相互反应,该反应的化学方程式为(6)X与Y可形成阳离子B,该阳离子的电子数为10,写出B的电子式:
您最近半年使用:0次



