有一种矿石,经测定含有镁、硅、氧三种元素且它们的质量比为12∶7∶16。
(1)用盐的组成表示其化学式:___________ 。
(2)用氧化物的组成表示其化学式:_______ 。
(3)该矿石的成分属于________ (填物质的分类)。
(4)写出该矿石(氧化物形式)与盐酸反应的化学方程式:______ 。
(1)用盐的组成表示其化学式:
(2)用氧化物的组成表示其化学式:
(3)该矿石的成分属于
(4)写出该矿石(氧化物形式)与盐酸反应的化学方程式:
19-20高一下·安徽淮北·课后作业 查看更多[2]
更新时间:2020-02-14 16:02:26
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】化学计量在化学中占有重要地位。请回答下列问题:
(1)青蒿素C15H22O5的摩尔质量为____ 。
(2)在标准状况下,22.4L由O2和N2组成的混合气体中,含有的分子总数约为____ 。
(3)在标准状况下,含有3.01×1023个氦原子的氦气的体积约为____ 。
(4)某消毒小组人员用17mol·L-1的浓硫酸配制480mL3.4mol·L-1的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为____ mL;所配溶液中的H+的物质的量浓度为____ 。
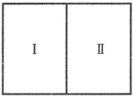
(5)如图所示,气缸的总体积一定,内部被活塞隔成I、II两部分,活塞可以自由移动,也可以固定。0℃时向I中充入8gSO2,II中充入8gO2,则当活塞不再移动时,I、II两部分体积比为____ 。
(1)青蒿素C15H22O5的摩尔质量为
(2)在标准状况下,22.4L由O2和N2组成的混合气体中,含有的分子总数约为
(3)在标准状况下,含有3.01×1023个氦原子的氦气的体积约为
(4)某消毒小组人员用17mol·L-1的浓硫酸配制480mL3.4mol·L-1的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为
(5)如图所示,气缸的总体积一定,内部被活塞隔成I、II两部分,活塞可以自由移动,也可以固定。0℃时向I中充入8gSO2,II中充入8gO2,则当活塞不再移动时,I、II两部分体积比为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】固体聚合硫酸铁(SPFS)是一种重要的无机高分子絮凝剂,极易溶于水,其化学组成可表示为Fex(OH)y(SO4)z•nH2O。
Ⅰ.SPFS的工业制备:
用绿矾(FeSO4·7H2O)与NaClO3溶液在酸性介质中充分反应,经水解、聚合、减压蒸发可得到聚合硫酸铁
Ⅱ.SPFS的组成测定:
取8.19g某固体聚合硫酸铁溶解于水,向其中加入过量的BaCl2溶液到沉淀完全,经过滤、洗涤、干燥得到9.32g白色沉淀;向滤液中加入NH3·H2O,调节溶液pH=6,经过滤、洗涤、干燥、灼烧得到4.00 g固体Fe2O3。
(1)从FeSO4溶液中得到绿矾的实验操作为___________________________ 。
(2)Ⅰ中绿矾与NaClO3溶液反应的离子方程式为______________________ 。
(3)Ⅱ中当溶液pH=6时,c(Fe3+)=_______ 。(已知:Ksp[Fe (OH) 3]=4.0×10-38)
(4)该SPFS的化学式为______________ (写出计算过程)。
Ⅰ.SPFS的工业制备:
用绿矾(FeSO4·7H2O)与NaClO3溶液在酸性介质中充分反应,经水解、聚合、减压蒸发可得到聚合硫酸铁
Ⅱ.SPFS的组成测定:
取8.19g某固体聚合硫酸铁溶解于水,向其中加入过量的BaCl2溶液到沉淀完全,经过滤、洗涤、干燥得到9.32g白色沉淀;向滤液中加入NH3·H2O,调节溶液pH=6,经过滤、洗涤、干燥、灼烧得到4.00 g固体Fe2O3。
(1)从FeSO4溶液中得到绿矾的实验操作为
(2)Ⅰ中绿矾与NaClO3溶液反应的离子方程式为
(3)Ⅱ中当溶液pH=6时,c(Fe3+)=
(4)该SPFS的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】物质的量是高中化学常用的物理量之一,请完成以下问题:
(1)某气体氧化物的化学式为 ,在标准状况下,1.28g该氧化物的体积为448mL,则R的相对原子质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则R的相对原子质量为_______ 。
(2)在标准状况下,15gCO与 的混合气体体积为11.2L,则
的混合气体体积为11.2L,则 与CO的体积比是
与CO的体积比是_____ 。
(3)把100mL含有 和
和 的混合溶液分成两等份,一份加入含bmolNaOH的溶液,恰好使镁离子沉淀完全;另一份加入含amol
的混合溶液分成两等份,一份加入含bmolNaOH的溶液,恰好使镁离子沉淀完全;另一份加入含amol 的溶液,恰好使硫酸根离子沉淀完全。则原混合溶液中钾离子的浓度为
的溶液,恰好使硫酸根离子沉淀完全。则原混合溶液中钾离子的浓度为_______ 。
(4)实验室中需要0.2mol/L的 溶液480mL,现配制该溶液,用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少
溶液480mL,现配制该溶液,用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少_______ (填仪器名称)。用托盘天平称取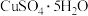 晶体的质量是
晶体的质量是_______ g。转移溶液后未洗涤烧杯和玻璃棒就直接定容,最终会使所配得的溶液浓度_______ (填“偏大”、“偏小”或“无影响”,下同);若在容量瓶中定容时俯视刻度线,最终会使配得的溶液浓度_______ 。
(1)某气体氧化物的化学式为
 ,在标准状况下,1.28g该氧化物的体积为448mL,则R的相对原子质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则R的相对原子质量为(2)在标准状况下,15gCO与
 的混合气体体积为11.2L,则
的混合气体体积为11.2L,则 与CO的体积比是
与CO的体积比是(3)把100mL含有
 和
和 的混合溶液分成两等份,一份加入含bmolNaOH的溶液,恰好使镁离子沉淀完全;另一份加入含amol
的混合溶液分成两等份,一份加入含bmolNaOH的溶液,恰好使镁离子沉淀完全;另一份加入含amol 的溶液,恰好使硫酸根离子沉淀完全。则原混合溶液中钾离子的浓度为
的溶液,恰好使硫酸根离子沉淀完全。则原混合溶液中钾离子的浓度为(4)实验室中需要0.2mol/L的
 溶液480mL,现配制该溶液,用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少
溶液480mL,现配制该溶液,用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少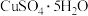 晶体的质量是
晶体的质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】请按照下列要求做题。
(1)滑石一种硅酸盐矿物,其化学式为Mg3Si4O10(OH)2,用氧化物的形式表示为__________ 。
(2)除去下列物质中所含杂质(括号内为杂质),写出除去杂质的试剂。
① Fe2O3(Al2O3)_____________ ② NO(NO2)_____________
③ Cl2(HCl)_______________ ④ FeCl3(FeCl2)____________
(3)用铝箔包裹0.1mol金属钠,用针扎若干小孔,放入水中,完全反应后,用排水取气法收集到标准状况下气体的体积是_________ (填字母序号)
a.1.12L b.>1.12L c.<1.12L
(1)滑石一种硅酸盐矿物,其化学式为Mg3Si4O10(OH)2,用氧化物的形式表示为
(2)除去下列物质中所含杂质(括号内为杂质),写出除去杂质的试剂。
① Fe2O3(Al2O3)
③ Cl2(HCl)
(3)用铝箔包裹0.1mol金属钠,用针扎若干小孔,放入水中,完全反应后,用排水取气法收集到标准状况下气体的体积是
a.1.12L b.>1.12L c.<1.12L
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请回答:
(1)用氧化物表示翡翠:NaAl(SiO3)2的组成___________________ 。
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由___________________ 。
(3)在NaHSO4溶液中滴加Ba(OH)2溶液恰好完全沉淀,写出反应的离子方程式____________
(4)写出化学反应方程式
①煅烧黄铁矿__________________________ 。
②用氨气制硝酸的第一步__________________________ 。
(1)用氧化物表示翡翠:NaAl(SiO3)2的组成
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由
(3)在NaHSO4溶液中滴加Ba(OH)2溶液恰好完全沉淀,写出反应的离子方程式
(4)写出化学反应方程式
①煅烧黄铁矿
②用氨气制硝酸的第一步
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】“蛇纹石石棉”主要成分有二氧化硅、氧化镁和结晶水,它的化学式是Mg6[(OH)4Si2O5]2。
(1)“蛇纹石石棉”的氧化物形式为______________________ ,其中原子半径最大的元素在周期表中的位置是______________________ 。
(2)Si原子的最外层的电子排布式为_____________ ,SiO2与NaOH溶液反应的化学方程式为________________________________________________ 。
(3)SiCl4比SiO2的熔点_____ (填“低”、“高”),原因是__________________________ 。
(4)从哪些方面不能判断Si和O的非金属性强弱________ 。
A.利用Si和O在周期表中的位置
B.SiO2与水不发生反应
C.Si在一定条件下与氧气反应,生成SiO2
D.H2SiO3的酸性比H2O的酸性强
(1)“蛇纹石石棉”的氧化物形式为
(2)Si原子的最外层的电子排布式为
(3)SiCl4比SiO2的熔点
(4)从哪些方面不能判断Si和O的非金属性强弱
A.利用Si和O在周期表中的位置
B.SiO2与水不发生反应
C.Si在一定条件下与氧气反应,生成SiO2
D.H2SiO3的酸性比H2O的酸性强
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)一个体重50 kg的健康人含铁元素2 g,这2 g铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4)。服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收。
①人体中经常进行Fe2+与Fe3+的转化,可表示为Fe2+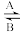 Fe3+。“服用维生素C可使食物中的Fe3+转化为Fe2+”, 由此可以推知维生素C在该过程中作
Fe3+。“服用维生素C可使食物中的Fe3+转化为Fe2+”, 由此可以推知维生素C在该过程中作___________ 剂。
②腌制食品中含有亚硝酸盐,亚硝酸盐能使人体内的铁元素发生A过程,过多食用会发生食物中毒,Fe2+此过程中表现出___________ 性。
③已知下列反应在一定条件下发生:
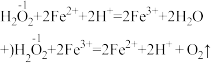
总反应式:2H2O2 2H2O+O2↑
2H2O+O2↑
在以上的反应中,Fe2+实际上起着___________ 的作用。
(2)硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
①下列物质不是硅酸盐材料的是___________
A.陶瓷 B.玻璃 C.水泥 D.生石灰
②SiO2是玻璃的成分之一,SiO2与氢氧化钠溶液反应的离子方程式___________ ,工艺师常用___________ (填物质名称)来雕刻玻璃。
③试管中加入3~5mL Na2SiO3溶液,滴入1~2滴酚酞溶液,再用胶头滴管逐滴加入稀盐酸,边加边振荡,至溶液红色变浅接近消失时停止,静置即得到硅酸胶体,该反应的化学方程式为___________ 。
①人体中经常进行Fe2+与Fe3+的转化,可表示为Fe2+
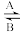 Fe3+。“服用维生素C可使食物中的Fe3+转化为Fe2+”, 由此可以推知维生素C在该过程中作
Fe3+。“服用维生素C可使食物中的Fe3+转化为Fe2+”, 由此可以推知维生素C在该过程中作②腌制食品中含有亚硝酸盐,亚硝酸盐能使人体内的铁元素发生A过程,过多食用会发生食物中毒,Fe2+此过程中表现出
③已知下列反应在一定条件下发生:
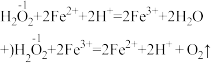
总反应式:2H2O2
 2H2O+O2↑
2H2O+O2↑在以上的反应中,Fe2+实际上起着
(2)硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
①下列物质不是硅酸盐材料的是
A.陶瓷 B.玻璃 C.水泥 D.生石灰
②SiO2是玻璃的成分之一,SiO2与氢氧化钠溶液反应的离子方程式
③试管中加入3~5mL Na2SiO3溶液,滴入1~2滴酚酞溶液,再用胶头滴管逐滴加入稀盐酸,边加边振荡,至溶液红色变浅接近消失时停止,静置即得到硅酸胶体,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】硅是带来人类文明的重要元素之一,从传统材料到信息材料的发展过程中创造了一个又一个奇迹。
(1)分别向Na2SiO3溶液中加入下列物质,能生成不溶于NaOH溶液的白色沉淀的是________ 。
①K ②稀盐酸 ③CaCl2溶液 ④KNO3溶液
(2)胃舒平的主要成分是氢氧化铝,同时含有三硅酸镁(Mg2Si3O8·4H2O)等化合物。写出三硅酸镁的氧化物形式为_______________ 。
(3)为什么实验室中盛放NaOH溶液的试剂瓶不能用玻璃塞(用离子方程式表示):_________________ 。
(4)当前制备高纯硅的主要生产过程示意图如下:_________________ 。
②高纯硅的用途:_____________ 。(写出一种)
③整个制备过程必须严格控制无水无氧。H2还原SiHCl3过程中若混有O2,可能引起的后果是_______________ 。
(1)分别向Na2SiO3溶液中加入下列物质,能生成不溶于NaOH溶液的白色沉淀的是
①K ②稀盐酸 ③CaCl2溶液 ④KNO3溶液
(2)胃舒平的主要成分是氢氧化铝,同时含有三硅酸镁(Mg2Si3O8·4H2O)等化合物。写出三硅酸镁的氧化物形式为
(3)为什么实验室中盛放NaOH溶液的试剂瓶不能用玻璃塞(用离子方程式表示):
(4)当前制备高纯硅的主要生产过程示意图如下:

②高纯硅的用途:
③整个制备过程必须严格控制无水无氧。H2还原SiHCl3过程中若混有O2,可能引起的后果是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)硅元素在自然界中通常以石英石( )和硅酸盐的形式存在。请写出
)和硅酸盐的形式存在。请写出 与氢氧化钠溶液反应的化学方程式
与氢氧化钠溶液反应的化学方程式___________ 。
(2)高纯硅单质可由石英砂(主要成分是 )制得,制备高纯硅的主要工艺流程如图所示:
)制得,制备高纯硅的主要工艺流程如图所示:___________ 。
ⅱ.流程①焦炭体现了___________ (填“氧化性”或“还原性”)。
(3)氮化硅是一种新型陶瓷材料,可由石英固体与焦炭颗粒在高温的氮气流中通过如下反应制得 ,请用单线桥表示该反应电子转移的方向与数目
,请用单线桥表示该反应电子转移的方向与数目___________ 。
(4)工业上可利用水玻璃和盐酸反应制备硅酸凝胶,写出水玻璃和盐酸反应的离子方程式___________ 。
(5)关于硅及其相关化合物的叙述正确的是___________。
(1)硅元素在自然界中通常以石英石(
 )和硅酸盐的形式存在。请写出
)和硅酸盐的形式存在。请写出 与氢氧化钠溶液反应的化学方程式
与氢氧化钠溶液反应的化学方程式(2)高纯硅单质可由石英砂(主要成分是
 )制得,制备高纯硅的主要工艺流程如图所示:
)制得,制备高纯硅的主要工艺流程如图所示: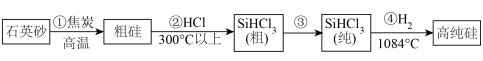
ⅱ.流程①焦炭体现了
(3)氮化硅是一种新型陶瓷材料,可由石英固体与焦炭颗粒在高温的氮气流中通过如下反应制得
 ,请用单线桥表示该反应电子转移的方向与数目
,请用单线桥表示该反应电子转移的方向与数目(4)工业上可利用水玻璃和盐酸反应制备硅酸凝胶,写出水玻璃和盐酸反应的离子方程式
(5)关于硅及其相关化合物的叙述正确的是___________。
A.已知 与 与 在同一主族,由于 在同一主族,由于 ,用类比法得知 ,用类比法得知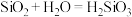 |
B.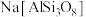 用氧化物形式表示为 用氧化物形式表示为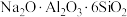 |
| C.硅元素在金属元素与非金属元素的分界线处,因此单质硅具有弱导电性,一般可用于作为半导体材料 |
| D.高温熔融纯碱时可选用石英玻璃坩埚 |
您最近一年使用:0次



