三硝酸甘油酯[C3H5(ONO2)3]是一种炸药,可因撞击而爆炸,同时产生高温。爆炸按下式进行:4C3H5(ONO2)3→wN2+xCO2+yH2O+zO2(式中w,x,y,z为化学计量数)。科学实验证明:相同条件(温度、压力)下相同体积的不同气体所含分子数相等。当三硝酸甘油酯爆炸并恢复到常温时,所得气体的体积比为____ 。
更新时间:2020-02-18 16:18:18
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】(1)同温同压下,等质量的SO2和SO3气体的体积比为:__________ ;密度比为:________ 。
(2)实验中需配制80 mL1 mol/L CuSO4溶液,若用CuSO4 • 5H2O替代,则应称取CuSO4 • 5H2O的质最为____ g。
(3)某气体在标准状况下的密度为1.25 g/L,则28g该气体所含有的分子数为_______ 。
(4)气体化合物A的分子式为NxOy,已知同温同压下10mLA受热分解生成10 mL N2和15 mLO2,则A的分子式为:_____________ 。
(5)用等体积的0.1 mol·L-1的BaCl2溶液,可使相同体积的Fe2(SO4)3、Na2SO4、KAl(SO4)2三种溶液中的 完全沉淀,则三种硫酸盐的物质的量浓度之比为
完全沉淀,则三种硫酸盐的物质的量浓度之比为________ 。
(2)实验中需配制80 mL1 mol/L CuSO4溶液,若用CuSO4 • 5H2O替代,则应称取CuSO4 • 5H2O的质最为
(3)某气体在标准状况下的密度为1.25 g/L,则28g该气体所含有的分子数为
(4)气体化合物A的分子式为NxOy,已知同温同压下10mLA受热分解生成10 mL N2和15 mLO2,则A的分子式为:
(5)用等体积的0.1 mol·L-1的BaCl2溶液,可使相同体积的Fe2(SO4)3、Na2SO4、KAl(SO4)2三种溶液中的
 完全沉淀,则三种硫酸盐的物质的量浓度之比为
完全沉淀,则三种硫酸盐的物质的量浓度之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)在14.2gNa2SO4中:含有的Na+的数目是___ ;含有的SO 的质量是
的质量是___ ;含氧原子的物质的量是___ 。
(2)同温同压下,若A容器中充满O2和B容器中充满O3。
①若所含分子总数相等,则A容器和B容器的容积之比是__ ;
②若两容器中所含原子总数相等,则A容器和B容器的容积比是___ ;
③若两容器的体积比为3:2,则O2和O3的质量之比为___ ,密度之比为____ 。
 的质量是
的质量是(2)同温同压下,若A容器中充满O2和B容器中充满O3。
①若所含分子总数相等,则A容器和B容器的容积之比是
②若两容器中所含原子总数相等,则A容器和B容器的容积比是
③若两容器的体积比为3:2,则O2和O3的质量之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)4.9 g H3PO4可与_______ molNaOH完全反应生成正盐。
(2)19 g某二价金属的氯化物中含有0.4 mol Cl-,此氯化物的摩尔质量___ 。
(3)8.4 g N2与9.6 g某单质RX,所含原子个数相同,且分子数之比为3:2,则R的相对原子质量是______ ,x的值为______
(4)液态化合物XOY常用作粮食的熏蒸剂,取一定量的XOY在O2中恰好完全燃烧,反应的化学方程式为:2XOY(液)+3O2(气)===2XO2(气)+2YO2(气),冷却至标准状况下(各物质状态见括号),测得生成物体积是448mL,密度是2.41g/L,则反应前O2在标况下的体积是_________ 。
(2)19 g某二价金属的氯化物中含有0.4 mol Cl-,此氯化物的摩尔质量
(3)8.4 g N2与9.6 g某单质RX,所含原子个数相同,且分子数之比为3:2,则R的相对原子质量是
(4)液态化合物XOY常用作粮食的熏蒸剂,取一定量的XOY在O2中恰好完全燃烧,反应的化学方程式为:2XOY(液)+3O2(气)===2XO2(气)+2YO2(气),冷却至标准状况下(各物质状态见括号),测得生成物体积是448mL,密度是2.41g/L,则反应前O2在标况下的体积是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】硫铁矿又称黄铁矿,是生产硫酸的原料,其主要成分为FeS2。850℃~950℃时,空气中煅烧,可能发生下列反应(设空气中N2与O2体积比为4:1):4FeS2+11O2→2Fe2O3+8SO2。
(1)含硫35%的硫铁矿样品(杂质不含硫),其FeS2的含量为________ 。
(2)设1t纯净的FeS2完全反应,产生标准状况下SO2________ m3。
(3)为使FeS2煅烧完全生成Fe2O3,工业上使用过量空气,当空气过量20%时,所得炉气中SO2的体积分数为多少________ 。
(1)含硫35%的硫铁矿样品(杂质不含硫),其FeS2的含量为
(2)设1t纯净的FeS2完全反应,产生标准状况下SO2
(3)为使FeS2煅烧完全生成Fe2O3,工业上使用过量空气,当空气过量20%时,所得炉气中SO2的体积分数为多少
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
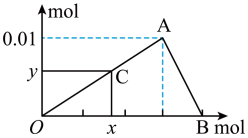
【推荐3】将3 mol/L氢氧化钠溶液滴入到25 mL一定浓度的氯化铝溶液中,如图是整个过程的数学分析曲线,其中横轴表示加入 的物质的量,纵轴表示产生的沉淀物质的量。图中OA曲线表示的离子反应是
的物质的量,纵轴表示产生的沉淀物质的量。图中OA曲线表示的离子反应是___________ ,由此可得A点的坐标为___________ ;AB曲线表示的离子反应是___________ ,由此可得B点的坐标为___________ 。由上述分析可求氯化铝溶液中 离子的浓度为
离子的浓度为___________ 。
 的物质的量,纵轴表示产生的沉淀物质的量。图中OA曲线表示的离子反应是
的物质的量,纵轴表示产生的沉淀物质的量。图中OA曲线表示的离子反应是 离子的浓度为
离子的浓度为
您最近一年使用:0次



