下表中的实线表示元素周期表的部分边界。

(1)请在上表中用实线补出元素周期表的上边界。_____________
(2)某主族元素原子的核外电子排布为: ,该元素在元素周期表中的位置为
,该元素在元素周期表中的位置为_______________ 。
(3)元素I的非金属性________ (填“强于”或“弱于”)元素H,用原子结构的观点解释原因:同周期元素随着原子序数的递增,______________________ ,非金属性增强。设计实验证明元素E的金属性强于元素F:__________________________ 。
(4)处于周期表中对角线位置(左上方和右下方) 的元素,其性质具有相似性,称为“对角线规则”。元素D与F的单质及其化合物性质相似,如D、DO、D(OH)2与NaOH溶液都能反应生成Na2DO2等物质。回答下列问题。
①写出F的单质与氢氧化钠溶液反应的离子方程式___________________________ 。
②鉴别元素D与E的氢氧化物可用试剂是_________________ 。

(1)请在上表中用实线补出元素周期表的上边界。
(2)某主族元素原子的核外电子排布为:
 ,该元素在元素周期表中的位置为
,该元素在元素周期表中的位置为(3)元素I的非金属性
(4)处于周期表中对角线位置(左上方和右下方) 的元素,其性质具有相似性,称为“对角线规则”。元素D与F的单质及其化合物性质相似,如D、DO、D(OH)2与NaOH溶液都能反应生成Na2DO2等物质。回答下列问题。
①写出F的单质与氢氧化钠溶液反应的离子方程式
②鉴别元素D与E的氢氧化物可用试剂是
更新时间:2020-02-15 10:39:10
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下表列出了①~⑨九种元素在周期表中的位置。

请按要求回答下列问题:
(1)元素②的原子结构示意图___ 。①、④按原子个数比为1:1组成的分子的电子式___ 。
(2)⑤⑥两种元素的离子半径由大到小的顺序是___ (填化学符号),⑧和⑨两种元素的最高价氧化物对应的水化物中酸性较强的是___ (填化学式)。
(3)元素⑤的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应水化物反应,其离子方程式为___ 。
(4)元素④、⑧的氢化物组成结构相似,二者相同条件下沸点较高的是___ (填化学式)。
(5)写出⑤的单质与水反应的离子方程式___ 。

请按要求回答下列问题:
(1)元素②的原子结构示意图
(2)⑤⑥两种元素的离子半径由大到小的顺序是
(3)元素⑤的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应水化物反应,其离子方程式为
(4)元素④、⑧的氢化物组成结构相似,二者相同条件下沸点较高的是
(5)写出⑤的单质与水反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表为元素周期表的一部分,请回答有关问题:
(1)①和⑤的元素符号是 ______ 和 ______ .
(2)表中最活泼的金属是______ ,非金属性最强的元素是 ______  填写元素符号
填写元素符号
(3)表中能形成两性氢氧化物的元素是______  填写元素符号
填写元素符号 ,分别写出该元素的氢氧化物与⑥⑨最高价氧化物的水化物反应的化学方程式:
,分别写出该元素的氢氧化物与⑥⑨最高价氧化物的水化物反应的化学方程式: ______ , ______ .
| 周期 | Ⅰ A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
(2)表中最活泼的金属是
 填写元素符号
填写元素符号
(3)表中能形成两性氢氧化物的元素是
 填写元素符号
填写元素符号 ,分别写出该元素的氢氧化物与⑥⑨最高价氧化物的水化物反应的化学方程式:
,分别写出该元素的氢氧化物与⑥⑨最高价氧化物的水化物反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】四种短周期主族元素在元素周期表中的相对位置如图所示,X元素的原子核外电子数是M的2倍,Y的氧化物具有两性。回答下列问题:
(1)元素Y在周期表中的位置是第________ 周期________ 族。
(2)这四种元素最高价氧化物对应的水化物中,酸性最强的是_________ (填化学式,下同),碱性最强的是________ 。
(3)气体分子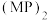 的电子式为
的电子式为_________ 。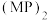 称为拟卤素,性质与卤素类似,其与NaOH溶液反应的化学方程式为
称为拟卤素,性质与卤素类似,其与NaOH溶液反应的化学方程式为__________ 。
M | P | ||
X | Y |
(1)元素Y在周期表中的位置是第
(2)这四种元素最高价氧化物对应的水化物中,酸性最强的是
(3)气体分子
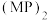 的电子式为
的电子式为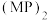 称为拟卤素,性质与卤素类似,其与NaOH溶液反应的化学方程式为
称为拟卤素,性质与卤素类似,其与NaOH溶液反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】为验证同主族元素性质的递变规律。某小组用如图所示的装置进行实验(夹持仪器已略去,装置气密性已检验)。
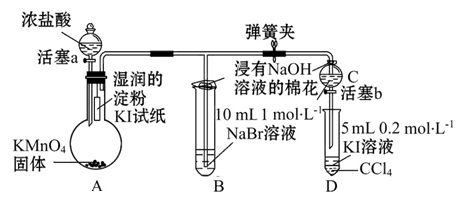
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当装置B和装置C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当装置B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
(1)浸有NaOH溶液的棉花的作用____________________________ 。
(2)装置A中发生的置换反应的化学方程式为___________________ 。
(3)装置B的溶液中NaBr完全被氧化,则消耗Cl2的物质的量为__________ 。
(4)为验证溴元素的非金属性强于碘元素,过程Ⅳ的操作和现象是__________ 。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当装置B和装置C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当装置B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
(1)浸有NaOH溶液的棉花的作用
(2)装置A中发生的置换反应的化学方程式为
(3)装置B的溶液中NaBr完全被氧化,则消耗Cl2的物质的量为
(4)为验证溴元素的非金属性强于碘元素,过程Ⅳ的操作和现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】同学们在实验室中用如图装置验证元素周期表中部分元素性质的递变规律。(部分夹持仪器已省略)
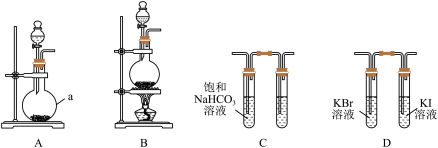
(1)仪器 的名称是
的名称是___________ 。
(2)欲验证氮元素的非金属性强于碳元素,应选择的装置是___________ (填字母)和C,发生装置中的药品是___________ (填字母(可选药品:A.石灰石B.亚硫酸钠C.木炭D.硫酸E.硝酸F.盐酸)。C装置中,右侧试管中的试剂是___________ 。
(3)元素 、
、 、
、 的非金属性由强到弱的顺序是
的非金属性由强到弱的顺序是___________ ,验证该结论时,装置 是制取
是制取___________ (化学式)的发生装置。装有 溶液的试管中的现象是溶液由无色变为
溶液的试管中的现象是溶液由无色变为___________ 色,有关反应的化学方程式是___________ 。该实验能否得出以上元素非金属性的强弱顺序?___________ (填“能”和“不能”)

(1)仪器
 的名称是
的名称是(2)欲验证氮元素的非金属性强于碳元素,应选择的装置是
(3)元素
 、
、 、
、 的非金属性由强到弱的顺序是
的非金属性由强到弱的顺序是 是制取
是制取 溶液的试管中的现象是溶液由无色变为
溶液的试管中的现象是溶液由无色变为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学课外活动小组为了验证主族元素化学性质的递变规律,设计实验如下图所示。
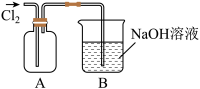
(1)为了验证氯气的氧化性比硫的氧化性强,装置A中盛放的试剂是_______ (填序号),装置A中发生反应的化学方程式为_______ 。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液
(2)下列不能用于验证氯元素比硫元素非金属性强的依据是_______。
(3)若装置A中加入淀粉碘化钾溶液,通入 后观察到装置A中溶液
后观察到装置A中溶液_______ ,即可证明非金属性: 。从原子结构角度解释
。从原子结构角度解释 的非金属性比I强的原因:同主族元素从上到下,
的非金属性比I强的原因:同主族元素从上到下,_______ 。

(1)为了验证氯气的氧化性比硫的氧化性强,装置A中盛放的试剂是
A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液(2)下列不能用于验证氯元素比硫元素非金属性强的依据是_______。
A. 比 比 稳定 稳定 |
B. 的氧化性比 的氧化性比 的强 的强 |
C. 的酸性比 的酸性比 的强 的强 |
D.铁与 反应生成 反应生成 ,而铁与硫反应生成 ,而铁与硫反应生成 |
 后观察到装置A中溶液
后观察到装置A中溶液 。从原子结构角度解释
。从原子结构角度解释 的非金属性比I强的原因:同主族元素从上到下,
的非金属性比I强的原因:同主族元素从上到下,
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】根据A-I元素在周期表中的位置,请用元素符号或化学式 回答有关题目:
(1)ABH组成的化合物存在的化学键有_______ ;元素E在周期表中的位置_______ 。
(2)最高价氧化物的水化物酸性最强的是_______ 。
(3)在B、E、I、K、J中,原子半径从大到小的排序是_______ ,A和D组成的最简单化合物的电子式_______ 。
(4)化合物AK与化合物AF3发生反应的现象是:_______ 。
(5)B的最高价氧化物的水化物和C的最高价氧化物相互反应的化学方程式_______ 。
族 周期 | I A | Ⅱ A | Ⅲ A | Ⅳ A | Ⅴ A | Ⅵ A | Ⅶ A | O |
| 1 | A | |||||||
| 2 | D | F | H | J | L | |||
| 3 | B | C | E | G | I | K |
(2)最高价氧化物的水化物酸性最强的是
(3)在B、E、I、K、J中,原子半径从大到小的排序是
(4)化合物AK与化合物AF3发生反应的现象是:
(5)B的最高价氧化物的水化物和C的最高价氧化物相互反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语 回答下列问题:
(1)④、⑤、⑧的简单离子半径由大到小的顺序是___________ 。
(2)③、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是___________ 。
(3)①与③能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质的电子式为___________ 。
(4)工业制⑥的单质时,电解其氧化物而不电解其氯化物的原因是___________ 。
(5)⑤在空气中加热形成化合物的化学式是___________ ,写出该物质与水反应的化学方程式___________ 。
(6)元素X与⑦同一主族,X原子比⑦原子多一个电子层,X的原子结构示意图为___________ ,其氢化物的化学式为___________ 。
族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)③、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是
(3)①与③能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质的电子式为
(4)工业制⑥的单质时,电解其氧化物而不电解其氯化物的原因是
(5)⑤在空气中加热形成化合物的化学式是
(6)元素X与⑦同一主族,X原子比⑦原子多一个电子层,X的原子结构示意图为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】已知A、B、C为同一短周期的三种元素,它们的原子序数依次增大且和为40;A是该周期中(除稀有气体元素外)原子半径最大的元素,B元素的原子核外M层上的电子数比K层上的电子数多1,从原子结构上看其原因是________________________________________________ 。A、B、C三元素形成简单离子的半径大小顺序为____________ 。(用离子符号表示)
比较A、B单质活泼性的实验方法是__________________________________________ 。
比较A、B单质活泼性的实验方法是
您最近一年使用:0次



