以甲醇为燃料的电池中,电解质溶液为酸性,则负极反应式为______________ ,正极反应式为__________________ 。理想状态下,该燃料电池消耗1mol甲醇所能产生的最大电能为702.1kJ,则该燃料电池的理论效率为________________ (燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比,甲醇的燃烧热为ΔH= -726.5kJ/mol)。
19-20高二上·福建莆田·期中 查看更多[2]
福建省莆田市仙游县枫亭中学2019-2020学年高二上学期期中考试(选考)化学试题(已下线)1.2.2 化学电源(基础练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)
更新时间:2020-03-03 17:38:27
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】电化学知识在生产、科技研究中应用广泛。
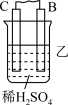
(1)某同学根据漂白粉的制备原理和电解原理制作了一种家用环保型消毒液发生器(如图所示,没有使用离子交换膜),用石墨作电极电解饱和氯化钠溶液。通电时,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液,则:
①a为电源的___________ (负极或正极)
②写出电解饱和食盐水的化学方程式___________ 。用惰性电极电解一段时间后(食盐水足量),加入___________ 恢复到电解前的浓度和pH。
(2)电化学原理在防止金属腐蚀、能量转换、物质合成、环境治理等方面应用广泛。研究金属腐蚀和防腐的原理很有现实意义。
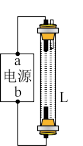
①下图中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择______ (填标号)。
A.碳棒 B.锌板 C.铜板

②金属腐蚀一般可分为化学腐蚀和电化学腐蚀。炒过菜的铁锅未及时清洗容易发生电化学腐蚀而生锈。请写出铁锅生锈过程的正极反应式:______ 。
③金属阳极钝化是一种电化学防腐方法。将Fe作阳极置于H2SO4溶液中,一定条件下Fe钝化形成致密Fe3O4氧化膜,试写出该阳极电极反应式______ 。
(3)随着国家大力发展清洁能源产业的要求,新能源产业规模迅速壮大。试完成下列问题。
现在电瓶车所用电池一般为铅酸蓄电池,如图所示:
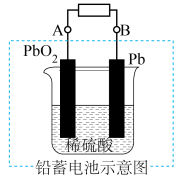
这是一种典型的可充电电池,电池总反应式为 。则电池放电时,当转移0.2mol电子时,B电极的质量将
。则电池放电时,当转移0.2mol电子时,B电极的质量将___________ (填“增加”“减小”或“不变”),______ g。
(1)某同学根据漂白粉的制备原理和电解原理制作了一种家用环保型消毒液发生器(如图所示,没有使用离子交换膜),用石墨作电极电解饱和氯化钠溶液。通电时,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液,则:

①a为电源的
②写出电解饱和食盐水的化学方程式
(2)电化学原理在防止金属腐蚀、能量转换、物质合成、环境治理等方面应用广泛。研究金属腐蚀和防腐的原理很有现实意义。
①下图中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择
A.碳棒 B.锌板 C.铜板

②金属腐蚀一般可分为化学腐蚀和电化学腐蚀。炒过菜的铁锅未及时清洗容易发生电化学腐蚀而生锈。请写出铁锅生锈过程的正极反应式:
③金属阳极钝化是一种电化学防腐方法。将Fe作阳极置于H2SO4溶液中,一定条件下Fe钝化形成致密Fe3O4氧化膜,试写出该阳极电极反应式
(3)随着国家大力发展清洁能源产业的要求,新能源产业规模迅速壮大。试完成下列问题。
现在电瓶车所用电池一般为铅酸蓄电池,如图所示:

这是一种典型的可充电电池,电池总反应式为
 。则电池放电时,当转移0.2mol电子时,B电极的质量将
。则电池放电时,当转移0.2mol电子时,B电极的质量将
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)下列关于充电电池、干电池的叙述合理的是___ 。
①干电池可以实现化学能向电能的转化和电能向化学能的转化
②锌锰干电池长时间连续使用时内装糊状物可能流出腐蚀电器
③充电电池可以无限制地反复放电、充电
④充电是使放电时的氧化还原反应逆向进行
(2)铅蓄电池中,正极材料为PbO2,负极材料为Pb,放电时其负极反应式为___ 。
(3)原电池在NaOH溶液介质中,铝为负极,其负极反应式为__ 。
(4)航天技术中使用的氢氧燃料电池具有高能、轻便和无污染等优点。氢氧燃料电池有酸式和碱式两种,它们放电时的电池总反应式都为2H2+O2=2H2O。
①酸式氢氧燃料电池的电解质溶液是稀硫酸,其负极反应式为2H2-4e-=4H+,则其正极反应式为____ 。
②碱式氢氧燃料电池的电解质溶液是KOH溶液,则其负极反应式为___ 。
①干电池可以实现化学能向电能的转化和电能向化学能的转化
②锌锰干电池长时间连续使用时内装糊状物可能流出腐蚀电器
③充电电池可以无限制地反复放电、充电
④充电是使放电时的氧化还原反应逆向进行
(2)铅蓄电池中,正极材料为PbO2,负极材料为Pb,放电时其负极反应式为
(3)原电池在NaOH溶液介质中,铝为负极,其负极反应式为
(4)航天技术中使用的氢氧燃料电池具有高能、轻便和无污染等优点。氢氧燃料电池有酸式和碱式两种,它们放电时的电池总反应式都为2H2+O2=2H2O。
①酸式氢氧燃料电池的电解质溶液是稀硫酸,其负极反应式为2H2-4e-=4H+,则其正极反应式为
②碱式氢氧燃料电池的电解质溶液是KOH溶液,则其负极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氮及其化合物在化肥、医药、材料和国防工业中具有广泛应用。回答下列问题:
(1)自上个世纪德国建立了第一套合成氨装置,合成氨工业为解决人类温饱问题做出了极大贡献。写出实验室制备氨气的方程式_______________ 。
(2)有人设想寻求合适的催化剂和电极材料,以 、
、 为电极反应物,以HCl、
为电极反应物,以HCl、 为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型电池,如图所示。
为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型电池,如图所示。________ (选填“正极”、“负极”);该电池正极的电极反应式是________________ 。
(3)盐酸羟胺( )主要用作还原剂和定影剂,是一种易溶于水的盐。以
)主要用作还原剂和定影剂,是一种易溶于水的盐。以 、
、 、盐酸为原料通过电化学方法一步制备盐酸羟胺的装置示意图如下。
、盐酸为原料通过电化学方法一步制备盐酸羟胺的装置示意图如下。_____________________ 。
②该电池在工作过程中 的浓度变化为
的浓度变化为_______ (选填“增大”、“减小”、“不变”),假设放电过程中电解质溶液的体积不变,当右室溶液质量增加4.1g时,消耗 的物质的量为
的物质的量为_________ 。
(4) 电化学传感器是将环境中
电化学传感器是将环境中 浓度转变为电信号的装置,工作原理如图所示,其中YSZ是固体电解质,当传感器在一定温度下工作时,在熔融
浓度转变为电信号的装置,工作原理如图所示,其中YSZ是固体电解质,当传感器在一定温度下工作时,在熔融 和YSZ之间的界面X会生成固体
和YSZ之间的界面X会生成固体 。
。 向
向___________ (填正极或负极)。
②写出金属电极b发生的电极反应式:_______________________ 。
(1)自上个世纪德国建立了第一套合成氨装置,合成氨工业为解决人类温饱问题做出了极大贡献。写出实验室制备氨气的方程式
(2)有人设想寻求合适的催化剂和电极材料,以
 、
、 为电极反应物,以HCl、
为电极反应物,以HCl、 为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型电池,如图所示。
为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型电池,如图所示。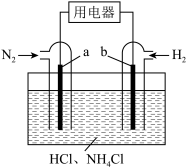
(3)盐酸羟胺(
 )主要用作还原剂和定影剂,是一种易溶于水的盐。以
)主要用作还原剂和定影剂,是一种易溶于水的盐。以 、
、 、盐酸为原料通过电化学方法一步制备盐酸羟胺的装置示意图如下。
、盐酸为原料通过电化学方法一步制备盐酸羟胺的装置示意图如下。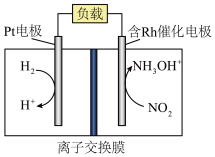
②该电池在工作过程中
 的浓度变化为
的浓度变化为 的物质的量为
的物质的量为(4)
 电化学传感器是将环境中
电化学传感器是将环境中 浓度转变为电信号的装置,工作原理如图所示,其中YSZ是固体电解质,当传感器在一定温度下工作时,在熔融
浓度转变为电信号的装置,工作原理如图所示,其中YSZ是固体电解质,当传感器在一定温度下工作时,在熔融 和YSZ之间的界面X会生成固体
和YSZ之间的界面X会生成固体 。
。
 向
向②写出金属电极b发生的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.被誉为改变未来世界的十大新科技之一的燃料电池。 右图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.
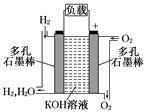
试回答下列问题:
(1)燃料电池的优点是________ ;电解质溶液中的OH -移向______ 极(填“负”或“正”).
(2)写出氢氧燃料电池工作时正极反应式:_______________________ 。
(3)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极反应式为___________ .
(4)利用该装置可以处理氮的氧化物和NH 3尾气,总反应为:6NO 2 +8NH 3=7N 2+12H 2O,负极反应式为__________ 。
II.将锌片和银片浸入稀硫酸中组成原电池,若该电池中两电极的总质量为80 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为41g,试计算:
(1)产生氢气的体积(标准状况)为________________ ;
(2)通过导线的电子数为__________ (用 N A表示).

试回答下列问题:
(1)燃料电池的优点是
(2)写出氢氧燃料电池工作时正极反应式:
(3)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极反应式为
(4)利用该装置可以处理氮的氧化物和NH 3尾气,总反应为:6NO 2 +8NH 3=7N 2+12H 2O,负极反应式为
II.将锌片和银片浸入稀硫酸中组成原电池,若该电池中两电极的总质量为80 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为41g,试计算:
(1)产生氢气的体积(标准状况)为
(2)通过导线的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】电化学研究的是化学现象与电现象之间的相互关系以及化学能与电能相互转化规律,要完成这样的电化学研究,需要涉及到原电池和电解池等电化学装置。
(1)铁是用途最广的金属材料之一,但生铁易生锈。某原电池装置如图所示,图中右侧烧杯中的电极反应式为___________ ,左侧烧杯中的c(Cl-)___________ (填“增大”、“减小”或“不变”)。
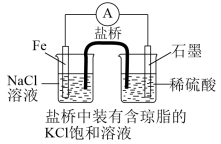
(2)用高铁酸盐设计的高铁电池是一种新型可充电电池,电解质溶液为KOH溶液,放电时的总反应为 。写出正极反应式:
。写出正极反应式:___________ 。
(3)为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一极通入空气,另一极通入甲醇气体,电解质是掺入了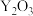 的
的 晶体,在高温下它能传导
晶体,在高温下它能传导 。电池工作时正极反应式为
。电池工作时正极反应式为___________ 。
(4)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是通电后将 氧化成
氧化成 ,然后以
,然后以 作氧化剂把水中的甲醇氧化成
作氧化剂把水中的甲醇氧化成 而净化。实验室用下图装置模拟上述过程。
而净化。实验室用下图装置模拟上述过程。
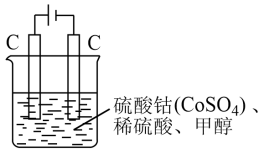
①写出阳极电极反应式:___________ 。
②除去甲醇反应为 ,该过程中被氧化的元素是
,该过程中被氧化的元素是___________ ,当产生标准状况下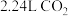 时,共转移电子
时,共转移电子___________ mol。
(1)铁是用途最广的金属材料之一,但生铁易生锈。某原电池装置如图所示,图中右侧烧杯中的电极反应式为

(2)用高铁酸盐设计的高铁电池是一种新型可充电电池,电解质溶液为KOH溶液,放电时的总反应为
 。写出正极反应式:
。写出正极反应式:(3)为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一极通入空气,另一极通入甲醇气体,电解质是掺入了
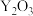 的
的 晶体,在高温下它能传导
晶体,在高温下它能传导 。电池工作时正极反应式为
。电池工作时正极反应式为(4)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是通电后将
 氧化成
氧化成 ,然后以
,然后以 作氧化剂把水中的甲醇氧化成
作氧化剂把水中的甲醇氧化成 而净化。实验室用下图装置模拟上述过程。
而净化。实验室用下图装置模拟上述过程。
①写出阳极电极反应式:
②除去甲醇反应为
 ,该过程中被氧化的元素是
,该过程中被氧化的元素是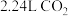 时,共转移电子
时,共转移电子
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
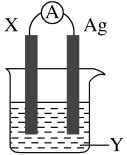
(1)电极X的材料是_______ ;电解质溶液Y是________ ;
(2)银电极上发生的电极反应式为___________________ ;
(3)外电路中的电子是从______ →______ ;
(4)当有1.6 g铜溶解时,银棒增重______ g 。

(1)电极X的材料是
(2)银电极上发生的电极反应式为
(3)外电路中的电子是从
(4)当有1.6 g铜溶解时,银棒增重
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按图所示装置进行实验,装置中电解质溶液为0.5mol·L-1的稀硫酸。
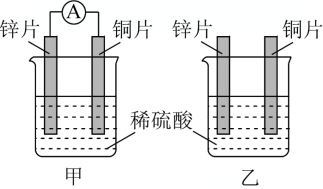
(1)对于甲乙装置,下列叙述正确的是_______ 。
(2)甲装置中SO 向
向_______ 极(填“正”或“负”)移动,正极的电极反应式为_______ 。
(3)若将甲装置中稀硫酸换成CuSO4溶液,一段时间后测得某电极增重12.8g,此时该电池反应共转移电子数为_______ 。

(1)对于甲乙装置,下列叙述正确的是
| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中铜片作正极,乙中铜片作负极 |
| C.两烧杯溶液中H+浓度均减小 |
| D.甲产生气泡的速率比乙慢 |
 向
向(3)若将甲装置中稀硫酸换成CuSO4溶液,一段时间后测得某电极增重12.8g,此时该电池反应共转移电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学反应中伴随着能量变化,请按要求回答下面的问题。
(1)下列反应中,生成物总能量大于反应物总能量的是______ (填序号)
①酸与碱的中和反应 ②碳酸氢钠和盐酸反应 ③镁和盐酸反应 ④碳与二氧化碳反应 ⑤ 晶体与
晶体与 混合搅拌
混合搅拌
(2)汽车发动机工作时会引发 和
和 反应,生成
反应,生成 等污染大气,如图是
等污染大气,如图是 和
和 反应生成
反应生成 的能量变化,则图中三种分子最稳定的是
的能量变化,则图中三种分子最稳定的是______ (写分子式)。若反应生成 气体,则
气体,则______ (填“吸收”或“放出”)______  的热量。
的热量。
根据实验现象回答:四种金属活泼性由强到弱的顺序是______ 。
(4)根据原电池原理可以制造化学电池。如:电动汽车上用的铅蓄电池,放电时的电池总反应为
该铅蓄电池负极材料是______ ,写出放电时正极的电极反应式______ 。
(5)为了验泟 与
与 氧化性强弱,下列装置能达到实验目的的是
氧化性强弱,下列装置能达到实验目的的是______ (写序号),写出其正极的电极反应式______ 。若开始时两极质量相等,当导线中通过 电子时,两个电极的质量差为
电子时,两个电极的质量差为______ 克。
(1)下列反应中,生成物总能量大于反应物总能量的是
①酸与碱的中和反应 ②碳酸氢钠和盐酸反应 ③镁和盐酸反应 ④碳与二氧化碳反应 ⑤
 晶体与
晶体与 混合搅拌
混合搅拌(2)汽车发动机工作时会引发
 和
和 反应,生成
反应,生成 等污染大气,如图是
等污染大气,如图是 和
和 反应生成
反应生成 的能量变化,则图中三种分子最稳定的是
的能量变化,则图中三种分子最稳定的是 气体,则
气体,则 的热量。
的热量。
| 装置 |
|
|
|
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(4)根据原电池原理可以制造化学电池。如:电动汽车上用的铅蓄电池,放电时的电池总反应为

该铅蓄电池负极材料是
(5)为了验泟
 与
与 氧化性强弱,下列装置能达到实验目的的是
氧化性强弱,下列装置能达到实验目的的是 电子时,两个电极的质量差为
电子时,两个电极的质量差为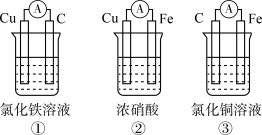
您最近一年使用:0次