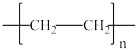(1)化学与生活关系密切。现有下列四种物质:
A. 青霉素 B. 亚硝酸钠 C. 维生素C D. 油脂
请根据题意,选择恰当的选项用字母代号填空。
①________ 是重要的体内能源;
②________ 广泛存在于新鲜水果和绿色蔬菜中,又称为抗坏血酸;
③________ 是最重要的抗生素,在注射之前,需要进行皮肤敏感试验;
④在腌制肉类食品时,可加入适量的________ 作防腐剂。
(2)保护环境、呵护地球已成为为类共同的呼声。
①水是一种宝贵的资源,保护水资源就是保护我们的生命。下列做法不利于水资源保护的是____ (填字母编号);
A.科学合理使用农药 B.任意排放化工厂废水 C.处理生活污水,达标排放
②矿泉水瓶不能随意丢弃。根据垃圾分类方法,矿泉水瓶属于_______ (填“可回收物”或“可堆肥垃圾”);
③在汽车尾气系统中安装催化转化器,可有效降低尾气中CO和NO等向向大气的排放,在催化转化器中,CO和NO发生反应。请完成该反应的化学主程式:2CO+2NO 2CO2+
2CO2+_______
(3)材料是人类赖以生存和发展的重要物质基础。
①有机高分子材料的出现是材料发展史上的一次重大突破。下列物质中含有有机高分子材料的是_____ ;
A. 普通水泥 B. 普通玻璃 C. 汽车轮胎
②生产和生活中,合金无处不在。我国最早使用的合金是_____ (填“铜合金”或“铝合金”);
③钢铁是目前用量最大、用途最广的金属材料,在潮湿空气中容易发生腐蚀。请写出钢铁发生电化学腐蚀的负极反应式_______________________________________ 。
A. 青霉素 B. 亚硝酸钠 C. 维生素C D. 油脂
请根据题意,选择恰当的选项用字母代号填空。
①
②
③
④在腌制肉类食品时,可加入适量的
(2)保护环境、呵护地球已成为为类共同的呼声。
①水是一种宝贵的资源,保护水资源就是保护我们的生命。下列做法不利于水资源保护的是
A.科学合理使用农药 B.任意排放化工厂废水 C.处理生活污水,达标排放
②矿泉水瓶不能随意丢弃。根据垃圾分类方法,矿泉水瓶属于
③在汽车尾气系统中安装催化转化器,可有效降低尾气中CO和NO等向向大气的排放,在催化转化器中,CO和NO发生反应。请完成该反应的化学主程式:2CO+2NO
 2CO2+
2CO2+(3)材料是人类赖以生存和发展的重要物质基础。
①有机高分子材料的出现是材料发展史上的一次重大突破。下列物质中含有有机高分子材料的是
A. 普通水泥 B. 普通玻璃 C. 汽车轮胎
②生产和生活中,合金无处不在。我国最早使用的合金是
③钢铁是目前用量最大、用途最广的金属材料,在潮湿空气中容易发生腐蚀。请写出钢铁发生电化学腐蚀的负极反应式
2013高二·湖南·学业考试 查看更多[1]
(已下线)2013年湖南省普通高中学业水平考试化学试题
更新时间:2020/03/09 22:22:14
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】研究金属腐蚀和防腐的原理很有现实意义,回答下列问题:
(1)某化学实验兴趣小组同学利用如图所示装置进行实验:___________ (填“析氢”或“吸氧”)腐蚀。
②实验进行一段时间后,在右侧小试管中,可观察到的现象为___________ 。
③在左侧大试管中,正极上发生反应的电极反应式为___________ 。
(2)实际生产中,可在铁的表面镀铜防止铁被腐蚀(如图所示):___________ (填“正极”或“负极”),判断的理由为___________ 。
②电镀时,Fe电极上发生反应的电极反应式为___________ 。
③电镀过程中,电解质溶液的pH将___________ (填“增大”、“减小”或“不变”)。
④电镀时,当电路中转移0.2mol电子时,此时两电极的质量差为_______ g(假设起始两电极的质量相等)。
(1)某化学实验兴趣小组同学利用如图所示装置进行实验:
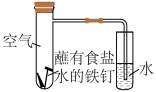
②实验进行一段时间后,在右侧小试管中,可观察到的现象为
③在左侧大试管中,正极上发生反应的电极反应式为
(2)实际生产中,可在铁的表面镀铜防止铁被腐蚀(如图所示):
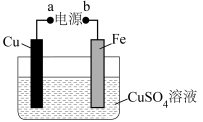
②电镀时,Fe电极上发生反应的电极反应式为
③电镀过程中,电解质溶液的pH将
④电镀时,当电路中转移0.2mol电子时,此时两电极的质量差为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】能源、资源问题是当前人类社会面临的一项重大课题。
(1)直接利用物质燃烧提供热能在当今社会仍然占很大比重,但存在利用率低的问题。CH4、H2、CO、CH3OH都是重要的能源物质,甲烷燃烧的化学方程式为:____ 。
(2)燃料电池将能量转化效率比直接燃烧效率高,如图为某种燃料电池的工作原理示意图,a、b均为惰性电极。
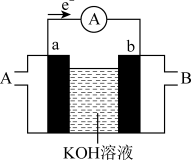
①使用时,空气从____ 口通入(填“A”或“B”);
②假设使用的“燃料”是甲醇,a极的电极反应式为:____ 。
(3)钢铁的腐蚀现象非常普遍,电化学腐蚀是造成钢铁腐蚀的主要原因,某同学按下图进行钢铁腐蚀的模拟,则正极的电极反应式为:____ ,当导线中有3.01×1023个电子流过,被腐蚀的铁元素为____ g。[ 提示:电化学的总反应式为2Fe+2H2O+O2=2Fe(OH)2]
(4)海水化学资源的开发利用具有重要的意义和作用,下图是海带中提取碘的示意图:

①中操作的名称是____ ;反应②的离子方程式是____ ,下述物质中不可做试剂③的是____ 。
A.乙醇 B.苯 C.乙酸 D.四氯化碳
(1)直接利用物质燃烧提供热能在当今社会仍然占很大比重,但存在利用率低的问题。CH4、H2、CO、CH3OH都是重要的能源物质,甲烷燃烧的化学方程式为:
(2)燃料电池将能量转化效率比直接燃烧效率高,如图为某种燃料电池的工作原理示意图,a、b均为惰性电极。

①使用时,空气从
②假设使用的“燃料”是甲醇,a极的电极反应式为:
(3)钢铁的腐蚀现象非常普遍,电化学腐蚀是造成钢铁腐蚀的主要原因,某同学按下图进行钢铁腐蚀的模拟,则正极的电极反应式为:

(4)海水化学资源的开发利用具有重要的意义和作用,下图是海带中提取碘的示意图:

①中操作的名称是
A.乙醇 B.苯 C.乙酸 D.四氯化碳
您最近一年使用:0次
【推荐3】利用NaCl溶液可以进行多种电化学实验或工业生产,完成下列题目。
Ⅰ:某同学在实验室中组装下列实验装置并进行实验探究。
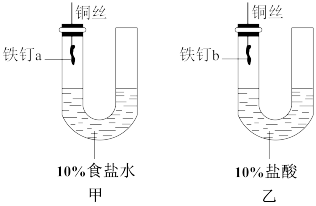
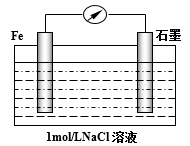
(1)该同学观察到甲装置中的液面变化情况为___________ 。反应过程中观察到乙装置中左边液面降低,右边液面升高,装置中发生原电池反应,正极的电极反应式为___________ 。
Ⅱ.工业上使用离子交换膜电解槽电解饱和食盐水生产氯气等重要化工产品。
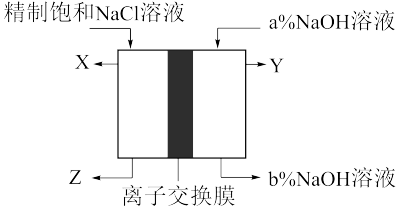
(2)电解槽左侧为___________ (填“阳极室”或“阴极室”)。
(3)写出电解饱和食盐水的总反应___________ 。
Ⅰ:某同学在实验室中组装下列实验装置并进行实验探究。

(1)该同学观察到甲装置中的液面变化情况为
Ⅱ.工业上使用离子交换膜电解槽电解饱和食盐水生产氯气等重要化工产品。

(2)电解槽左侧为
(3)写出电解饱和食盐水的总反应
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】化学在改善大气质量、污水处理和实现垃圾资源化等方面发挥了重要的作用。
① 家用燃料燃烧、烹调和吸烟会产生碳氧化物、氮氧化物、尼古丁等空气污染物,其中______________ 会使人对烟草成瘾;
② 污水处理的方法很多,从化学角度看,处理酸性废水可采用_______________ (选填“中合法”或“沉淀法”);
③ 下列方法符合垃圾资源化原则的是_________ (选填字母);
a.废旧塑料深埋地下 b.废旧轮胎露天焚烧 c.炼铁炉渣制水泥
④ 废旧电池必须回收处理的首要原因是________________________________ 。
① 家用燃料燃烧、烹调和吸烟会产生碳氧化物、氮氧化物、尼古丁等空气污染物,其中
② 污水处理的方法很多,从化学角度看,处理酸性废水可采用
③ 下列方法符合垃圾资源化原则的是
a.废旧塑料深埋地下 b.废旧轮胎露天焚烧 c.炼铁炉渣制水泥
④ 废旧电池必须回收处理的首要原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】水体污染的种类主要有_______ ,_______ ,_______ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】《化学与生活》模块试题
(1)我国农业因遭受酸雨而造成的损失每年高达15亿多元,酸雨是指pH小于________ 的雨水,这主要是由人为排放的_______ 和________ (填元素名称)的氧化物等酸性气体转化而成的。为治理酸雨的影响,可将CaCO3粉末撒到受酸雨影响的湖泊中,若用离子方程式表示该反应的本质,请完成如下离子反应:CaCO3+2H+==_____________________________ 。
(2)“民以食为天”,人类生命活动所需的各种营养物质主要来自食物。上表制定的食谱中,主食含有的基本营养物质主要是__________ ,副食含有的基本营养物质主要是_____________ ;豆浆所属的分散系为__________________ 。考虑营养成分的均衡搭配,应补充的配菜是__________________ 。
(3)水是一种宝贵的自然资源。
①生活污水中,经常包括含__________ 、___________ (填元素符号)的化合物,会造成水体植物营养物质污染。水中的氨在微生物的作用下,可被氧化成HNO2,进而氧化成HNO3,写出这一过程的化学方程式____________________________ 。
②氧化还原法是处理污水常用的方法。某地工厂排放的污水,经检测,污水中含有0.012 mol/L的游离溴,可用Na2SO3还原除去污水中的溴,请写出其化学方程式:___________________________ ;处理5 L这种污水,至少需加入0.05 mol/L的 Na2SO3 溶液________ L才能将溴全部除去。
(1)我国农业因遭受酸雨而造成的损失每年高达15亿多元,酸雨是指pH小于
| 主食 | 米饭 |
| 副食 | 红烧鱼 |
| 饮品 | 豆浆 |
| 配菜 | ? |
(2)“民以食为天”,人类生命活动所需的各种营养物质主要来自食物。上表制定的食谱中,主食含有的基本营养物质主要是
(3)水是一种宝贵的自然资源。
①生活污水中,经常包括含
②氧化还原法是处理污水常用的方法。某地工厂排放的污水,经检测,污水中含有0.012 mol/L的游离溴,可用Na2SO3还原除去污水中的溴,请写出其化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】回答下列问题。
(1)下表中是四种金属的熔、沸点数据:
①根据表中数据,归纳两种金属不能形成合金的有哪些组合?___________
②概括出能形成合金的两种金属应具备的条件。___________
(2)黄铜和金的颜色均为黄色,如何鉴别?___________
(1)下表中是四种金属的熔、沸点数据:
金属 | Na | Al | Cu | Fe |
熔点/℃ | 97.81 | 660 | 1 038 | 1 535 |
沸点/℃ | 883 | 2 467 | 2 567 | 2 750 |
②概括出能形成合金的两种金属应具备的条件。
(2)黄铜和金的颜色均为黄色,如何鉴别?
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】下图是部分金属和非金属材料发现和使用的时间简轴。请回答:
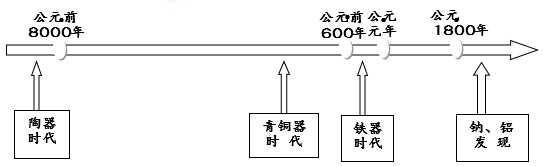
(1)我国最早使用的合金是_________ ;
(2)Cu、Fe、Na、Al四种金属元素中,金属性最强的是_______ (填元素符号);
Al的原子结构示意图是________________________ ;
(3)我国西汉时期就开始冶炼铜,古人有“曾青得铁则化为铜”的记载,是现代“湿法炼铜”的先驱,请写出上述反应的化学方程式:____________________________ ;
(4)19世纪初,钠和铝的发现得益于电解技术的应用。
冶炼铝的原料Al2O3属于_____ 氧化物(选填“酸性”、“碱性”或“两性”);冶炼铝的反应为:2 Al2O3(熔融) 4Al +3O2↑ ,反应中生成1molAl转移电子
4Al +3O2↑ ,反应中生成1molAl转移电子_________ mol。

(1)我国最早使用的合金是
(2)Cu、Fe、Na、Al四种金属元素中,金属性最强的是
Al的原子结构示意图是
(3)我国西汉时期就开始冶炼铜,古人有“曾青得铁则化为铜”的记载,是现代“湿法炼铜”的先驱,请写出上述反应的化学方程式:
(4)19世纪初,钠和铝的发现得益于电解技术的应用。
冶炼铝的原料Al2O3属于
 4Al +3O2↑ ,反应中生成1molAl转移电子
4Al +3O2↑ ,反应中生成1molAl转移电子
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】(1)为了证明某NaCl样品中含有钠元素,可以采用的实验方法是利用__________ 反应,操作方法是使用带有铂丝的玻璃棒蘸取待测样品放到酒精灯上灼烧,观察火焰呈_________ 色。若再需检验某样品中是否含钾元素,则要先将该铂丝用________ 洗净后反复灼烧至无色再蘸取待测样品,此时观察火焰颜色需要透过_________________ 。
(2)合金具有很多优良性能,例如,合金的硬度一般_________ 组分金属,而熔点_______ 组分金属。铜的合金主要有__________ 、___________ 、白铜等。铁的合金之一----钢可分为__________ 和________ 两大类。
(2)合金具有很多优良性能,例如,合金的硬度一般
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】高分子材料在生产、生活中的应用极为广泛,已知高分子材料的相关知识如下。
(1)高分子材料结构示意图:
a、用于制备塑料薄膜
b、用于制备光学仪器
c、用于制备汽车轮胎
请从上述各项中选择出最恰当的选项,将其代号填入下表中。
(1)高分子材料结构示意图:

a、用于制备塑料薄膜
b、用于制备光学仪器
c、用于制备汽车轮胎
请从上述各项中选择出最恰当的选项,将其代号填入下表中。
| 项目 | 硫化 橡胶 |
|
|
| 结构 | |||
| 用途 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】阅读科技材料,回答下列问题
2022年2月20日,第二十四届冬奥会在北京胜利闭幕,本届冬奥会大量使用了高科技。
材料1:国家速滑馆“冰丝带”中神奇的二氧化碳跨临界直接制冰。该技术就是将气态二氧化碳通过加温加压形成超临界二氧化碳流体(超临界二氧化碳流体是 形成气态与液态交融在一起的流体),再对超临界二氧化碳进行降温降压达到-20℃至-15℃,再相变蒸发吸热完成制冷和制冰的过程。该技术碳排放趋近于零,且对大气臭氧层没有影响,是目前世界上最环保的制冰技术。
形成气态与液态交融在一起的流体),再对超临界二氧化碳进行降温降压达到-20℃至-15℃,再相变蒸发吸热完成制冷和制冰的过程。该技术碳排放趋近于零,且对大气臭氧层没有影响,是目前世界上最环保的制冰技术。
材料2:冬奥会服装中的“黑科技”。本次冬奥会颁奖礼仪服装的衣服内胆里特意添加了第二代石墨烯发热材料,石墨烯是从石墨中分离出来的一层或几层碳原子构成的石墨片,是目前世界上最薄、最坚硬的纳米材料,石墨烯导热系数非常高。穿着礼仪服装前进行充电,充电完成后,石墨烯发热服会产生一种由内而外的温暖。此外,比赛服装中的科技含量更高,例如速滑竞赛服中,含有弹性超强的橡胶材料,可以最大程度减少体力消耗。
(1)文中涉及的有机合成材料是_______ 。
(2)第二代石墨烯作为一种新材料,它_______ (选填“是”或“不是”)优良的导体,画出构成石墨烯的原子结构示意图_______ 。
(3)下列说法正确的是_______。
(4)二氧化碳跨临界直接制冰的优点_______ 。
2022年2月20日,第二十四届冬奥会在北京胜利闭幕,本届冬奥会大量使用了高科技。
材料1:国家速滑馆“冰丝带”中神奇的二氧化碳跨临界直接制冰。该技术就是将气态二氧化碳通过加温加压形成超临界二氧化碳流体(超临界二氧化碳流体是
 形成气态与液态交融在一起的流体),再对超临界二氧化碳进行降温降压达到-20℃至-15℃,再相变蒸发吸热完成制冷和制冰的过程。该技术碳排放趋近于零,且对大气臭氧层没有影响,是目前世界上最环保的制冰技术。
形成气态与液态交融在一起的流体),再对超临界二氧化碳进行降温降压达到-20℃至-15℃,再相变蒸发吸热完成制冷和制冰的过程。该技术碳排放趋近于零,且对大气臭氧层没有影响,是目前世界上最环保的制冰技术。材料2:冬奥会服装中的“黑科技”。本次冬奥会颁奖礼仪服装的衣服内胆里特意添加了第二代石墨烯发热材料,石墨烯是从石墨中分离出来的一层或几层碳原子构成的石墨片,是目前世界上最薄、最坚硬的纳米材料,石墨烯导热系数非常高。穿着礼仪服装前进行充电,充电完成后,石墨烯发热服会产生一种由内而外的温暖。此外,比赛服装中的科技含量更高,例如速滑竞赛服中,含有弹性超强的橡胶材料,可以最大程度减少体力消耗。
(1)文中涉及的有机合成材料是
(2)第二代石墨烯作为一种新材料,它
(3)下列说法正确的是_______。
| A.石墨烯在常温下化学性质非常稳定 |
| B.超临界:二氧化碳流体与普通二氧化碳化学性质不同 |
| C.超临界二氧化碳流体中分子之间没有间隔 |
| D.在一定条件下石墨烯可以还原氧化铜 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】材料是人类赖以生存与发展的重要物质基础,是时代进步的重要标志。
以下是生活中常见的物品:a.玻璃杯 b.废旧干电池c.废报纸d.尼龙绳 e.轮胎 f.铁锅
请用相应的字母 填空:
(1)用合成高分子材料中橡胶制作的是______ 。
(2)随意丢弃会对水体和土壤都造成污染的是_________ 。
(3)如图所示,物品c可投入________ (填“A”或“B”)标志的垃圾桶中______ 方法加以分离。
A. 萃取 B.渗析 C.过滤 D.蒸馏 E.蒸发 F.分液
以下是生活中常见的物品:a.玻璃杯 b.废旧干电池c.废报纸d.尼龙绳 e.轮胎 f.铁锅
请用相应的
(1)用合成高分子材料中橡胶制作的是
(2)随意丢弃会对水体和土壤都造成污染的是
(3)如图所示,物品c可投入

A. 萃取 B.渗析 C.过滤 D.蒸馏 E.蒸发 F.分液
您最近一年使用:0次