以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如图,下列说法不正确的是( )
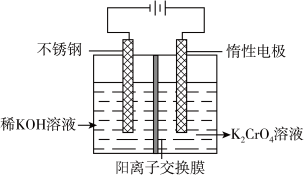

| A.在阴极室,发生的电极反应为:2H2O+2e-=2OH-+H2↑ |
B.在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2CrO42-+2H+ Cr2O72-+H2O向右移动 Cr2O72-+H2O向右移动 |
C.该制备过程总反应的化学方程式为:4K2CrO4+4H2O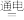 2K2Cr2O7+4KOH+2H2↑+O2↑ 2K2Cr2O7+4KOH+2H2↑+O2↑ |
| D.测定阳极液中K和Cr的含量,若K与Cr的物质的量之比为d,则此时铬酸钾的转化率为1-0.5d |
更新时间:2020-03-11 19:49:38
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列叙述中正确的是
| A.在原电池的负极和电解池的阴极上都发生失电子的氧化反应 |
| B.用情性电极电解饱和NaCl溶液,若有1mol电子转移,则生成1mol NaOH |
C.用情性电极电解 溶液,阴阳两极产物的物质的量之比为1∶2 溶液,阴阳两极产物的物质的量之比为1∶2 |
| D.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法中正确的是
| A.加强对煤、石油、天然气等综合利用的研究,可提高燃料的利用率 |
| B.电解水生成H2利O2的实验中,可加入少量盐酸或硫酸增强导电性 |
| C.同一可逆反应使用不同的催化剂时,高效催化剂可增大平衡转化率 |
| D.升高温度能使吸热反应速率加快,使放热反应速率减慢 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】室温下,用惰性电极电解下列物质的稀溶液,其中pH增大的是
| A.NaOH | B. | C. | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】如图,甲池的总反应为2CH3OH+3O2+4KOH=2K2CO3+6H2O。下列说法不正确的是
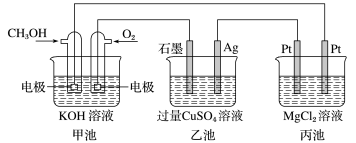

| A.甲池中每消耗2mol CH3OH,电解液中通过12mol电子 |
| B.反应一段时间后,向乙池中加入一定量CuO固体能使CuSO4溶液恢复原浓度 |
| C.反应一段时间后,丙池中会产生白色沉淀且不会溶解 |
| D.反应一段时间后,甲、乙两池pH均减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】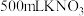 和
和 的混合溶液中
的混合溶液中 ,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到
,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到 气体(标准状况),假定电解后溶液体积仍为
气体(标准状况),假定电解后溶液体积仍为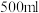 ,下列说法错误的是
,下列说法错误的是
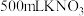 和
和 的混合溶液中
的混合溶液中 ,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到
,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到 气体(标准状况),假定电解后溶液体积仍为
气体(标准状况),假定电解后溶液体积仍为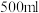 ,下列说法错误的是
,下列说法错误的是| A.原混合溶液中c(K+)为2 mol·L-1 |
| B.上述电解过程中共转移4 mol电子 |
| C.电解后溶液中c(H+)为2 mol·L-1 |
| D.混合溶液中c(Cu2+)为2 mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】乙醛酸是一种重要的化工中间体,可以用如下图所示的电化学装置合成。图中的双极膜中间层中的 解离为
解离为 和
和 ,并在直流电场作用下分别向两极迁移。下列说法正确的是
,并在直流电场作用下分别向两极迁移。下列说法正确的是

 解离为
解离为 和
和 ,并在直流电场作用下分别向两极迁移。下列说法正确的是
,并在直流电场作用下分别向两极迁移。下列说法正确的是
A.双极膜中间层中的 在外电场作用下向石墨电极方向迁移 在外电场作用下向石墨电极方向迁移 |
| B.KBr在上述电化学合成过程中只起电解质的作用 |
C.铅电极上的反应式为: |
| D.理论上外电路中迁移了2mol电子时,制得2mol乙醛酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
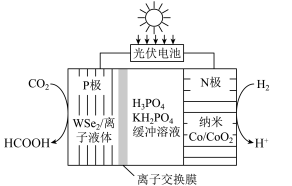
【推荐1】我国科研工作者通过研发新型催化剂,利用太阳能电池将工业排放的 转化为
转化为 ,实现碳中和目标,原理如图所示。下列说法正确的是
,实现碳中和目标,原理如图所示。下列说法正确的是
 转化为
转化为 ,实现碳中和目标,原理如图所示。下列说法正确的是
,实现碳中和目标,原理如图所示。下列说法正确的是
| A.该过程中存在的能量转化形式只有太阳能→化学能 |
| B.离子交换膜为阴离子交换膜 |
C.P极的电极反应式为: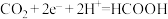 |
D.N极催化转化 时,P极生成 时,P极生成 的质量为 的质量为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】将亚磷酸氢二钠(Na2HPO3)溶液通过电渗析法来制备亚磷酸(H3PO3)的原理如图所示,下列有关说法错误的是


| A.阳极的电极反应式为2H2O-4e-=4H++O2↑ |
| B.在原料室与产品室间设计缓冲室的主要目的是提高产品的纯度 |
| C.阴极的电极反应式为2H2O+2e-=2OH-+H2↑ |
| D.膜①、③、④均为阳离子交换膜 |
您最近一年使用:0次



 )是生产新型聚酰胺产品的重要原料。利用双极膜(BPM,在直流电场的作用下,双极膜复合层间的
)是生产新型聚酰胺产品的重要原料。利用双极膜(BPM,在直流电场的作用下,双极膜复合层间的 和
和 )转换为1,5-戊二胺,实现无害化提取,工作原理如图所示。下列说法错误的是
)转换为1,5-戊二胺,实现无害化提取,工作原理如图所示。下列说法错误的是
 为阳极,
为阳极, 为阴极
为阴极 膜
膜 +2OH-=
+2OH-= +2H2O
+2H2O 硫酸
硫酸


