锂因其重要的用途,被誉为“能源金属”和“推动世界前进的金属”.
(1)Li3N可由Li在N2中燃烧制得.取4.164g 锂在N2中燃烧,理论上生成Li3N__ g;因部分金属Li没有反应,实际反应后固体质量变为6.840g,则固体中Li3N的质量是__ g(保留三位小数,Li3N的式量:34.82)
(2)已知:Li3N+3H2O→3LiOH+NH3↑.取17.41g纯净Li3N,加入100g水,充分搅拌,完全反应后,冷却到20℃,产生的NH3折算成标准状况下的体积是__ L.过滤沉淀、洗涤、晾干,得到LiOH固体26.56g,计算20℃时LiOH的溶解度__ .(保留1位小数,LiOH的式量:23.94)
锂离子电池中常用的LiCoO2,工业上可由碳酸锂与碱式碳酸钴制备.
(3)将含0.5molCoCl2的溶液与含0.5molNa2CO3的溶液混合,充分反应后得到碱式碳酸钴沉淀53.50g;过滤,向滤液中加入足量HNO3酸化的AgNO3溶液,得到白色沉淀143.50g,经测定溶液中的阳离子只有Na+,且Na+有1mol;反应中产生的气体被足量NaOH溶液完全吸收,使NaOH溶液增重13.20g,通过计算确定该碱式碳酸钴的化学式__ ,写出制备碱式碳酸钴反应的化学方程式__ .
(4)Co2(OH)2CO3和Li2CO3在空气中保持温度为600~800℃,可制得LiCoO2,已知: 3Co2(OH)2CO3+O2→2Co3O4+3H2O+3CO2;4Co3O4+6Li2CO3+O2→12LiCoO2+6CO2
按钴和锂的原子比1:1混合固体,空气过量70%,800℃时充分反应,计算产物气体中CO2的体积分数__ .(保留三位小数,已知空气组成:N2体积分数0.79,O2体积分数0.21)
(1)Li3N可由Li在N2中燃烧制得.取4.164g 锂在N2中燃烧,理论上生成Li3N
(2)已知:Li3N+3H2O→3LiOH+NH3↑.取17.41g纯净Li3N,加入100g水,充分搅拌,完全反应后,冷却到20℃,产生的NH3折算成标准状况下的体积是
锂离子电池中常用的LiCoO2,工业上可由碳酸锂与碱式碳酸钴制备.
(3)将含0.5molCoCl2的溶液与含0.5molNa2CO3的溶液混合,充分反应后得到碱式碳酸钴沉淀53.50g;过滤,向滤液中加入足量HNO3酸化的AgNO3溶液,得到白色沉淀143.50g,经测定溶液中的阳离子只有Na+,且Na+有1mol;反应中产生的气体被足量NaOH溶液完全吸收,使NaOH溶液增重13.20g,通过计算确定该碱式碳酸钴的化学式
(4)Co2(OH)2CO3和Li2CO3在空气中保持温度为600~800℃,可制得LiCoO2,已知: 3Co2(OH)2CO3+O2→2Co3O4+3H2O+3CO2;4Co3O4+6Li2CO3+O2→12LiCoO2+6CO2
按钴和锂的原子比1:1混合固体,空气过量70%,800℃时充分反应,计算产物气体中CO2的体积分数
更新时间:2020-03-22 09:50:41
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】现有某温度下饱和NaCl溶液VmL,密度为ρg•cm-3,物质的量浓度为Cmol•L-1则该温度下NaCl的溶解度为___________ (用V、ρ、C表示)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某固态混合物中含有mgKNO3和若干不溶于水的杂质,将此混合物加入ng水中,在10℃、40℃、75℃时观察,充分溶解后的结果如下(溶解度曲线如图所示):
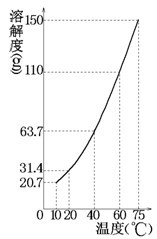
通过计算回答:
(1)m的值为____________ ,n的值为____________ ;
(2)75℃时所得溶液____________ (填“是”或“否”)饱和?
(3)在____________ 温度将mg硝酸钾溶于ng水中恰好达到饱和状态?
| 温度 | 10℃ | 40℃ | 75℃ |
| 未溶固体 | 261 g | 175 g | 82 g |

通过计算回答:
(1)m的值为
(2)75℃时所得溶液
(3)在
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压放电管来制取臭氧:
(1)在一定条件下,有aL氧气和臭氧的混合气体,当其中的臭氧完全转化为氧气,体积变为1.2aL,原混合气体中氧气的质量分数为 。
(2)若在标况下,在臭氧发生器中装入100mL氧气,最后体积为95mL。最终状态时混合气体的密度是 g/L。(保留一位小数)
(3)实验室将氧气和臭氧的混合气体0.896L(标准状况)通入盛有20.0g铜粉的反应器中,充分加热后,粉末的质量变为21.6g。原混合气中臭氧的体积分数为__________________。

(1)在一定条件下,有aL氧气和臭氧的混合气体,当其中的臭氧完全转化为氧气,体积变为1.2aL,原混合气体中氧气的质量分数为 。
(2)若在标况下,在臭氧发生器中装入100mL氧气,最后体积为95mL。最终状态时混合气体的密度是 g/L。(保留一位小数)
(3)实验室将氧气和臭氧的混合气体0.896L(标准状况)通入盛有20.0g铜粉的反应器中,充分加热后,粉末的质量变为21.6g。原混合气中臭氧的体积分数为__________________。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】(1)在标准状况下,由CO和CO2组成的混合气体8.96L,质量是16g。此混合物中CO和CO2的物质的量之比是_____________ ,CO的体积分数是_____________ ,该混合气体对于氢气的相对密度为________ 。
(2) 1.12g金属铁跟某稀盐酸恰好完全反应,得到100mL溶液,试计算:
①生成的气体在标准状况下的体积是_________________
②反应后所得溶液中溶质的物质的量浓度是______________________
(2) 1.12g金属铁跟某稀盐酸恰好完全反应,得到100mL溶液,试计算:
①生成的气体在标准状况下的体积是
②反应后所得溶液中溶质的物质的量浓度是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】某氮肥NH4HCO3中混有少量的(NH4)2CO3,现采用下列方案测定该氮肥中(NH4)2CO3的质量分数:称取5.7 g上述样品与2.0 mol/L NaOH溶液混合,完全溶解后,低温加热使其充分反应(该温度下铵盐不分解),并使生成的氨气全部被硫酸吸收,测得氨气的质量与所用NaOH溶液体积的关系如图所示:

请回答下列问题:
(1)A点前样品与NaOH反应的离子方程式为______________________ 。
(2)为使生成的氨气被硫酸吸收时不发生倒吸,可以选用下列装置中的_________ (填编号)。
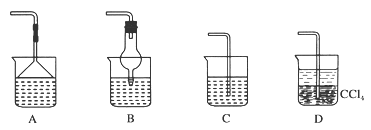
(3)样品中(NH4)2CO3的质量分数是________ %(保留一位小数)。
(4)当V[NaOH(aq)]=50 mL时,生成NH3的质量为________ 。

请回答下列问题:
(1)A点前样品与NaOH反应的离子方程式为
(2)为使生成的氨气被硫酸吸收时不发生倒吸,可以选用下列装置中的

(3)样品中(NH4)2CO3的质量分数是
(4)当V[NaOH(aq)]=50 mL时,生成NH3的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某赤铁矿石样品中含Fe2O380%,杂质中不含铁元素,某炼铁厂用这种赤铁矿石冶炼生铁,每天消耗这种赤铁矿石10000t,若生产过程中铁元素损失4%,则该厂年产(一年按360天计)生铁(含铁96%)的质量是___ (写出计算过程)。
您最近一年使用:0次




