 、
、 、
、 是三种处在不同短周期元素,原子序数依次减小,三种元素可组成化合物AxByCz,已知:
是三种处在不同短周期元素,原子序数依次减小,三种元素可组成化合物AxByCz,已知:(1)
 、
、 、
、 均为正整数且
均为正整数且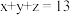 ;
;(2)
 该化合物与过量水反应生成
该化合物与过量水反应生成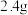 气体
气体 ,同时生成
,同时生成 的白色沉淀
的白色沉淀 ,
, 既能溶于盐酸又能溶于氢氧化钠溶液;
既能溶于盐酸又能溶于氢氧化钠溶液;(3)同温同压下
 由
由 、
、 组成的气体
组成的气体 完全燃烧时,需要
完全燃烧时,需要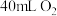 ,燃烧产物是
,燃烧产物是 和
和 。由此可知:三种元素分别是
。由此可知:三种元素分别是


 的电子式为
的电子式为
14-15高二上·上海杨浦·期末 查看更多[1]
(已下线)上海市控江中学2015-2016学年高二上学期期末考试化学试题
更新时间:2020-03-24 14:12:15
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】五种短周期元素甲、乙、丙、丁、戊的原子序数依次增大,甲和丙同族,乙离子和丙离子具有相同的电子层结构。甲和乙、丁、戊均能形成共价型化合物。甲和乙形成的化合物在水中呈碱性,单质丁在单质戊中可燃烧产生白色烟雾。回答下列问题:
(1)由甲和乙、丁、戊所形成的共价型化合物中,热稳定性最差的是_______ (用化学式表示);
(2)除乙外,上述元素的电负性从大到小依次为_______ (填元素符号);
(3)单质戊与水反应的离子方程式为_______ ;
(4)一定条件下1.86g单质丁与2.912L单质戊(标准状况)反应, 则产物为_______ (用化学式表示),其物质的量之比为_______ 。
(1)由甲和乙、丁、戊所形成的共价型化合物中,热稳定性最差的是
(2)除乙外,上述元素的电负性从大到小依次为
(3)单质戊与水反应的离子方程式为
(4)一定条件下1.86g单质丁与2.912L单质戊(标准状况)反应, 则产物为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子最外层共有10个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素符号:A__________ ,B___________ ;
(2)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:__________ ;
(3)写出A与氧元素形成的原子个数比为1:1的化合物的电子式__________ ;
(4)C、D、E的最高价氧化物水化物的酸性由强到弱的顺序(用化学式表示):________ ;
(5)A、B、D、E形成的简单离子的半径由大到小的顺序(用离子符号表示):_________ ;
(6)A的最高价氧化物的水化物中含有的化学键类型(填离子键、极性键、非极性键)_______ 。
(1)写出下列元素符号:A
(2)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:
(3)写出A与氧元素形成的原子个数比为1:1的化合物的电子式
(4)C、D、E的最高价氧化物水化物的酸性由强到弱的顺序(用化学式表示):
(5)A、B、D、E形成的简单离子的半径由大到小的顺序(用离子符号表示):
(6)A的最高价氧化物的水化物中含有的化学键类型(填离子键、极性键、非极性键)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下表列出了10种元素在周期表中的位置。用化学符号回答下列问题:
(1)10种元素中,第一电离能最大的是_______ ,电负性最小的金属元素是_______ 。
(2)①③⑥三种元素最高价氧化物对应的水化物中,碱性最强的是_______ 。
(3)②③④三种元素形成的简单离子,离子半径由大到小的顺序是_______ 。
(4)①和⑨的最高价氧化物对应的水化物的化学式分别为_______ 、_______ 。
(5)①和⑥的最高价氧化物对应的水化物相互反应的离子方程式为_______ 。
(6)用电子式表示第三周期主族元素中电负性最小的元素和电负性最大的元素形成化合物的过程:_______ 。
(7)⑨元素原子的价电子的轨道表示式为_______ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 第2周期 | ⑤ | ⑦ | ||||||
| 第3周期 | ① | ③ | ⑥ | ⑧ | ⑩ | |||
| 第4周期 | ② | ④ | ⑨ |
(2)①③⑥三种元素最高价氧化物对应的水化物中,碱性最强的是
(3)②③④三种元素形成的简单离子,离子半径由大到小的顺序是
(4)①和⑨的最高价氧化物对应的水化物的化学式分别为
(5)①和⑥的最高价氧化物对应的水化物相互反应的离子方程式为
(6)用电子式表示第三周期主族元素中电负性最小的元素和电负性最大的元素形成化合物的过程:
(7)⑨元素原子的价电子的轨道表示式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】有A、B、C、D、E五种短周期主族元素,其元素特征信息如下表:
请回答下列问题:
(1) 写出A、B、C三种元素形成的化合物的化学式为_____________ 。
(2) B、C、D的简单离子半径由大到小的顺序是(用离子符号表示)_______________ 。
(3)写出电解CE溶液的化学方程式:
_______________________________________________________ 。
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带有两个单位的负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子具有相同的电子层结构,且核电荷数与B相差3 |
| D | 与C同周期,且最外层电子是C的3倍 |
| E | 与D同周期,原子半径在该周期中最小 |
请回答下列问题:
(1) 写出A、B、C三种元素形成的化合物的化学式为
(2) B、C、D的简单离子半径由大到小的顺序是(用离子符号表示)
(3)写出电解CE溶液的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】R、W、X、Y、M是原子序数依次增大的五种主族元素。R最常见同位素的原子核中不含中子。W与X可形成两种稳定的化合物:WX和WX2。工业革命以来,人类使用的化石燃料在燃烧过程中将大量WX2排入大气,在一定程度导致地球表面平均温度升高。Y与X是同一主族的元素,且在元素周期表中与X相邻。
(1)W的原子结构示意图是__________________________ 。
(2)WX2的电子式是_______________________ 。
(3)R2X、R2Y中,稳定性较高的是____ (填化学式),请从原子结构的角度解释其原因:_____ 。
(4)Se与Y是同一主族的元素,且在元素周期表中与Y相邻。
①根据元素周期律,下列推断正确的是________ (填字母序号)。
a.Se的最高正化合价为+7价
b.H2Se的还原性比H2Y强
c.H2SeO3的酸性比H2YO4强
d.SeO2在一定条件下可与NaOH溶液反应
②室温下向SeO2固体表面吹入NH3,可得到两种单质和H2O,该反应的化学方程式为_____________ 。
(5)科研人员从矿石中分离出一种氧化物,化学式可表示为M2O3。为确定M元素的种类,进行了一系列实验,结果如下:
①M的相对原子质量介于K和Rb(铷)之间;
②0.01 mol M2O3在碱性溶液中与Zn充分反应可得到M的简单氢化物,反应完全时,被M2O3氧化的Zn为0.06 mol;
综合以上信息推断,M可能位于元素周期表第_________________ 族。
(1)W的原子结构示意图是
(2)WX2的电子式是
(3)R2X、R2Y中,稳定性较高的是
(4)Se与Y是同一主族的元素,且在元素周期表中与Y相邻。
①根据元素周期律,下列推断正确的是
a.Se的最高正化合价为+7价
b.H2Se的还原性比H2Y强
c.H2SeO3的酸性比H2YO4强
d.SeO2在一定条件下可与NaOH溶液反应
②室温下向SeO2固体表面吹入NH3,可得到两种单质和H2O,该反应的化学方程式为
(5)科研人员从矿石中分离出一种氧化物,化学式可表示为M2O3。为确定M元素的种类,进行了一系列实验,结果如下:
①M的相对原子质量介于K和Rb(铷)之间;
②0.01 mol M2O3在碱性溶液中与Zn充分反应可得到M的简单氢化物,反应完全时,被M2O3氧化的Zn为0.06 mol;
综合以上信息推断,M可能位于元素周期表第
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E五种元素,已知:
①A原子的最外层电子数是次外层电子数的两倍,B的阴离子与C的阳离子跟氖原子的电子层结构相同,E原子的最外层上的电子数比最内层多5。
②常温下B2是气体,它的相对分子质量是氢气的16倍。
③C的单质在B2中燃烧,生成淡黄色固体F,F与AB2反应可生成B2。
④D的单质在B2中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体DB2,D在DB2中的含量为50%。根据以上情况回答:
(1)E位于第___ 周期___ 族;
(2)C的离子结构示意图是_____ ,F中的化学键为______ ;
(3)AB2的电子式为___ ; F和AB2反应的化学方程式为_______ ;
(4)C、D、E三种元素的原子半径从小到大的顺序为___ ; (用元素符号回答)
(5)常温下,E的单质与C的最高价氧化物对应水化物的水溶液反应的离子方程式为__________ 。
①A原子的最外层电子数是次外层电子数的两倍,B的阴离子与C的阳离子跟氖原子的电子层结构相同,E原子的最外层上的电子数比最内层多5。
②常温下B2是气体,它的相对分子质量是氢气的16倍。
③C的单质在B2中燃烧,生成淡黄色固体F,F与AB2反应可生成B2。
④D的单质在B2中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体DB2,D在DB2中的含量为50%。根据以上情况回答:
(1)E位于第
(2)C的离子结构示意图是
(3)AB2的电子式为
(4)C、D、E三种元素的原子半径从小到大的顺序为
(5)常温下,E的单质与C的最高价氧化物对应水化物的水溶液反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】氯化铁是常见的水处理剂,无水FeCl3 的熔点为282℃,沸点为315℃。工业上制备无水FeCl3 的一种工艺流程如下:

(1)氯化铁的净水原理和最常用的____________________ (写出结晶水合物的化学式)净水原理相同。
(2)捕集器中温度超过400℃时,捕集到另一种物质,其相对分子质量为325,该物质的分子式为________ 。
(3)吸收塔中反应的离子方程式是__________________ 。
(4)从副产物FeCl3 溶液中获得FeCl3·6H2O 的方法是在溶液中加入适量的浓盐酸,再进行___________ 、__________ 、过滤,洗涤、晾干。
(5)FeCl3的质量分数通常可用碘量法测定:称取m克无水氯化铁样品(不考虑杂质是否反应),溶于稀盐酸,再转移到100mL容量瓶,用蒸馏水定容;取出10mL,加入稍过量的KI溶液,充分反应后,滴入2-3滴淀粉溶液,当滴定终点时,用去cmol/L Na2S2O3溶液滴定用去VmL.
(已知:第一步反应2Fe3++2I—= I2+2Fe2+;第二步反应 I2+2S2O32-=2I-+S4O62-)
该实验确定样品中氯化铁的质量分数为_________________ 。

(1)氯化铁的净水原理和最常用的
(2)捕集器中温度超过400℃时,捕集到另一种物质,其相对分子质量为325,该物质的分子式为
(3)吸收塔中反应的离子方程式是
(4)从副产物FeCl3 溶液中获得FeCl3·6H2O 的方法是在溶液中加入适量的浓盐酸,再进行
(5)FeCl3的质量分数通常可用碘量法测定:称取m克无水氯化铁样品(不考虑杂质是否反应),溶于稀盐酸,再转移到100mL容量瓶,用蒸馏水定容;取出10mL,加入稍过量的KI溶液,充分反应后,滴入2-3滴淀粉溶液,当滴定终点时,用去cmol/L Na2S2O3溶液滴定用去VmL.
(已知:第一步反应2Fe3++2I—= I2+2Fe2+;第二步反应 I2+2S2O32-=2I-+S4O62-)
该实验确定样品中氯化铁的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】铁触媒(铁的氧化物)是硫酸工业的催化剂。某同学设计了以下两种方案研究铁触媒的组成。
方案一:用下列流程测定铁触媒的含铁量,确定其组成。
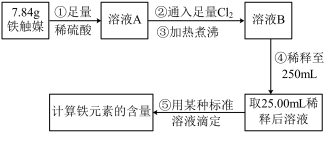
(1)步骤④中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和____________ 。
(2)若通入Cl2不足量,溶液B中还含有____________ ,会影响测定结果。
(3)若通入Cl2过量且加热煮沸不充分,溶液B中可能含有Cl2。请设计实验方案检验Cl2,完成下列实验报告。限选试剂:0.1 mol·L-1酸性KMnO4溶液、紫色石蕊试液、品红溶液、淀粉-KI溶液、0.1 mol·L-1 KSCN溶液。
方案二:用下列装置测定铁触媒的含铁量,确定其组成。
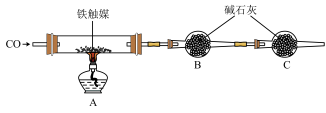
(4)干燥管C的作用是________________________ 。
(5)称取15.2 g铁触媒进行上述实验。充分反应后,测得干燥管B增重11.0 g,则该铁触媒的化学式可表示为________________________ 。
方案一:用下列流程测定铁触媒的含铁量,确定其组成。

(1)步骤④中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和
(2)若通入Cl2不足量,溶液B中还含有
(3)若通入Cl2过量且加热煮沸不充分,溶液B中可能含有Cl2。请设计实验方案检验Cl2,完成下列实验报告。限选试剂:0.1 mol·L-1酸性KMnO4溶液、紫色石蕊试液、品红溶液、淀粉-KI溶液、0.1 mol·L-1 KSCN溶液。
| 实验操作 | 预期现象与结论 |
方案二:用下列装置测定铁触媒的含铁量,确定其组成。
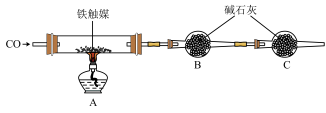
(4)干燥管C的作用是
(5)称取15.2 g铁触媒进行上述实验。充分反应后,测得干燥管B增重11.0 g,则该铁触媒的化学式可表示为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】为了除去KCl固体中少量的MgCl2、MgSO4,可选用Ba(OH)2、HCl和K2CO3三种试剂,按下图步骤操作:

(1)写出三种试剂的化学式:A________ ,B________ ,C________ 。
(2)①加入过量A的目的是______________ ,有关化学方程式为___________________ 。
②加入过量B的目的是______________ ,有关化学方程式为_________________ 。
③加热煮沸目的是_____________________________________________ 。
(3)操作Ⅰ是________ ,操作Ⅱ是________ 。

(1)写出三种试剂的化学式:A
(2)①加入过量A的目的是
②加入过量B的目的是
③加热煮沸目的是
(3)操作Ⅰ是
您最近一年使用:0次



