碱式碳酸铜的成分有多种,其化学式一般可表示为xCu(OH)2·yCuCO3。孔雀石呈绿色,是一种名贵的宝石,其主要成分是Cu(OH)2·CuCO3。某兴趣小组为探究制取孔雀石的最佳反应条件,设计了如下实验:
实验1:将2.0mL 0.50 mol/LCu(NO3)2溶液、2.0mL 0.50 mol/LNaOH溶液和0.25 mol/LNa2CO3溶液按表Ⅰ所示体积混合。
实验2:将合适比例的混合物在表Ⅱ所示温度下反应。
实验记录如下:
表I
表II
(1)实验室制取少许孔雀石,应该采用的最佳反应条件:①Cu(NO3)2溶液与Na2CO3溶液的体积比为________________ ;②反应温度是_______________ 。
(2)80℃时,所制得的孔雀石有少量褐色物质的原因是_____________ 。
实验1:将2.0mL 0.50 mol/LCu(NO3)2溶液、2.0mL 0.50 mol/LNaOH溶液和0.25 mol/LNa2CO3溶液按表Ⅰ所示体积混合。
实验2:将合适比例的混合物在表Ⅱ所示温度下反应。
实验记录如下:
表I
| 编号 | V(Na2CO3)/mL | 沉淀情况 |
| 1 | 2.8 | 多、蓝色 |
| 2 | 2.4 | 多、蓝色 |
| 3 | 2.0 | 较多、绿色 |
| 4 | 1.6 | 较少、绿色 |
| 编号 | 反应温度/℃ | 沉淀情况 |
| 1 | 40 | 多、蓝色 |
| 2 | 60 | 少、浅绿色 |
| 3 | 75 | 较多、绿色 |
| 4 | 80 | 较多、绿色(少量褐色) |
(2)80℃时,所制得的孔雀石有少量褐色物质的原因是
2013·上海闵行·一模 查看更多[1]
(已下线)上海市闵行区2013年高考一模化学试题
更新时间:2020-03-30 09:40:31
|
相似题推荐
解答题-无机推断题
|
容易
(0.94)
名校
【推荐1】铁、铝的混合物进行如下实验:

(1)操作X的名称是____________ ;
(2)气体A是____________ (填化学式);
(3)A与Cl2混合光照可能发生爆炸,生成_____________ (填化学式),A在该反应中作为_____________ (填“氧化剂”或“还原剂”);
(4)溶液B中阴离子除OH- 外还有____________________ (填离子符号),溶液D中存在的金属离子为__________________ (填离子符号);
(5)加入足量NaOH溶液时发生反应的离子方程式为:_______________ ;加入稀盐酸发生反应的离子方程式为: ________________________ ;
(6)向溶液D加入NaOH溶液,观察到产生的白色絮状沉淀迅速变为灰绿色,最终变为红褐色,请写出沉淀转化的化学方程式:________________________________________________ 。

(1)操作X的名称是
(2)气体A是
(3)A与Cl2混合光照可能发生爆炸,生成
(4)溶液B中阴离子除OH- 外还有
(5)加入足量NaOH溶液时发生反应的离子方程式为:
(6)向溶液D加入NaOH溶液,观察到产生的白色絮状沉淀迅速变为灰绿色,最终变为红褐色,请写出沉淀转化的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
容易
(0.94)
名校
解题方法
【推荐2】某研究小组利用含硫酸亚铁和硫酸铜的工业废料制备铁红 氧化铁
氧化铁 和硫酸铵晶体。流程如图:
和硫酸铵晶体。流程如图:
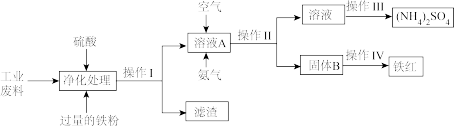
请回答下列问题:
(1)操作Ⅰ的名称是_____________ ,滤渣的成分为______________ 。
(2)简述下列实验操作:
①检验溶液A中金属阳离子的方法为__________________________ ;
②检验固体B是否被洗涤干净的方法是____________ 。
(3)测定废料中硫酸铜的质量分数:称取a g废料样品,将操作Ⅰ得到的滤渣用足量稀硫酸溶解、过滤、洗涤、干燥,称得固体质量为b g,则废料中硫酸铜的质量分数______________  写出含a、b的表达式
写出含a、b的表达式 。
。
 氧化铁
氧化铁 和硫酸铵晶体。流程如图:
和硫酸铵晶体。流程如图:
请回答下列问题:
(1)操作Ⅰ的名称是
(2)简述下列实验操作:
①检验溶液A中金属阳离子的方法为
②检验固体B是否被洗涤干净的方法是
(3)测定废料中硫酸铜的质量分数:称取a g废料样品,将操作Ⅰ得到的滤渣用足量稀硫酸溶解、过滤、洗涤、干燥,称得固体质量为b g,则废料中硫酸铜的质量分数
 写出含a、b的表达式
写出含a、b的表达式 。
。
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
【推荐3】已知硫铁矿的主要成分是FeS2(铁元素呈+2价,硫元素呈-1价)。以下是分析硫铁矿中FeS2含量的三种方法,各方法的操作流程图如下:
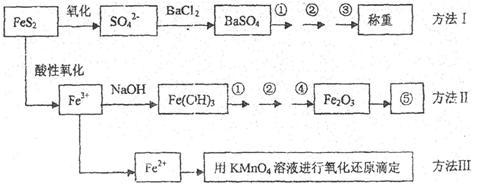
请回答下列问题:
(1)流程图中操作①、②、③分别指的是:①____________ 、②___________ 、③________ 。
操作④、⑤用到的主要仪器是:④_________ 、⑤__________ (每空填1~2个仪器)。
(2)判断溶液中SO42-离子已沉淀完全的方法是_______________________________ 。
(3)某同学用方法Ⅲ测定试样中Fe元素的含量,需要准确配制KMnO4标准溶液,下列因素导致所配制的溶液浓度偏大的有_______
A.砝码生锈 B.定容时俯视
C.称量时物质和砝码位置反了(需要游码) D.容量瓶用待装液润
(4)某同学采用方法Ⅱ分析矿石中的Fe含量,发现测定结果总是偏高,则产生误差的可能原因是______________________________________ 。
(5)称取矿石试样1.60g,按方法Ⅰ分析,称得BaSO4的质量为4.66g,假设矿石中的硫元素全部来自于FeS2,则该矿石中FeS2的质量分数是_________________________ 。

请回答下列问题:
(1)流程图中操作①、②、③分别指的是:①
操作④、⑤用到的主要仪器是:④
(2)判断溶液中SO42-离子已沉淀完全的方法是
(3)某同学用方法Ⅲ测定试样中Fe元素的含量,需要准确配制KMnO4标准溶液,下列因素导致所配制的溶液浓度偏大的有
A.砝码生锈 B.定容时俯视
C.称量时物质和砝码位置反了(需要游码) D.容量瓶用待装液润
(4)某同学采用方法Ⅱ分析矿石中的Fe含量,发现测定结果总是偏高,则产生误差的可能原因是
(5)称取矿石试样1.60g,按方法Ⅰ分析,称得BaSO4的质量为4.66g,假设矿石中的硫元素全部来自于FeS2,则该矿石中FeS2的质量分数是
您最近一年使用:0次
解答题-工业流程题
|
容易
(0.94)
名校
【推荐1】为充分利用资源,变废为宝,实验室里利用废铁屑制取硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]。某兴趣小组以废铁屑制得硫酸亚铁铵后,按下列流程制备二水合草酸亚铁(FeC2O4·2H2O),进一步制备高纯度还原铁粉。

已知:①硫酸亚铁铵晶体在空气中不易被氧化,易溶于水,不溶于乙醇。
②FeC2O4·2H2O难溶于水,150℃开始失结晶水;H2C2O4易溶于水,溶解度随温度升高而增大。
请回答下列问题:
(1)步骤②中,H2C2O4稍过量的主要原因是___________ 。
(2)为了提高步骤③得到的FeC2O4·2H2O的纯度,宜用___________ (填“热水”“冷水”或“无水乙醇”)洗涤,检验洗涤是否干净的操作是___________ 。
(3)实现步骤④必须用到的两种仪器是___________ 。
(供选仪器:a.烧杯;b.坩埚;c.蒸馏烧瓶;d.高温炉;e.表面皿;f.锥形瓶)
(4)为实现步骤⑤,不宜用碳粉还原Fe2O3,理由是___________ 。
(5)硫酸亚铁铵是重要的工业原料,几种物质的溶解性如表所示:
(注意:高于73.3℃,FeSO4·7H2O发生分解)
以铁屑(有油污)、硫酸、硫酸铵为原料,补充制取硫酸亚铁铵晶体的实验方案:将铁屑置于锥形瓶中,___________ 低温干燥。[实验中须使用的试剂:铁屑、1.0mol·L-1的Na2CO3溶液、蒸馏水、3.0mol·L-1的H2SO4溶液,饱和(NH4)2SO4溶液、无水乙醇]

已知:①硫酸亚铁铵晶体在空气中不易被氧化,易溶于水,不溶于乙醇。
②FeC2O4·2H2O难溶于水,150℃开始失结晶水;H2C2O4易溶于水,溶解度随温度升高而增大。
请回答下列问题:
(1)步骤②中,H2C2O4稍过量的主要原因是
(2)为了提高步骤③得到的FeC2O4·2H2O的纯度,宜用
(3)实现步骤④必须用到的两种仪器是
(供选仪器:a.烧杯;b.坩埚;c.蒸馏烧瓶;d.高温炉;e.表面皿;f.锥形瓶)
(4)为实现步骤⑤,不宜用碳粉还原Fe2O3,理由是
(5)硫酸亚铁铵是重要的工业原料,几种物质的溶解性如表所示:
| 温度/℃ 物质溶解度/g | 10 | 20 | 30 | 40 | 50 | 60 |
| (NH4)2SO4 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 91.9 |
| FeSO4·7H2O | 40.0 | 48.0 | 60.0 | 73.3 | — | — |
| (NH4)2Fe(SO4)2·6H2O | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
以铁屑(有油污)、硫酸、硫酸铵为原料,补充制取硫酸亚铁铵晶体的实验方案:将铁屑置于锥形瓶中,
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
【推荐2】某同学应用如下所示装置研究物质的性质。其中气体A的主要成分是氯气,还含有少量空气和水蒸气。请回答下列问题:

(1)浓硫酸的作用是_______________ 。
(2)B中观察到的实验现象是____________________ 。
(3)从物质性质方面来看,这样的实验设计还存在事故隐患,应如何处理,请画出装置图(填在上图内),用化学方程式表达原理_________________________________________ ;装置图:_____________________ 。

(1)浓硫酸的作用是
(2)B中观察到的实验现象是
(3)从物质性质方面来看,这样的实验设计还存在事故隐患,应如何处理,请画出装置图(填在上图内),用化学方程式表达原理
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
【推荐3】氯气在工业生产中有重要的用途。某课外活动小组利用下列化学反应在实验室中制备氯气,并进行有关氯气性质的研究。
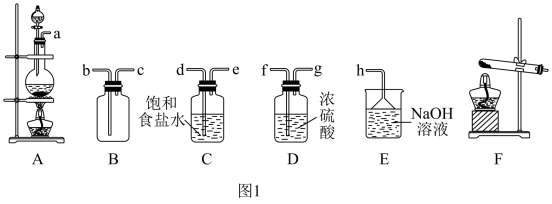
(1)该小组同学欲用图1所示仪器及试剂(不一定全用)制备并收集纯净、干燥的氯气。
①写出实验室制氯气的化学反应方程式:___________ ;浓盐酸起酸性作用和还原剂作用的质量之比为___________ 。
②选择装置,将各仪器按先后顺序连接起来,应该是a接___________,___________接___________,___________接___________,___________接h。(用导管口处的字母表示)___________
(2)E装置吸收氯气,可得漂白液的有效成分:___________ (填化学式);若将氯气通入冷的石灰乳中,可得漂白粉,写出反应方程式:___________ 。
(3)该小组同学设计并分别利用图2和图3所示装置探究氯气的氧化性,已知碘单质遇淀粉会变蓝。
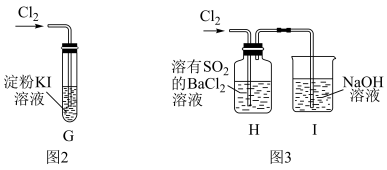
①G中的现象是___________ ,原因是___________ (用化学方程式表示)。
②H中的现象是___________ 。

(1)该小组同学欲用图1所示仪器及试剂(不一定全用)制备并收集纯净、干燥的氯气。
①写出实验室制氯气的化学反应方程式:
②选择装置,将各仪器按先后顺序连接起来,应该是a接___________,___________接___________,___________接___________,___________接h。(用导管口处的字母表示)
(2)E装置吸收氯气,可得漂白液的有效成分:
(3)该小组同学设计并分别利用图2和图3所示装置探究氯气的氧化性,已知碘单质遇淀粉会变蓝。

①G中的现象是
②H中的现象是
您最近一年使用:0次




