短周期主族元素X、Y、Z、W的原子序数依次增大,X原子核外最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,常温下0.01 mol∙L-1Z的最高价氧化物对应的水化物溶液的pH= 12,W在元素周期表中的族序数是周期数的2倍。下列说法正确的是
| A.W的单质的氧化性比Y的强 |
| B.原子半径:r(Z)>r(W)>r(Y)>r(X) |
| C.工业上常用电解法冶炼Z单质 |
| D.X的最高价氧化物对应的水化物的酸性比W强 |
更新时间:2020-04-04 09:00:39
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
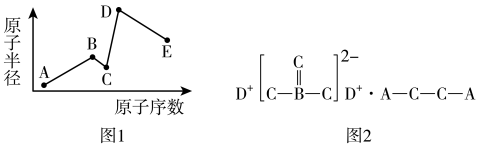
【推荐1】某种离子液体的阴离子结构如图,Q、W、X、Y、Z五种短周期元素的原子半径依次增大,基态Q原子的电子填充3个能级,有4对成对电子,Z与其他元素不在同一周期,下列说法正确的是
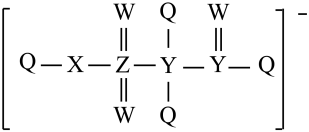
| A.最高价氧化物对应水化物的酸性:Q>X |
| B.Q、W、X的第一电离能依次减小 |
| C.氢化物的沸点:W>Y |
| D.X、Y、Z均至少有两种氧化物 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
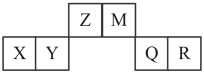
【推荐2】已知短周期元素X、Y、Z、M、Q和R在周期表中的相对位置如图所示,其中Y的最高化合价为 。下列说法错误的是
。下列说法错误的是
 。下列说法错误的是
。下列说法错误的是
| A.原于半径X>Y>Z>M |
| B.Z与R形成的化合物属于离子化合物 |
| C.Z的氢化物常温下可能为固体 |
| D.M最高价氧化物对应水化物能与其最低价氢化物反应 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】现有W、X、Y、Z均为短周期元素且原子序数依次增大,元素X和Z同族。盐YZW与浓盐酸反应,有黄绿色气体产生,此气体同冷烧碱溶液作用,可得到含YZW的溶液。下列错误的是( )
| A.X与Z具有相同的最高化合价 | B.X和Y形成的化合物的水溶液呈碱性 |
| C.Y的氢化物为离子化合物 | D.简单离子半径:Y<X<W |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
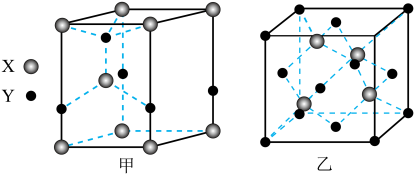
【推荐2】元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2;元素Y基态原子的3p轨道上有4个电子。元素Z的原子最外层电子数是其内层的3倍。X、Y形成的化合物晶体有两种常见的晶胞,如图所示。下列说法错误是

| A.Y元素位于周期表中第三周期第ⅥA族 |
B.由晶胞甲和晶胞乙推知该化合物的化学式为 |
C.元素电负性的关系是: |
D.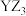 的空间结构为平面三角形 的空间结构为平面三角形 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】分别由短周期元素m、n、p、q组成的单质依次为甲、乙、丙、丁,有关反应关系如图所示(部分产物省略)。其中甲为黄绿色气体,M、N均为10电子分子且M的水溶液呈碱性,Q为离子化合物,下列说法中正确的是


| A.原子半径的大小:m>q>n>p |
| B.元素非金属性:q>p>n |
| C.n和p两元素形成的化合物可能组成离子化合物 |
| D.M和甲反应的另一个产物可能显碱性 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】有原子序数小于18的M1、M2、M3、M4四种元素。已知M1、M3最外层电子数相同,M2、M4电子层数相同。若M3的简单阴离子比M1的简单阴离子易失电子,M4的阳离子半径大于M2的阳离子半径,M3的阴离子比M2的阳离子多一个电子层。下列说法不正确的是
| A.最高价氧化物对应水化物的碱性M4>M2 | B.原子半径M4>M2>M3>M1 |
| C.气态氢化物的稳定性M3>M1 | D.原子序数M3>M2>M4>M1 |
您最近半年使用:0次

 甲的水溶液的
甲的水溶液的 。下列说法错误的是
。下列说法错误的是