浙江省杭州市西湖区2021-2022学年九年级9月月考科学试题
浙江
九年级
阶段练习
2021-09-28
406次
整体难度:
容易
考查范围:
物质的结构、物质的运动与相互作用、常见的物质、科学探究所需要的基本技能
一、选择题 添加题型下试题
| A.澄清石灰水 | B.液态氧 | C.干冰 | D.大理石 |
【知识点】 常见物质的分类
| A.KNO3和HCl | B.Mg(OH)2和稀H2SO4 | C.CaCO3和HCl | D.CaCl2和Na2CO3 |
【知识点】 复分解反应及其应用
| A.化学可以为人类研制新材料 | B.化学正在环境保护领域发挥重要作用 |
| C.化学可以为人类提供新能源 | D.化学的发展必然导致生态环境恶化 |
【知识点】 化学变化和物理变化的判别
| A.O2 | B.H2O | C.KClO3 | D.KMnO4 |
【知识点】 化学式
| A.+ 2价 | B.+5价 | C.+6价 | D.+7价 |
【知识点】 有关元素化合价的计算
| A.烧菜时,应先加含碘食盐 |
| B.碘酸钾中钾元素、碘元素、氧元素的质量比为1:1:3 |
| C.含碘食盐中含碘量越高越好 |
| D.碘酸钾中碘元素的质量分数为59.3% |
【知识点】 化学式 有关化学式的计算和推断
| A.白酒 | B.食醋 |
| C.氢氧化钠溶液 | D.碳酸钠溶液 |
| A.Cu、P2O5、、H2SO4 | B.Hg、CO2、HCl、 |
| C.C、CuO、Na2SO4 | D.Mg、H2O、HNO3 |
【知识点】 常见物质的分类
| A.氯化钠和碳酸钙 | B.氢氧化钠和硝酸钾 |
| C.氧化镁和氯化氢 | D.氧化钙和氢氧化钙 |
【知识点】 氧化物、酸、碱和盐的概念
| A.食盐 | B.纯碱 | C.铁钉 | D.石灰石 |
【知识点】 酸的化学性质
| A.NH4H2PO4 | B.NH4NO3 | C.CO(NH2)2 | D.K2SO4 |
【知识点】 盐与化肥
| A.CO2 | B.NH3 | C.H2 | D.HCl |
【知识点】 常见气体的检验与除杂方法 酸的化学性质 碱的化学性质
| A.硫酸铜溶液 | B.硝酸银溶液 | C.盐酸 | D.硝酸钠溶液 |
【知识点】 金属活动性顺序及其应用 酸的化学性质
| 选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
| A | MnO2(KCl) | 水 | 溶解、过滤、结晶 |
| B | CO2(CO) | 氧气 | 点燃 |
| C | Cu(CuO) | 稀盐酸 | 溶解、过滤、洗涤、干燥 |
| D | CuSO4(H2SO4) | 氢氧化钠溶液 | 过滤 |
| A.A | B.B | C.C | D.D |
【知识点】 物质除杂或净化
| A.硫酸铜、氯化镁、硝酸钾(石灰水) | B.氯化钠、硝酸银、碳酸钠(稀盐酸) |
| C.醋酸、纯碱、食盐(酚酞试液) | D.硫酸、硝酸钡、氯化钾(碳酸钠溶液) |
二、填空题 添加题型下试题

请回答下面问题:
(1)金属活动性顺序表中的X是
(2)把一根用砂纸打磨过的铝丝浸入硫酸铜溶液中,过了一会儿,观察到的现象有
【知识点】 金属活动性顺序及其应用
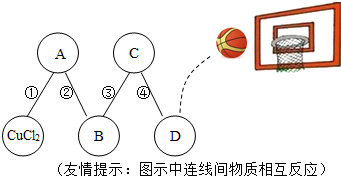
(1)已知D位置上投篮的“队员”是个灭火“能手”,则D位置“队员”代表的物质是
(2)B位置“队员”所代表的物质的一种用途是
(3)写出连线④代表的物质间发生反应的化学方程式
【知识点】 金属活动性顺序及其应用 碱的化学性质 物质的推断
| 加入NaOH溶液的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.0 | 7.0 | 11.0 | 12.2 |
(1)当加入氢氧化钠溶液的体积为
(2)当加入氢氧化钠溶液的体积为13mL时,溶液显
(3)当烧杯中溶液的pH=1.4时,溶液中的溶质有哪些?
【知识点】 中和反应及其应用 溶液的酸碱性与pH值的关系
 、
、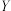 、
、 三种较活泼金属中,生民
三种较活泼金属中,生民 的质量与反应时间的关系如右图所示.这三种金属的活动性顺序为
的质量与反应时间的关系如右图所示.这三种金属的活动性顺序为 、
、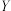 、
、 都是
都是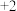 价金属,则相对原子质量由大到小的顺序为
价金属,则相对原子质量由大到小的顺序为
【知识点】 金属活动性顺序及其应用
三、解答题 添加题型下试题
①将固体混合物溶于水,得到无色、透明的溶液。
②取少量溶液加入少量氢氧化钡溶液,有白色沉淀生成。过滤,得到白色沉淀。
③在白色沉淀中加入足量稀硝酸,沉淀部分溶解。
由以上实验可知,该固体混合物中一定含有
【知识点】 盐的性质及用途 酸、碱、盐的鉴别 常见离子的检验方法及现象 常见物质的鉴定
四、填空题 添加题型下试题

(1)打开止水夹后观察到的现象是
(2)反应后将集气瓶中混合物过滤,所得溶液中CaCl2外,还存在的溶质有

(1)该气体一定不存在
(2)若实验中观察到
【知识点】 常见气体的检验与除杂方法 金属的冶炼
五、探究题 添加题型下试题

(1)写出此过程中生成沉淀的化学方程式
(2)在灼烧过程中,如果空气不充足和温度过高,会有部分沉淀物转化为BaS,这会使x的测定结果
| 实验序号 | 1 | 2 | 3 | 4 |
| 金属 | 丝状 | 粉末状 | 丝状 | 丝状 |
| 稀硫酸质量分数 | 5% | 5% | 10% | 10% |
| 溶液温度/℃ | 20 | 20 | 20 | 35 |
| 金属消失的时间/s | 500 | 50 | 125 | 50 |
分析上述数据,回答下列问题:
(1) 该实验需要用到的测量仪器除了天平、量筒之外还应该有
(2)小明是比较分析
(3)通过实验1和3,可得出的实验结论是
【知识点】 金属的化学性质 影响化学反应速率的因素
【提出问题】过氧化钠与水反应生成了什么物质?
【作出猜想】甲同学:生成氢氧化钠 乙同学:生成碳酸钠
丙同学:生成氢气 丁同学:生成氧气
(1)大家一致认为乙同学的推测不正确,理由是
【实验探究】
| 实验方法 | 实验现象 | 实验结论 |
| 用试管收集生成的气体,堵住试管口,移近酒精灯火焰,点燃 | 无现象 | 无氢气生成 |
| 用试管收集生成的气体,将带火星的木条伸入试管内 | (2) | 有氧气生成 |
| (3) | 溶液变红 | 溶液显碱性 |
【得出结论】
过氧化钠与水反应生成氢氧化钠和氧气。
【反思拓展】
(4)根据所学知识,请你预测将少量过氧化钠粉末加入硫酸铜溶液中的反应现象
【知识点】 碱的化学性质
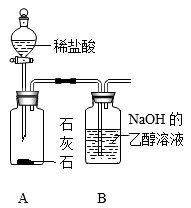
资料卡片:
①20℃时,碳酸钠在乙醇中几乎不溶解;
②氯化钙溶液呈中性;
(1)若装置 B 中溶液为饱和状态,反应一段时间后出现的现象是
(2)反应完成后同学们对装置 A 中所得溶液的溶质成分展开探究:
【提出问题】装置中A溶液的溶质是什么?
【猜想与假设】小滨认为溶质只有CaCl2;
小崔认为除 CaCl2外,可能还含有HCl;
【实验与结论】小滨取反应后装置 A 中部分溶液于试管中,滴加酚酞试液,发现溶液颜色呈无色,于是小滨认为自己的猜想是正确的;
【反思与评价】小崔认为小滨的实验方案是错误的,理由是
A.碳酸钠溶液 B.石蕊试液 C.锌粒来代替酚酞试液。
六、解答题 添加题型下试题
【知识点】 盐与化肥
七、填空题 添加题型下试题
(1)硅元素与锌元素之间最根本的区别是
(2)新型玻璃具有更好的延展性, 这属于物质的
(3)请列式计算咪唑钠(C3H3N2Na)中碳元素的质量分数。
【知识点】 化学性质与物理性质的差别及应用 元素的概念 有关元素化合价的计算
(1)早在西汉时期,我国就有湿法炼铜的记载,将铁置于硫酸铜溶液中得到铜单质,该反应属于
(2)玻璃是一种常见的非金属材料,
 是生产玻璃的原料之一。
是生产玻璃的原料之一。 属于
属于(3)未来,人类在生产材料时会更注重环境保护,将二氧化碳作为原料应用于“绿色”化学可以更好地保护环境。人类每年因能源消费而向大气排放的200亿吨的
 ,若这些
,若这些 按化学方程式“
按化学方程式“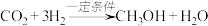 ”进行反应,理论上可以转化为
”进行反应,理论上可以转化为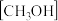 (结果保留一位小数)。
(结果保留一位小数)。
【知识点】 金属的化学性质 金属的冶炼 书写化学方程式、文字表达式 置换反应及其应用
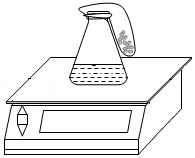
| 实验次数 | 1 | 2 | 3 |
| 碳酸钠质量/克 | 0.53 | 1.06 | 2.12 |
| 反应前装置总质量/克 | 66.33 | 66.86 | 67.92 |
| 反应后装置总质量/克 | 66.19 | 66.62 | 67.42 |
(1)计算第1次反应产生的二氧化碳质量。
(2)分析数据发现每次反应前后装置的总质量均不相等,请以第1次反应为例,通过计算说明该反应是否遵循质量守恒定律。(空气密度取1.3克/升,二氧化碳密度取2.0克/升,结果精确到0.01)
【知识点】 质量守恒定律及其应用 根据化学反应方程式的计算
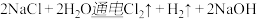 。某科学兴趣小组模拟氯碱工业,将一定浓度的氧化钠溶液通电一段时间(只发生上述反应),收集到0.02克
。某科学兴趣小组模拟氯碱工业,将一定浓度的氧化钠溶液通电一段时间(只发生上述反应),收集到0.02克 。停止通电,向所得溶液中加入10克盐酸后,将液恰好为中性。求:
。停止通电,向所得溶液中加入10克盐酸后,将液恰好为中性。求:(1)电解过程中消耗氯化钠的质量。
(2)所加盐酸中溶质的质量分数(用化学方程式计算)。
【知识点】 盐的性质及用途 质量守恒定律及其应用 根据化学反应方程式的计算
 溶液来测定,其它成分均不参与反应(
溶液来测定,其它成分均不参与反应(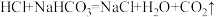 )
)(1)配制一定溶质质量分数的
 溶液,需要用到的玻璃仪器有烧杯、滴管和
溶液,需要用到的玻璃仪器有烧杯、滴管和(2)向锥形瓶中加入100克该品牌的洁厕灵,再逐次加入相同质量分数的
 溶液,测出每次锥形瓶中反应后溶液的总质量,数据记录如下:
溶液,测出每次锥形瓶中反应后溶液的总质量,数据记录如下:| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
加入 溶液的质量/g 溶液的质量/g | 40 | 40 | 40 | 40 | 40 |
| 反应后溶液的总质量/g | 138.9 | 177.8 | 216.7 | 255.6 | 295.6 |
试分析计算下列问题:
①第─次实验时,所加
 溶液中溶质质量是多少克?
溶液中溶质质量是多少克?②该品牌洁厕灵中HCl的质量分数是多少?
【知识点】 溶质质量分数的简单计算 根据化学反应方程式的计算
八、探究题 添加题型下试题
 关闭活塞,点燃燃烧匙内的红磷,立即塞紧瓶塞,待火焰熄灭后,过一段时间打开活塞,观察到集气瓶中的水位上升.待集气瓶内的水面不再上升时,集气瓶内的气体体积为
关闭活塞,点燃燃烧匙内的红磷,立即塞紧瓶塞,待火焰熄灭后,过一段时间打开活塞,观察到集气瓶中的水位上升.待集气瓶内的水面不再上升时,集气瓶内的气体体积为 然后向右边容器内加入一定量的水至两边水面再次相平,此时集气瓶内的气体体积为
然后向右边容器内加入一定量的水至两边水面再次相平,此时集气瓶内的气体体积为 在点燃红磷至打开活塞这一过程中,观察到数显设备显示集气瓶内的气体压强先上升后下降,再趋于稳定。
在点燃红磷至打开活塞这一过程中,观察到数显设备显示集气瓶内的气体压强先上升后下降,再趋于稳定。
(1)数显设备显示,开始一段时间集气瓶内气体压强上升,这是因为温度升高导致的气压变化量
(2)基于数显设备显示的气压变化,“过一段时间打开活塞”中的“一段时间”指的是火焰熄灭后到
(3)整个实验过程中,集气瓶中减少的氧气体积为
 ” 、“
” 、“ ”或“
”或“ ”)
”)
【知识点】 空气组成的测定
试卷分析
试卷题型(共 38题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 氧化物、酸、碱和盐的概念 | |
| 2 | 0.85 | 常见物质的分类 | |
| 3 | 0.85 | 复分解反应及其应用 | |
| 4 | 0.94 | 化学变化和物理变化的判别 | |
| 5 | 0.94 | 化学式 | |
| 6 | 0.85 | 有关元素化合价的计算 | |
| 7 | 0.65 | 化学式 有关化学式的计算和推断 | |
| 8 | 0.85 | 盐的性质及用途 酸、碱的使用注意事项 酸碱性对生命活动和农作物生长的影响 | |
| 9 | 0.65 | 碱的化学性质 中和反应及其应用 酸碱指示剂及其性质 | |
| 10 | 0.85 | 常见物质的分类 | |
| 11 | 0.94 | 盐与化肥 | |
| 12 | 0.65 | 酸的化学性质 盐的性质及用途 | |
| 13 | 0.85 | 氧化物、酸、碱和盐的概念 | |
| 14 | 0.65 | 盐的性质及用途 常见物质的鉴定 | |
| 15 | 0.85 | 酸的化学性质 | |
| 16 | 0.85 | 盐与化肥 | |
| 17 | 0.85 | 常见气体的检验与除杂方法 酸的化学性质 碱的化学性质 | |
| 18 | 0.65 | 金属活动性顺序及其应用 酸的化学性质 | |
| 19 | 0.65 | 物质除杂或净化 | |
| 20 | 0.65 | 酸、碱、盐的鉴别 酸碱指示剂及其性质 | |
| 二、填空题 | |||
| 21 | 0.65 | 金属活动性顺序及其应用 | |
| 22 | 0.65 | 金属活动性顺序及其应用 碱的化学性质 物质的推断 | |
| 23 | 0.65 | 中和反应及其应用 溶液的酸碱性与pH值的关系 | |
| 24 | 0.65 | 金属活动性顺序及其应用 | |
| 26 | 0.65 | 二氧化碳的化学性质 碱的化学性质 盐的性质及用途 | |
| 27 | 0.85 | 常见气体的检验与除杂方法 金属的冶炼 | |
| 33 | 0.65 | 化学性质与物理性质的差别及应用 元素的概念 有关元素化合价的计算 | |
| 34 | 0.65 | 金属的化学性质 金属的冶炼 书写化学方程式、文字表达式 置换反应及其应用 | |
| 35 | 0.65 | 质量守恒定律及其应用 根据化学反应方程式的计算 | |
| 36 | 0.65 | 盐的性质及用途 质量守恒定律及其应用 根据化学反应方程式的计算 | |
| 37 | 0.65 | 溶质质量分数的简单计算 根据化学反应方程式的计算 | |
| 三、解答题 | |||
| 25 | 0.4 | 盐的性质及用途 酸、碱、盐的鉴别 常见离子的检验方法及现象 常见物质的鉴定 | |
| 32 | 0.85 | 盐与化肥 | |
| 四、探究题 | |||
| 28 | 0.65 | 误差分析 盐的性质及用途 | |
| 29 | 0.85 | 金属的化学性质 影响化学反应速率的因素 | |
| 30 | 0.65 | 碱的化学性质 | |
| 31 | 0.85 | 酸的化学性质 酸碱指示剂及其性质 | |
| 38 | 0.85 | 空气组成的测定 | |



