浙江省台州市黄岩区黄岩实验中学2019年九年级上学期期中科学试题
浙江
九年级
期中
2020-09-30
44次
整体难度:
适中
考查范围:
科学探究所需要的基本技能、常见的物质、物质的运动与相互作用、物质的结构
一、选择题 添加题型下试题
A. 熄灭酒精灯 熄灭酒精灯 | B.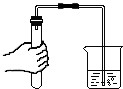 检查装置气密性 检查装置气密性 |
C.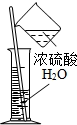 稀释浓硫酸 稀释浓硫酸 | D.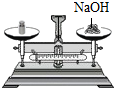 称量氢氧化钠固体 称量氢氧化钠固体 |
【知识点】 常见实验操作 碱的物理性质及用途 浓硫酸的性质及浓硫酸的稀释
| A.用稀盐酸除去金属表面的铁锈 |
| B.盐酸使指示剂变色 |
| C.用小木棍蘸少量浓硫酸,小木棍逐渐变为黑色 |
| D.浓盐酸在空气里敞口放置瓶口有白雾生成 |
【知识点】 化学变化和物理变化的判别

| A.铵态氮肥能与碱性物质混合施用 |
| B.NH4H2PO4属于复合肥 |
| C.从图中得知碳酸氢铵的化学性质是受热易分解 |
| D.当农作物出现倒伏症状时,说明缺钾 |

用所学化学知识判断,下列说法正确的是()
| A.“可燃空气”可以用排水集气法收集 | B.上述六种金属包括铜 |
| C.“可燃空气”是从金属中分解出来的 | D.上述反应属于复分解反应 |
【知识点】 金属活动性顺序及其应用 置换反应及其应用
| A.X一定是CuO | B.相对分子质量大小:X>Y |
| C.Y可能是Na2O | D.Y可能是NaCl |
【知识点】 碱的化学性质 质量守恒定律及其应用 复分解反应及其应用
| 酚酞溶液 | 铁锈 | 碳酸氢钠 | |
| 物质X | 无明显变化 | 溶液变为黄色 | 产生气泡 |
| A.Ca(OH)2 | B.CuSO4 | C.NaOH | D.HCl |
【知识点】 酸的化学性质
| A.加入酸化的AgNO3溶液,出现白色沉淀,说明有Cl−存在 |
| B.加入NaOH溶液,出现红褐色沉淀,说明有Fe3+存在 |
| C.加入Ca(OH)2并用湿润的蓝色石蕊试纸检验,试纸变红,说明有NH4+存在 |
| D.加入无色酚酞,溶液变红,说明有OH−存在 |
【知识点】 盐的性质及用途 常见离子的检验方法及现象
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |
【知识点】 化合反应及其应用 置换反应及其应用 复分解反应及其应用 识别化学反应基本类型
选项 | 混合物(括号内为杂质) | 除杂试剂 |
A | O2(SO2) | 适量的氢氧化钠溶液 |
B | NaCl溶液(Na2SO4) | 足量硝酸钡溶液 |
C | Cu粉(Fe) | 足量的稀硫酸 |
D | CuSO4溶液(H2SO4) | 足量的氧化铜粉末 |
| A.A | B.B | C.C | D.D |

| A.CO2 、Fe2O3 | B.Na2CO3 、NaCl | C.KOH、Ba(OH)2 | D.HNO3 、H2CO3 |
【知识点】 常见物质的分类
| A.FeCl3 NaCl Ba(OH)2 | B.KCl HCl NaNO3 |
| C.Na2SO4 HCl H2SO4 | D.CuCl2 NaNO3 K2SO4 |
【知识点】 酸、碱、盐的鉴别
| A.NaF的水解产物是NaOH和HF | B.CaO2的水解产物是Ca(OH)2和H2O2 |
| C.PCl3的水解产物之一是PH3 | D.Mg3N2水解产物是Mg(OH)2和NH3 |
【知识点】 复分解反应及其应用

| A.c 点对应溶液中含有的金属离子为 Zn2+和 Cu2+ |
| B.bc 段(不含两端点)析出的金属是 Fe |
| C.ab 段(不含两端点)对应溶液中含有的金属离子为Zn2+、Ag+、Cu2+、Fe2+ |
| D.若 bc 段和 cd 段中析出固体质量相等,参加反应的锌粉质量分别为m1和m2,m1>m2 |
【知识点】 金属活动性顺序及其应用 金属的化学性质
二、填空题 添加题型下试题
(1)农业上可用来改良酸性土壤的是
(2)稀盐酸和稀硫酸都可以用于金属除锈,是因为它们的溶液中都含有
(3)测定番茄汁的酸碱度可选用的是
A.酚酞试液 B.氨水 C.pH试纸 D.石蕊试液
【知识点】 酸的化学性质 碱的化学性质 溶液的酸碱性与pH值的关系
(1)维生素C所属的物质类别
(2)下列物质中能与维生素C反应的是
A.食盐 B.纯碱 C.硫酸钾 D.苛性钠
【知识点】 酸的化学性质 有机物与无机物的区别




