2016届浙江省乐清市育英学校普通班九年级上学期9月月考科学试卷
浙江
九年级
阶段练习
2015-10-21
213次
整体难度:
适中
考查范围:
常见的物质、物质的运动与相互作用、物质的结构、科学探究所需要的基本技能
一、选择题 添加题型下试题
| A.加热 | B.加入适量纯碱 | C.加入适量氯化钡 | D.加入适量明矾 |
【知识点】 盐的性质及用途
| A.酸都能电离出H+ | B.酸都含有酸根 |
| C.酸中都含有氢元素 | D.酸中都含有氧元素 |
【知识点】 酸的化学性质
 ,则该反应的类型属于( )
,则该反应的类型属于( )| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |
【知识点】 识别化学反应基本类型

| A.CO2 、Fe2O3 | B.Na2CO3 、NaCl | C.KOH、Ba(OH)2 | D.HNO3 、H2CO3 |
【知识点】 常见物质的分类
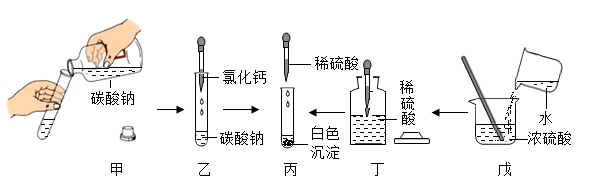
| A.甲中试剂瓶标签正对手心,是为了防止手被腐蚀 |
| B.乙中将滴管伸入试管内,是为了防止试剂滴落到试管外 |
| C.丁中试剂瓶盖倒放在桌面上,主要是为了避免瓶中试剂受污染 |
| D.戊中将水缓缓倒入浓硫酸并搅拌,是为了防止局部过热引起酸液飞溅 |
【知识点】 实验操作注意事项的探究 浓硫酸的性质及浓硫酸的稀释
| 物质 | 盐酸 | CuSO4溶液 | NaCl溶液 | 水 | Na2CO3溶液 | NaOH溶液 |
| PH | <7 | <7 | =7 | =7 | >7 | >7 |
| A.pH<7一定是酸的溶液 | B.pH>7一定是酸的溶液 |
| C.pH=7一定是酸的溶液 | D.盐的溶液可能显酸性、碱性或中性 |
【知识点】 盐的性质及用途 溶液的酸碱性与pH值的关系
具有美容养颜,解酒护肝健胃的重要用途。下列关于红枣醋饮的说法中正确的是( )

| A.红枣醋饮是胃酸过多病人养胃首选饮料 |
| B.该酸中碳元素的质量分数为最大 |
| C.该酸为有机物,它的相对分子质量为134 |
| D.该酸是由14个碳原子、10个氢原子和4个氧原子构成 |

| A.①③ | B.②③ | C.②④ | D.④⑤ |
【知识点】 金属活动性顺序及其应用
①石灰石和稀盐酸 ②镁和稀硫酸 ③碳酸钙固体和水 ④氧化铜和稀硫酸

| A.①②③④ | B.①② | C.①②④ | D.②③④ |
【知识点】 二氧化碳的实验室制法 金属的化学性质 酸的化学性质
| A.反应后溶液质量一定增加 |
| B.该金属可能是铁 |
| C.R的活泼性比Ag弱 |
| D.R表面有固体析出 |
【知识点】 金属活动性顺序及其应用 金属的化学性质
| A.BaCl2、HCl、Na2CO3 | B.K2CO3、NaNO3、KOH |
| C.MgCl2、H2SO4、NaOH | D.NaOH、H2SO4、HCl |
【知识点】 盐的性质及用途 离子或物质的共存问题 复分解反应及其应用
| A.Na2CO3、CuCl2 | B.Na2CO3、BaCl2 |
| C.KCl、CuCl2 | D.Na2CO3、KCl |
A. | B. |
C. | D. |
【知识点】 溶质质量分数的简单计算 金属的化学性质 pH值的变化

对此粉末成分判断正确的是( )
| A.该粉末可能是碳酸钠 | B.该粉末可能是碳酸钙 |
| C.该粉末一定是一种碱 | D.该粉末一定是生石灰 |
【知识点】 常见离子的检验方法及现象 物质的推断
二、填空题 添加题型下试题
(1)汽水中含有的一种酸___ ___;
(2)重要的化工原料,俗称烧碱__ __;
(3)非金属单质 __;
(4)盐 。
(1)由于人的胃里有 (填化学式),因此胃液分泌过多会引起胃病,服用含有氢氧化铝的药物可缓解病痛的原理是(用化学方程式表示) 。
(2)人被昆虫叮咬后皮肤红肿起泡 ,这是由于昆虫在皮肤内注入了少量甲酸(一种酸性物质)所致。把少许下表所列的生活常用品 (填编号)涂在被咬的皮肤上,痛痒会消失。
| 物质 | A | B | C |
| 食醋 | 牙膏 | 食盐水 | |
| pH | 3 | 9 | 7 |
【知识点】 碱的化学性质
三、解答题 添加题型下试题
(1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液,则白色沉淀可能是 ,(漏写、错写不给分)原混合物中一定不含有 。
(2)向实验(1)滤出的白色沉淀中加入足量的稀盐酸,沉淀全部溶解,并产生无色气体,则原混合物中一定含有 。
四、填空题 添加题型下试题
五、解答题 添加题型下试题

| 组别 | A组 | B组 | C组 | D组 |
| 试管I | Ca(OH)2 稀HCl | CaCO3 稀HCl | Zn 稀H2SO4 | Cu 稀H2SO4 |
| 试管Ⅱ | KNO3溶液 | Ca(OH)2溶液 | Ba(OH)2溶液 | Ba(OH)2溶液 |
(1)在试管I中加入试剂后,塞紧橡皮塞,关闭止水夹a,打开止水夹b,试管Ⅱ中液面上升,溶液变浑浊。符合以上实验现象的试剂是 组,此时Ⅱ中发生反应化学方程式为________ _______。
(2)在试管I中加入试剂后,塞紧橡皮塞,立即打开止水夹a,关闭止水夹b,试管Ⅱ中有气泡冒出,溶液变浑浊。符合以上实验现象的试剂是 组。此时Ⅱ中发生反应的化学方程式为___________________________。
六、填空题 添加题型下试题
(1)氢氧化钠的俗名是 (只写一种)。氢氧化钠与硫酸反应的化学方程式为 。
(2)实验室有一瓶久置的固体,标签上写着“氢氧化钠”。为了检验里面是否还存在NaOH,实验员取少量该固体样品进行以下实验:

此实验的现象说明样品中含有 (填序号)。
| A.CaCl2 | B.Na2CO3 | C.NaOH | D.Na2CO3和NaOH |
如果白色沉淀中含有两种物质,一种可能是Ca(OH)2另一种一定是 (填化学式)
某金属与同体积盐酸溶液反应实验数据表:
| 盐酸溶液浓度 | 反应开始时酸 溶液的温度 | 反应开始到2分钟产生的气体体积 | 反应结束共产生气体体积 |
| 5% | 20℃ | 10 mL | 60 mL |
| 10% | 20℃ | 19 mL | 118 mL |
| 15% | 20℃ | 28 mL | 175 mL |
| 5% | 35℃ | 28 mL | 60 mL |
| 10% | 35℃ | 72 mL | 118 mL |
| 15% | 35℃ | 103 mL | 175 mL |
(1)分析实验数据得出:一定质量的某种金属和同体积盐酸反应,影响金属和酸反应快慢的主要因素有 、 。
(2)可以通过比较 实验数据来确定金属和酸反应的快慢。
(3)过量锌粒加入盐酸中,反应开始的一段时间,反应速率逐渐加快,而不是逐渐减慢。请分析原因。 。
【知识点】 置换反应及其应用
七、探究题 添加题型下试题
小明根据初中学过的科学知识,认为铁制容器中的液体肯定不是稀硫酸或盐酸。这种液体到底是什么?第二天小明请教老师,老师没有直接告诉答案,而是在实验室配制了一种液体后,对小明说:铁制容器中装的就是这种液体,它是一种常见化合物的溶液。还提供了相关信息,请小明自己动手探究。
提供的信息:许多金属或它们的化合物在灼烧时都会使火焰呈现特殊的颜色。如:钾——紫色;钠——黄色;钡——黄绿色;钙——砖红色。
下表是小明的实验步骤和现象记录:
| 序号 | 实验步骤 | 实验现象 |
| ① | 观察溶液 | 无色液体 |
| ② | 取少量该溶液于试管中,滴加紫色石蕊试液 | 紫色石蕊试液变蓝色 |
| ③ | 另取少量溶液在酒精灯火焰上灼烧 | 火焰呈现黄色 |
| ④ | 取少量该溶液于试管中,先滴加硫酸铜溶液,再滴加稀盐酸 | 先有蓝色沉淀生成,加入稀盐酸后沉淀消失,无其它明显现象 |
(1)小明认为铁制容器中的液体肯定不是稀硫酸或盐酸。理由是 。
(2)在步骤④中,小明加入稀盐酸的目的是防止 的干扰(填写离子符号)。
(3)小明通过实验,可得出该溶液中的溶质是 。
(4)小明想进一步了解铝和这种溶液反应的原理,再次请教科学老师,老师启发小明说:铝和这种溶质以及水发生反应,生成含有偏铝酸根离子(AlO2-)的盐和氢气两种物质。请你尝试写出该反应的化学方式: 。
【知识点】 金属的化学性质 盐的性质及用途 常见离子的检验方法及现象
八、填空题 添加题型下试题
| 实验步骤 | 实验操作 | 现象 |
| 一 | 取混合溶液100克,加入过量的氯化钡溶液 | 产生白色沉淀 |
| 二 | 滴加无色酚酞试液 | 红色 |
| 三 | 逐滴加入稀盐酸 | 无色 |
利用下列提供的资料和你所学知识,从微观角度分析实验步骤三中向混有Ba2CO3白色沉淀的NaOH溶液中直接滴加稀盐酸,为什么不会使Ba2CO3与稀盐酸反应而影响实验结果,原因是 。
资料:
1.沉淀物是处于晶体状态,晶体中的离子和分子都是固定在晶格中无法移动。
2.酸、碱溶液中溶质电离出自由移动的离子,离子在溶液中处于高度分散状态。
3.其他条件一定时,反应物间的接触面积越大,化学反应速率越快。
4.其他条件一定时,反应物之间接触机会越多,化学反应速率越快。
【知识点】 酸的化学性质
九、解答题 添加题型下试题
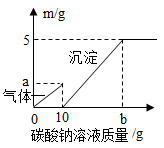
(1)滴加的溶液中溶质属于
(2)10克碳酸钠溶液中含有的溶质质量是
(3)图像中的a点数值是
(4)废液中含有的溶质是
(5)通过计算说明,图像横坐标中的b点表示的溶液的质量是多少克
【知识点】 初中科学综合库
(1)在D中滴入无色酚酞试液,D呈红色,然后向D中逐滴加入B,有白色沉淀析出,溶液红色就逐渐变淡,最后呈无色,再加稀硝酸,白色沉淀不溶解。
(2)把C分别加入A和E中,都生成白色沉淀,分别加入稀HNO3,C和A生成的白色沉淀溶解,而C和E生成的白色沉淀不溶解。
试推断(写物质的名称):A: B: C: D: 。
| 加入Na2CO3溶液的质量/g | 25 | 50 | 75 | 100 | 125 |
| 生成沉淀的质量/g | 0 | 1 | 3 | 4 | X |
请回答下列问题:
(1)对实验数据进行分析后该同学认为实验时他所取的盐酸过量,理由是
(2)表格中X为
(3)求所加碳酸钠溶液的溶质质量分数
【知识点】 盐的性质及用途
(1)赤铜(Cu2O)是我国古代制取黄铜的一种原料。Cu2O中铜元素与氧元素的质量比是 。
(2)弹壳的黄铜只含有锌和铜。将22 g弹壳放在盛有100 g稀硫酸的烧杯中(硫酸足量),当弹壳不再溶解后,烧杯中混合物的质量是121.8 g。计算:
①产生氢气的质量。
②弹壳中铜的质量。
③反应后所得溶液中ZnSO4的质量分数(计算结果保留一位小数)。
【知识点】 金属的化学性质
试卷分析
试卷题型(共 28题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.64 | 盐的性质及用途 | |
| 2 | 0.65 | 酸的化学性质 | |
| 3 | 0.85 | 识别化学反应基本类型 | |
| 4 | 0.65 | 常见物质的分类 | |
| 5 | 0.85 | 实验操作注意事项的探究 浓硫酸的性质及浓硫酸的稀释 | |
| 6 | 0.65 | 盐的性质及用途 溶液的酸碱性与pH值的关系 | |
| 7 | 0.85 | 碱的化学性质 盐的性质及用途 酸碱指示剂及其性质 | |
| 8 | 0.65 | 有机物与无机物的区别 相对原子质量 有关化学式的计算和推断 化学符号及其周围数字的意义 | |
| 9 | 0.65 | 金属活动性顺序及其应用 | |
| 10 | 0.65 | 二氧化碳的实验室制法 金属的化学性质 酸的化学性质 | |
| 11 | 0.65 | 金属活动性顺序及其应用 金属的化学性质 | |
| 12 | 0.4 | 盐的性质及用途 离子或物质的共存问题 复分解反应及其应用 | |
| 13 | 0.65 | 盐的性质及用途 常见物质的鉴定 | |
| 14 | 0.65 | 溶质质量分数的简单计算 金属的化学性质 pH值的变化 | |
| 15 | 0.4 | 常见离子的检验方法及现象 物质的推断 | |
| 二、填空题 | |||
| 16 | 0.65 | 碱的物理性质及用途 酸的物理性质及用途 常见物质的分类 | |
| 17 | 0.85 | 碱的化学性质 | |
| 19 | 0.65 | 铁锈的主要成分 金属的化学性质 | |
| 21 | 0.65 | 碱的化学性质 中和反应及其应用 | |
| 22 | 0.64 | 置换反应及其应用 | |
| 24 | 0.4 | 酸的化学性质 | |
| 三、解答题 | |||
| 18 | 0.4 | 盐的性质及用途 常见物质的鉴定 | |
| 20 | 0.65 | 金属的化学性质 酸的化学性质 碱的化学性质 | |
| 25 | 0.64 | ||
| 26 | 0.4 | 酸的化学性质 碱的化学性质 盐的性质及用途 物质的推断 | |
| 27 | 0.65 | 盐的性质及用途 | |
| 28 | 0.4 | 金属的化学性质 | |
| 四、探究题 | |||
| 23 | 0.65 | 金属的化学性质 盐的性质及用途 常见离子的检验方法及现象 | |







