浙江省金华市义乌市北苑中学2023-2024学年九年级上学期科学学力检测卷
浙江
九年级
阶段练习
2024-05-24
11次
整体难度:
容易
考查范围:
常见的物质、科学探究所需要的基本技能、物质的运动与相互作用、物质的结构
一、选择题 添加题型下试题
| A.铜雕锈蚀 | B.枯木腐朽 |
| C.冰雪消融 | D.火山烈燃 |
【知识点】 化学变化和物理变化的判别
种类 | 苹果汁 | 牛奶 | 白开水 | 豆浆 |
pH值 | 2.9-3.3 | 6.3-6.6 | 7.0 | 7.4-7.9 |
| A.苹果汁 | B.牛奶 | C.白开水 | D.豆浆 |
【知识点】 溶液的酸碱性与pH值的关系
| A.浓硫酸的脱水性 | B.浓硫酸的吸水性 |
| C.氢氧化钠易潮解 | D.浓盐酸的挥发性 |
【知识点】 化学性质与物理性质的差别及应用 酸的化学性质 碱的化学性质
| A.食盐 | B.食用纯碱 |
| C.山茶油 | D.食醋 |
A. 闻气体气味 闻气体气味 | B.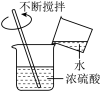 稀释浓硫酸 稀释浓硫酸 |
C. 点燃酒精灯 点燃酒精灯 | D. 测溶液酸碱度 测溶液酸碱度 |
【知识点】 常见实验操作 浓硫酸的性质及浓硫酸的稀释 pH值的测量及方法
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |
A.   | B.   |
C.   | D.   |
【知识点】 盐的性质及用途
| A.稀盐酸不能用于除铁锈 | B.浓硫酸具有腐蚀性 |
| C.浓盐酸没有挥发性 | D.稀盐酸能使无色酚酞试液变红 |
【知识点】 酸的化学性质
| A.CO、H2、HCl | B.SO2、CO2、HCl | C.H2、O2、N2 | D.SO2、H2、CO |
【知识点】 碱的化学性质
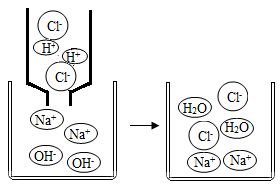
| A.反应结束时溶液的pH=7 |
| B.反应前后元素的种类没有变化 |
| C.反应后溶液中存在的粒子只有Na+和Cl- |
| D.该反应的实质是H+和OH-结合生成水 |
【知识点】 中和反应及其应用 质量守恒定律及其应用
| A.氢氧化钠可用于干燥二氧化碳气体 |
| B.人体胃液中含有硫酸,可以帮助消化 |
| C.氢氧化钙可用于配制波尔多液、改良酸性土壤 |
| D.氢氧化钠的和氢氧化钙溶于水都会放出大量的热 |
A. 将等质量的锌粉、铁粉分别放入盛有足量且相同浓度稀盐酸的容器中 将等质量的锌粉、铁粉分别放入盛有足量且相同浓度稀盐酸的容器中 |
B. 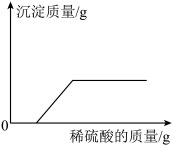 向NaOH和BaCl2的混合溶液中滴加H2SO4溶液 向NaOH和BaCl2的混合溶液中滴加H2SO4溶液 |
C. 实验室的浓硫酸、浓盐酸敞口放置一段时间 实验室的浓硫酸、浓盐酸敞口放置一段时间 |
D. 向20g10%氢氧化钠溶液中逐滴滴入7.3%的稀盐酸(Q点表示恰好完全反应) 向20g10%氢氧化钠溶液中逐滴滴入7.3%的稀盐酸(Q点表示恰好完全反应) |
| A.BaCl2、HCl、Na2CO3 | B.K2CO3、NaNO3、KOH |
| C.MgCl2、H2SO4、NaOH | D.NaOH、H2SO4、HCl |
【知识点】 盐的性质及用途 离子或物质的共存问题 复分解反应及其应用
二、填空题 添加题型下试题
(1)写出水杨酸的一条物理性质
(2)水杨酸(C7H4O3)中碳元素和氧元素的质量比为
【知识点】 化学性质与物理性质的差别及应用 有关化学式的计算和推断
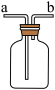
(2)若要用来检验二氧化碳气体,则瓶中所盛放液体的化学式是
【知识点】 常见气体的检验与除杂方法 二氧化碳的实验室制法
(1)
(2)
(1)X的化学式为
(2)硝酸铵用做肥料时,要避免与
(2)根据颜色对比,空地土壤的pH约为7.8,查阅资料,常见作物最适生长的土壤pH范围如表,则这块空地上适合种植的作物有
| 作物 | 马铃薯 | 胡萝卜 | 西瓜 | 海水稻 | 沙枣 |
| 最适pH范围 | 4.8~5.5 | 5.3~6.0 | 6.0~8.5 | 7.5~8.5 | 8.0~8.7 |
【知识点】 溶液的酸碱性与pH值的关系
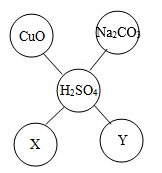
(2)请写出稀硫酸与Y反应的一个化学方程式:
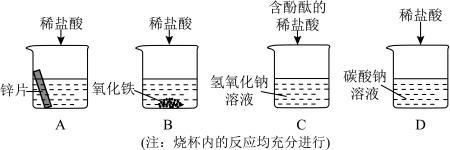
(2)D中发生反应的化学方程式是
【知识点】 酸的化学性质
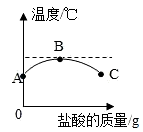
(2)B处溶液的溶质是
【知识点】 中和反应及其应用
三、解答题 添加题型下试题
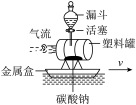
(2)气体从左边罐底小孔喷出使船向右前进,这是由于
四、探究题 添加题型下试题
①取试样溶于水,搅拌、过滤,得到无色澄清溶液A和白色沉淀B。
②取上述无色澄清溶液A,通入适量的CO2,生成白色沉淀C。
③取上述白色沉淀B,加入过量的稀硝酸,沉淀全部消失。综合上述实验现象,回答下列问题:
(1)由①得原固体粉末中一定不含
(2)写出固体粉末的可能组成中含有物质种类最多的一种组合
【知识点】 碱的化学性质 盐的性质及用途 离子或物质的共存问题 物质的推断
五、填空题 添加题型下试题

(2)若在测定A点pH过程中,错用湿润的玻璃棒蘸取待测液,测量结果将
(3)下列物质中能与NaOH溶液反应,但溶液颜色无明显变化的是
A.
 B.
B. C.
C. D.
D.
【知识点】 碱的化学性质 溶液的酸碱性与pH值的关系
六、探究题 添加题型下试题

(2)b点可以观察到的实验现象是
(3)甲组同学提出直接蒸发溶剂可从剩余废液中回收纯净CaCl2,乙组同学认为此方法会对空气造成污染。在不借助其它试剂和仪器的情况下,除去废液中对空气造成污染的物质,建议最好先在废液中加入下面(填选项序号)试剂
A.CaO B.Ca(OH)2 C.CaCO3
【收集资料】通过阅读标签及查阅资料,她获得如下信息:
(1)该固体酒精中含有酒精、氯化钙、氢氧化钠三种物质;
(2)酒精的化学式为C2H5OH;
(3)氯化钙、氯化钡的水溶液均呈中性。
【提出问题】
(1)酒精的化学式与NaOH相比,都有“OH”,那么酒精的水溶液是不是显碱性?
(2)固体酒精中的氢氧化钠是否变质及变质的程度如何?
【实验探究】
实验一:她取少量酒精溶液于试管中,滴加硫酸铜溶液,未观察到蓝色沉淀,说明酒精溶液
实验二:(1)她先取少量固体酒精于烧杯中,加入足量水溶解后静置,发现烧杯底部有白色沉淀,再取沉淀于试管中加稀盐酸,观察到
(2)她取上述烧杯中上层清液于试管中,先滴加足量澄清石灰水,发现生成白色沉淀,再滴入几滴无色酚酞溶液,液体呈红色,她认为氢氧化钠部分变质。老师发现后,提示她由该实验得出的结论不可靠。你认为只要将上述实验中的澄清石灰水变为
【拓展应用】除去部分变质的氢氧化钠溶液中的杂质,方法是
【知识点】 碱的化学性质 盐的性质及用途 常见物质的鉴定 书写化学方程式、文字表达式
【提出问题】该瓶粉末的成分是什么?
(1)【猜想与假设】猜想一:该瓶粉末的成分可能为氢氧化钙
猜想二:该瓶粉末的成分可能为氢氧化钙和碳酸钙
猜想三:该瓶粉末的成分可能为碳酸钙。
(2)【实验验证】请你参与探究,完成下面的实验报告.
| 实验步骤 | 实验现象 | 实验结论 | 猜想二正确 |
| (1)取少量样品于小烧杯中,加入适量水,充分搅拌,过滤,取少量滤渣于试管中,加入稀盐酸。 | 有大量气泡产生 | 说明含有 | |
| (2)取步骤(1)中的 | 说明含有 |
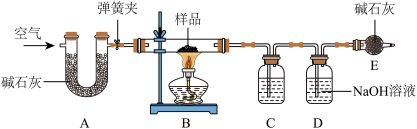
②碱石灰是CaO与NaOH的固体混合物
③加热条件下,纯碱稳定不分解,小苏打易分解,反应的化学方程式为:2NaHCO3
 Na2CO3+H2O+CO2↑探究过程如下:
Na2CO3+H2O+CO2↑探究过程如下:Ⅰ.称量样品和已装入相关药品的装置C、D的质量,分别为:m、m1、m2;
Ⅱ.将质量为m的样品装入B玻璃管中,按图连接好装置,关闭弹簧夹,给玻璃管加热
Ⅲ.待玻璃管中样品完全反应,打开弹簧夹通空气,再熄灭酒精灯,直到玻璃管冷却
Ⅳ.再次称量装置C、D的质量,分别为m3、m4
请回答下列问题:
(1)装置C中所装药品为
(2)鼓入空气的作用是
(3)依据实验所得数据计算,该样品中小苏打的质量分数为
【知识点】 盐的性质及用途 质量守恒定律及其应用
七、解答题 添加题型下试题
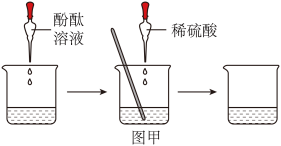
(2)计算所得溶液的溶质质量分数
(3)查阅资料:已知酚酞溶液的变红色范围是pH在8.2~10.0之间。若硫酸滴到溶液颜色刚好由红色变为无色时,请写出此时溶液中存在的离子有
【知识点】 中和反应及其应用 根据化学反应方程式的计算

(2)反应后产生气体的质量是多少克
(3)试通过计算求2片钙片中碳酸钙的含量
【知识点】 根据化学反应方程式的计算
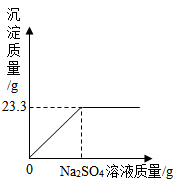
(1)完全反应后生成BaSO4沉淀
(2)恰好完全反应时消耗Na2SO4溶液的质量是多少克
(3)恰好完全反应时所得溶液中溶质的质量分数是多少
【知识点】 盐的性质及用途 根据化学反应方程式的计算
| 实验次数 | 1 | 2 | 3 | 4 | 5 | 6 |
| 样品质量/克 | 30 | 30 | 30 | 30 | 30 | 30 |
| 稀硫酸质量/克 | 30 | 60 | 90 | 120 | 150 | 180 |
| 产生气体质量/克 | 0 | 0.1 | 0.3 | 0.5 | m | 0.6 |
(2)表格中m的数值为
(3)请计算该实验中的铁粉中的铁单质的质量分数
【知识点】 酸的化学性质 根据化学反应方程式的计算

试卷分析
试卷题型(共 35题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.94 | 化学变化和物理变化的判别 | |
| 2 | 0.85 | 溶液的酸碱性与pH值的关系 | |
| 3 | 0.94 | 化学性质与物理性质的差别及应用 酸的化学性质 碱的化学性质 | |
| 4 | 0.85 | 酸的化学性质 盐的性质及用途 酸碱指示剂及其性质 | |
| 5 | 0.94 | 常见实验操作 浓硫酸的性质及浓硫酸的稀释 pH值的测量及方法 | |
| 6 | 0.94 | 碱的物理性质及用途 盐的性质及用途 常见物质的俗称 | |
| 7 | 0.94 | 盐的性质及用途 复分解反应及其应用 | |
| 8 | 0.94 | 盐的性质及用途 | |
| 9 | 0.94 | 酸的化学性质 | |
| 10 | 0.85 | 碱的化学性质 盐的性质及用途 物质除杂或净化 | |
| 11 | 0.85 | 碱的化学性质 | |
| 12 | 0.65 | 中和反应及其应用 质量守恒定律及其应用 | |
| 13 | 0.65 | 碱的物理性质及用途 酸的物理性质及用途 酸的化学性质 碱的化学性质 | |
| 14 | 0.85 | 碱的化学性质 中和反应及其应用 盐的性质及用途 | |
| 15 | 0.4 | 盐的性质及用途 离子或物质的共存问题 复分解反应及其应用 | |
| 二、填空题 | |||
| 16 | 0.94 | 化学性质与物理性质的差别及应用 有关化学式的计算和推断 | |
| 17 | 0.94 | 常见气体的检验与除杂方法 二氧化碳的实验室制法 | |
| 18 | 0.94 | 碱的物理性质及用途 盐的性质及用途 | |
| 19 | 0.85 | 盐与化肥 化学方程式的配平 | |
| 20 | 0.94 | 溶液的酸碱性与pH值的关系 | |
| 21 | 0.85 | 酸的化学性质 碱的化学性质 盐的性质及用途 | |
| 22 | 0.94 | 酸的化学性质 | |
| 23 | 0.94 | 中和反应及其应用 | |
| 26 | 0.85 | 碱的化学性质 溶液的酸碱性与pH值的关系 | |
| 三、解答题 | |||
| 24 | 0.65 | 酸的化学性质 盐的性质及用途 力的作用是相互的 | |
| 31 | 0.65 | 中和反应及其应用 根据化学反应方程式的计算 | |
| 32 | 0.85 | 根据化学反应方程式的计算 | |
| 33 | 0.65 | 盐的性质及用途 根据化学反应方程式的计算 | |
| 34 | 0.65 | 酸的化学性质 根据化学反应方程式的计算 | |
| 35 | 0.65 | 碱的化学性质 盐的性质及用途 | |
| 四、探究题 | |||
| 25 | 0.4 | 碱的化学性质 盐的性质及用途 离子或物质的共存问题 物质的推断 | |
| 27 | 0.85 | 碱的化学性质 盐的性质及用途 | |
| 28 | 0.65 | 碱的化学性质 盐的性质及用途 常见物质的鉴定 书写化学方程式、文字表达式 | |
| 29 | 0.85 | 碱的化学性质 盐的性质及用途 | |
| 30 | 0.65 | 盐的性质及用途 质量守恒定律及其应用 | |



