浙教版科学九年级上册第一章物质及其变化综合检测
全国
九年级
单元测试
2019-09-03
367次
整体难度:
适中
考查范围:
常见的物质、物质的结构、物质的运动与相互作用、科学探究所需要的基本技能
一、选择题 添加题型下试题
| A.石蜡熔化,干冰用于人工降雨 |
| B.煤干馏,稀有气体用作焊接金属的保护气 |
| C.钢铁生锈,氦气用于填充探空气球 |
| D.活性炭去除冰箱异味,熟石灰用来改良酸性土壤 |
【知识点】 化学变化和物理变化的判别
| A.甲、乙、丙、丁不可能含有同一种元素 |
| B.丙为盐、丁为水,则该反应一定为复分解反应 |
| C.甲、乙为化合物,则该反应一定为复分解反应 |
| D.丙为Cu(NO3)2,则甲可能为单质、氧化物、碱或盐 |
【知识点】 氧化物、酸、碱和盐的概念 复分解反应及其应用
| A.红色、蓝色、无色 | B.红色、蓝色、紫色 |
| C.蓝色、红色、无色 | D.蓝色、红色、紫色 |
【知识点】 酸碱指示剂及其性质
| A.CO(NH2)2 | B.Ca3(PO4)2 |
| C.K2SO4 | D.NH4Cl |
【知识点】 盐与化肥
A.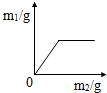 | B.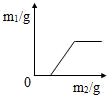 | C.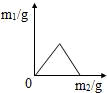 | D.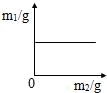 |
| A.取少量样品,加入几滴酚酞溶液,溶液由无色变红色,证明氢氧化钠溶液没有变质 |
| B.取少量样品,加入少量稀盐酸,没有气泡产生,证明氢氧化钠溶液没有变质 |
| C.取少量样品,加入过量的氯化钡溶液,有白色沉淀生成,过滤,向滤液中加入几滴酚酞溶液,溶液不变色,证明氢氧化钠溶液完全变质 |
| D.取少量样品,加入过量的氢氧化钡溶液,有白色沉淀生成,过滤,向滤液中加入几滴酚酞溶液,溶液由无色变红色,证明氢氧化钠溶液部分变质 |
【知识点】 碱的化学性质 盐的性质及用途 常见离子的检验方法及现象
A.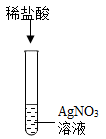 | B.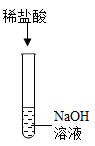  |
C.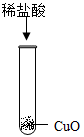  | D.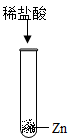 |
【知识点】 酸的化学性质
| 选项 | 物质 | 杂质 | 除杂所用的试剂和方法 |
| A | CaO固体 | CaCO3固体 | 加入适量的稀盐酸 |
| B | NaOH溶液 | Ca(OH)2溶液 | 先加入过量的Na2CO3溶液,再过滤 |
| C | CO2气体 | CO气体 | 点燃 |
| D | H2气体 | HCl气体 | 先通过NaOH溶液,再通过浓硫酸 |
| A.A | B.B | C.C | D.D |
【知识点】 常见气体的检验与除杂方法 盐的性质及用途 物质除杂或净化
| A.碱溶液显碱性,则显碱性的溶液一定是碱溶液 |
| B.pH<7的溶液呈酸性,则pH<7的雨水是酸雨 |
| C.单质只含一种元素,则只含一种元素的物质一定是单质 |
| D.复分解反应只是两种化合物相互交换成分,则复分解反应一定没有元素化合价的改变 |
【知识点】 碱的化学性质 溶液的酸碱性与pH值的关系 复分解反应及其应用
| A.氢氧化钠可用于干燥二氧化碳气体 |
| B.人体胃液中含有硫酸,可以帮助消化 |
| C.氢氧化钙可用于配制波尔多液、改良酸性土壤 |
| D.氢氧化钠的和氢氧化钙溶于水都会放出大量的热 |
| A.④⑤②①③ | B.②④⑤①③ |
| C.②⑤④①③ | D.⑤②④③① |
【知识点】 粗盐提纯实验
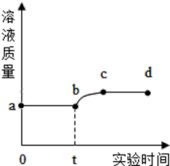
| A.ab段说明Cu不能转换出硫酸中的氢 |
| B.从b点到c点,溶液的pH逐渐增大 |
| C.从c点到d点,溶液中的溶质只可能有一种 |
D.bc段发生的反应为2Cu+2H2SO4+O2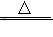 2CuSO4+2H2O 2CuSO4+2H2O |
【知识点】 金属活动性顺序及其应用 酸的化学性质 pH值的变化
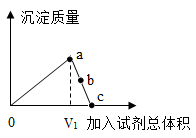
| A.b点时所加试剂一定是稀盐酸 |
| B.加入试剂总体积为V1时,溶液中不存在NaOH |
| C.c点时溶液中的溶质都是盐 |
| D.a点时溶液中一定不存在Cu2+ |
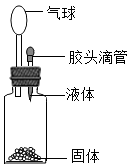
①硝酸铵和水;②铁和稀硫酸;③固体氢氧化钠和水;④生石灰和水;⑤石灰石和稀盐酸。
| A.①②③④⑤ | B.②③④⑤ | C.②③⑤ | D.②④⑤ |
【知识点】 溶解时的吸热或放热现象 酸的化学性质
二、填空题 添加题型下试题
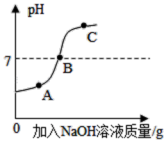
(1)写出C点的溶质
(2)A点溶液中的阳离子有
【知识点】 中和反应及其应用 pH值的变化 溶液的酸碱性与pH值的关系
(2)打开盛有浓盐酸的试剂瓶会看到瓶口出现
(3)向滴加两滴酚酞试剂的氢氧化钠溶液中,逐滴滴加稀硫酸至过量,可观察到的现象
(1)将该盐酸敞口露置于空气中,一段时间后,其溶质的质量分数
(2)该盐酸因含有少量Fe3+而显黄色(其他杂质忽略不计)。现取少量样品,与适量硝酸银溶液恰好完全反应。经实验测得,反应后溶液中的H+和NO3﹣的个数比为91:94,则该盐酸中Fe3+和Cl﹣的个数比为
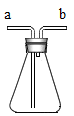
(1)若用此装置除去氢气中混入的少量水蒸气,在瓶内应装的试剂是
(2)若要验证氢气中是否混有少量的氯化氢气体,则瓶内应装的试剂是
(3)若要用排水法收集一瓶氧气,气体应从
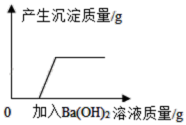
(1)可观察一的宏观现象是:有
(2)从微观层面分析,沉淀是Cu2+与OH﹣相互结合生成了不溶于水的物质;溶液颜色的变化是因为
(3)上述反应可以用化学方程式表示为:
【知识点】 碱的化学性质 常见离子的检验方法及现象 书写化学方程式、文字表达式
【知识点】 盐的性质及用途 离子或物质的共存问题
(1)在试管中加入少量粉末,注入足量的蒸馏水充分振荡溶液无色透明;
(2)取少量上述溶液滴入盐酸, 有气泡产生;
(3)另取(1)中少量溶液滴入氯化钡溶液,有白色沉淀产生;
(4)在(3)中滴加稀硝酸沉淀全部溶解,并有气泡产生。
该白色粉末中一定含有 ;一定没有 ;可能含有 。(填化学式)
【知识点】 酸、碱、盐的鉴别 常见离子的检验方法及现象
实验一:Mg和稀硫酸
实验二:MgO和稀硫酸
实验三:Ba(NO3)2溶液和稀硫酸
实验四:KOH溶液和稀硫酸
(1)实验三中发生反应的化学方程式为
(2)实验四无明显现象,再将打磨过的铁丝浸入该试验后的溶液中,仍无明显现象,据此
(3)将上述所有实验后的溶液混合,并进行如下实验:
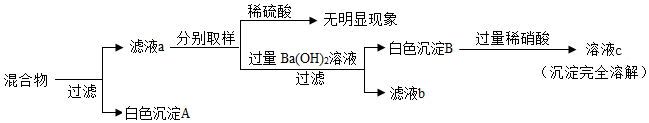
①写出滤液a中所含溶质的所有可能情况
②分析上述实验,下列说法正确的是
A.用白色沉淀A一定能除去MgC12溶液中的少量盐酸
B.用白色沉淀B能检验CaCl2溶液中是否含有盐酸
C.用滤液b与适量的K2SO4溶液混合,过滤,制备KNO3溶液
D.向溶液c中加入过量的NaOH溶液或过量的Na2CO3溶液都有明显的现象
【知识点】 酸的化学性质 碱的化学性质 盐的性质及用途 常见离子的检验方法及现象
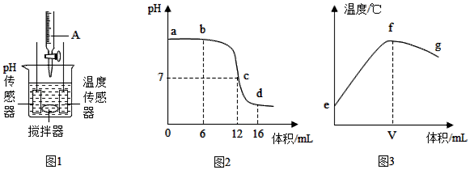
(2)仪器A中溶液的溶质是
(3)图3中V的数值最接近
(4)下列说法错误的是
A.图2中b点所示溶液中的溶质是NaCl和NaOH;
B.取图2中d点所示溶液加热蒸干所得固体为纯净物
C.图2中c→d所示溶液中NaCl的质量不断增加;
D.图3中e→f变化趋势可说明该反应是放热反应。
三、解答题 添加题型下试题
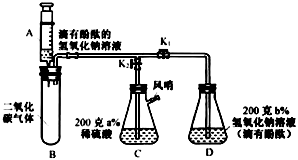
③再打开止水夹K2,风哨振动鸣叫,C中的部分溶液被吸入B和D中,反应后B、D中溶液都变为无色。
回答:
(1)步骤①中,充分反应后,试管B里的CO2最终转化为
(2)解释步骤②中“风哨振动鸣叫”的原因。
(3)实验开始时C、D中两种溶液中溶质质量分数大小关系为:a%
【知识点】 溶质质量分数的简单计算 二氧化碳的化学性质 碱的化学性质
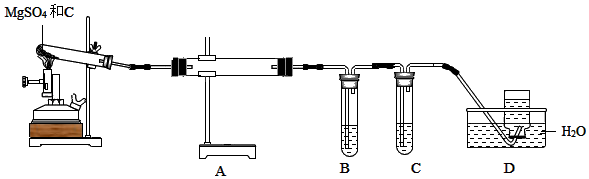
①装置B、C中的溶液分别是
a.NaOH溶液 b.KMnO4溶液
③装置D的作用是
④若将装置A中的固体隔绝空气加热至500℃,就会变成蒸气,其中有一种相对分子质量为128的气体。该气体的化学式为
【知识点】 常见气体的检验与除杂方法 碱的化学性质

(1)写出反应③的化学方程式
(2)溶液D的颜色是
(3)写出溶液D中一定存在的离子的符号
【知识点】 盐的性质及用途 常见离子的检验方法及现象 物质的推断
四、填空题 添加题型下试题
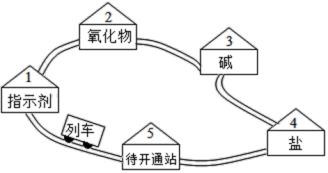
①与“碳酸钠溶液”和“稀盐酸”都能反应的“3号站”的对应物质为
②“稀盐酸”列车途经“5号站”时,反应的化学方程式为
③“稀盐酸”列车途经“1、2、3号站”时,原“碳酸钠溶液”列车途经某站的对应物质必须更换为
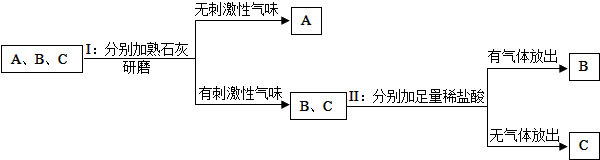
根据上述实验回答:
(1)写出三种化肥的名称:A
(2)如果实验II中B、C两种样品没有另取,对实验结果
(3)写出操作Ⅰ中涉及的化学反应的方程式:
五、探究题 添加题型下试题
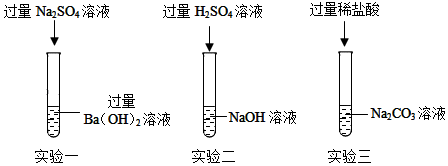
(1)实验一中反应后的溶液呈
(2)实验二中反应的化学方程式为
(3)实验三中的现象是
(4)将实验一、三所得物质倒入同一废液缸,得白色沉淀和无色溶液,为探究无色溶液中的溶质成分,下列实际组合可行的是
A、稀盐酸和BaCl2溶液 B、NH4Cl溶液和CuO C、酚酞溶液和Na2CO3溶液。
六、解答题 添加题型下试题
(1)原固体混合物中碳酸钠的质量;
(2)原固体混合物中氢氧化钠的质量分数;
(3)反应后所得溶液的溶质质量分数。
【知识点】 碱的化学性质 盐的性质及用途 根据化学反应方程式的计算
| 学 生 物 质 质 量 | 甲 | 乙 | 丙 | 丁 |
| 所取固体样品的质量(g) | 30 | 25 | 20 | 20 |
| 加入硫酸溶液的质量(g) | 100 | 100 | 100 | 120 |
| 反应后剩余固体的质量(g) | 22 | 17 | 12 | 12 |
分析实验数据,回答下列问题:
(1)写出氧化铜与硫酸反应的化学方程式
(2)求混合物中氧化铜的质量分数。
(3)求硫酸溶液中溶质的质量分数。
【知识点】 溶质质量分数的简单计算 酸的化学性质 根据化学反应方程式的计算
第一步:取一定量的固体粉末。加入足量的水充分搅拌,得到蓝色溶液。则此固体粉末中一定没有_________________________。(写化学式)
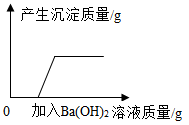
第二步:为进一步确定此固体粉末的组成,实验小组同学用天平称46.2克此固体粉末,完全溶于水中得到174.6克溶液,再向其中加入溶质质量分数为8%的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液质量的关系如图所示。据图回答:
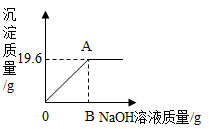
(1)产生最大沉淀量时加入氢氧化钠溶液的质量为___________克。
(2)通过计算确定46.2克固体粉末的组成 。(回答出物质名称及质量)
(3)计算A点所示溶液中溶质的质量分数 。
【知识点】 盐的性质及用途 离子或物质的共存问题 根据化学反应方程式的计算
试卷分析
导出试卷题型(共 34题)
试卷难度
知识点分析
细目表分析
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.65 | 化学变化和物理变化的判别 | |
| 2 | 0.65 | 氧化物、酸、碱和盐的概念 复分解反应及其应用 | |
| 3 | 0.85 | 酸碱指示剂及其性质 | |
| 4 | 0.85 | 盐与化肥 | |
| 5 | 0.65 | 中和反应及其应用 盐的性质及用途 | |
| 6 | 0.65 | 碱的化学性质 盐的性质及用途 常见离子的检验方法及现象 | |
| 7 | 0.65 | 酸的化学性质 | |
| 8 | 0.65 | 常见气体的检验与除杂方法 盐的性质及用途 物质除杂或净化 | |
| 9 | 0.65 | 酸的化学性质 盐的性质及用途 pH值的变化 | |
| 10 | 0.65 | 碱的化学性质 溶液的酸碱性与pH值的关系 复分解反应及其应用 | |
| 11 | 0.65 | 碱的物理性质及用途 酸的物理性质及用途 酸的化学性质 碱的化学性质 | |
| 12 | 0.85 | 粗盐提纯实验 | |
| 13 | 0.65 | 金属活动性顺序及其应用 酸的化学性质 pH值的变化 | |
| 14 | 0.65 | 碱的化学性质 盐的性质及用途 | |
| 15 | 0.65 | 溶解时的吸热或放热现象 酸的化学性质 | |
| 二、填空题 | |||
| 16 | 0.65 | 中和反应及其应用 pH值的变化 溶液的酸碱性与pH值的关系 | |
| 17 | 0.85 | 酸的物理性质及用途 酸碱指示剂及其性质 | |
| 18 | 0.65 | 酸的物理性质及用途 盐的性质及用途 | |
| 19 | 0.65 | 常用气体的发生装置和收集装置与选取方法 常见气体的检验与除杂方法 酸的化学性质 | |
| 20 | 0.65 | 碱的化学性质 常见离子的检验方法及现象 书写化学方程式、文字表达式 | |
| 21 | 0.65 | 中和反应及其应用 复分解反应及其应用 | |
| 22 | 0.4 | 盐的性质及用途 离子或物质的共存问题 | |
| 23 | 0.65 | 酸、碱、盐的鉴别 常见离子的检验方法及现象 | |
| 24 | 0.65 | 酸的化学性质 碱的化学性质 盐的性质及用途 常见离子的检验方法及现象 | |
| 25 | 0.65 | 酸的化学性质 碱的化学性质 中和反应及其应用 | |
| 29 | 0.65 | 碱的化学性质 盐的性质及用途 物质的推断 | |
| 30 | 0.65 | 盐与化肥 常见物质的鉴定 | |
| 三、解答题 | |||
| 26 | 0.65 | 溶质质量分数的简单计算 二氧化碳的化学性质 碱的化学性质 | |
| 27 | 0.65 | 常见气体的检验与除杂方法 碱的化学性质 | |
| 28 | 0.4 | 盐的性质及用途 常见离子的检验方法及现象 物质的推断 | |
| 32 | 0.4 | 碱的化学性质 盐的性质及用途 根据化学反应方程式的计算 | |
| 33 | 0.65 | 溶质质量分数的简单计算 酸的化学性质 根据化学反应方程式的计算 | |
| 34 | 0.4 | 盐的性质及用途 离子或物质的共存问题 根据化学反应方程式的计算 | |
| 四、探究题 | |||
| 31 | 0.65 | 酸的化学性质 碱的化学性质 盐的性质及用途 | |



