浙江省绍兴市诸暨市十校共进2019-2020学年九年级上学期11月份联考科学试题
浙江
九年级
阶段练习
2020-02-07
185次
整体难度:
适中
考查范围:
生物的新陈代谢、常见的物质、科学探究所需要的基本技能、物质的结构、物质的运动与相互作用
一、选择题 添加题型下试题
A.煤矿自燃  | B.下冰雹  | C.树叶变黄  | D.植物进行光合作用 |
【知识点】 光合作用的条件和产物 化学变化和物理变化的判别
A.水银、银、Hg、单质  | B.熟石灰、氧化钙、CaO、氧化物 |
| C.苏打、碳酸钠、Na2CO3、盐 | D.纯碱、氢氧化钠、NaOH、碱 |
【知识点】 常见物质的俗称 常见物质的分类 氧化物、酸、碱和盐的概念
| A.①、② | B.②、④ |
| C.②、③ | D.④、⑤ |
| A.能量无处不在,能量的形式多种多样 |
| B.我们的生活离不开能量,即使在睡觉的时候也需要能量 |
| C.运动的物体具有能量,静止的物体没有能量 |
| D.所有的自然现象都涉及能量 |
【知识点】 能量及其存在的不同形式
| A.所用氢氧化钠溶液和稀盐酸的溶质质量分数一定不相等 |
| B.混合溶液中钠离子与氯离子个数相等 |
C.混合后水分子总数增加 |
| D.混合前后阴离子总数不变 |
【知识点】 溶质质量分数的简单计算 中和反应及其应用
| A.向待测固体中加稀盐酸,产生气泡,固体中一定含有CO32﹣或HCO3﹣ |
| B.向待测溶液中加氯化钡溶液,产生不溶于硝酸的白色沉淀,待测液中一定含SO42﹣ |
| C.向待测溶液中加硝酸银溶液,产生白色沉淀,待测液中一定含有Cl﹣ |
| D.向待测溶液中加氧化铜,固体消失,溶液变蓝色,待测液中一定含有H+ |
【知识点】 酸的化学性质 盐的性质及用途 常见离子的检验方法及现象 常见物质的鉴定
| A.NaNO3 HCl Na2SO4 | B.NaNO3 NaCl CuSO4 |
| C.NaCl Na2SO4 Na2CO3 | D.NaOH BaCl2 Na2SO4 |
【知识点】 复分解反应及其应用
| A.对酸的认识 | B.对碱的认识 |
| ①酸溶液中都存在H+ ②人体胃液中含有硫酸帮助消化 ③酸雨的pH小于5.6 | ①碱溶液中都存在OH﹣ ②氢氧化钠俗称烧碱、苛性钠 ③氨水可以作为氮肥使用 |
| C.对盐的认识 | D.对有机物的认识 |
| ①盐溶液都是中性的 ②碳酸盐加稀盐酸都会产生CO2 ③工业用盐含有毒的亚硝酸钠 | ①有机物都含有碳元素 ②甲烷、食醋都是常见的有机物 ③淀粉属于有机高分子化合物 |
| A.A | B.B | C.C | D.D |
| 选项 | 物质 | 杂质 | 除杂所用的试剂和方法 |
| A | CaO固体 | CaCO3固体 | 加入适量的稀盐酸 |
| B | NaOH溶液 | Ca(OH)2溶液 | 先加入过量的Na2CO3溶液,再过滤 |
| C | CO2气体 | CO气体 | 点燃 |
| D | H2气体 | HCl气体 | 先通过NaOH溶液,再通过浓硫酸 |
| A.A | B.B | C.C | D.D |
【知识点】 常见气体的检验与除杂方法 盐的性质及用途 物质除杂或净化

| A.原气体中一定含有碳元素和氢元素 | B.可能只有甲烷 |
| C.可能只含有甲烷和氢气 | D.可能只含有氢气和一氧化碳 |

①反应后镁有剩余 ②反应后铁有剩余
③反应后稀硫酸有剩余 ④反应后稀盐酸有剩余
⑤消耗的铁和镁的质量相等 ⑥消耗的稀硫酸和稀盐酸质量相等
| A.①③⑤ | B.①②③ |
| C.①②④ | D.②③⑥ |
【知识点】 金属的化学性质 根据化学反应方程式的计算

| A.若甲是碳酸钙,则乙转化成丙的反应可以是放热反应 |
| B.若甲是碳酸钠,乙是硫酸钠,则丁可以是氯化钡 |
| C.若乙是常用的溶剂,则丁可以是单质碳 |
| D.若丙是二氧化碳,丁是熟石灰,则丁可以通过复分解反应转化为乙 |
| A.甲溶液中一定含有Ba2+ | B.乙溶液中可能含有SO42- |
C.丙溶液中一定含有Cl- | D.丁溶液中一定含有Na+ |
【知识点】 盐的性质及用途 离子或物质的共存问题 常见离子的检验方法及现象 常见物质的鉴定

| A.男演员的质量必须要大于女演员的质量 |
| B.甲处男演员的势能一定要大于乙处女演员的势能 |
| C.男演员离开跳台时的机械能一定大于乙处女演员的势能 |
| D.女演员弹起时的动能与她站在乙处时的机械能相等 |
【知识点】 动能和势能的转化与守恒
二、填空题 添加题型下试题
(1)天然气的主要成分
(2)雪碧饮料中的一种酸
(3)主要用于生产石灰和水泥的盐
(4)常用来降低土壤酸性的是

(1)性质2发生的化学反应属于哪类基本反应类型
(2)根据性质5,硫酸可以与下列哪些物质发生反应
A. 烧碱溶液
 B. 纯碱溶液
B. 纯碱溶液 C. 氯化钡溶液
 D. 食盐溶液
D. 食盐溶液
(1)加入固体后可以观察的实验现象是
(2)这个实验可以说明氢氧化钠固体具有
【知识点】 碱的物理性质及用途
(1)写出实验Ⅲ发生的化学方程式
(2)上述实验
(3)将铁、铜、银三种金属浸入
【知识点】 金属活动性顺序及其应用 金属的化学性质
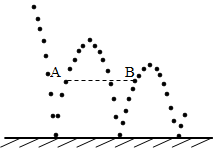

(1)有同学根据右下图中的曲线判断实验中采用了A和B中的哪一个装置的操作?
(2)在以上实验中用了酚酞作指示剂,能够说明盐酸和氢氧化钠溶液恰好完全中和的实验现象是
【知识点】 酸的化学性质 中和反应及其应用 pH值的变化 溶液的酸碱性与pH值的关系

(1)A、B两种金属的活动性大小关系是:A
(2)在Mg、Fe、Zn、Al中选择,则A、B两种金属可能是
a.Mg和Fe b.Zn和Fe c.Mg和Zn d.Al和Mg e.Al和Zn
【知识点】 金属活动性顺序及其应用 金属的化学性质

(1)Fe3O4粉末在复印机的电磁场作用下能使墨粉形成字迹或图案,这不仅利用了Fe3O4有磁性,还利用了Fe3O4是
(2)第②步加入试剂X,生成Fe(OH)2的反应方程式为
(3)在第③步反应中要控制通入O2的量,以使生成的Fe(OH)2和Fe(OH)3的质量比等于
【知识点】 金属的化学性质 酸的化学性质 盐的性质及用途 有关化学式的计算和推断
三、探究题 添加题型下试题
小海对该样品进行了系列探究:
[提出问题1]:该样品真的变质了吗?
[实验方案1]:取该样品少量于试管里,加入适量的水,振荡,样品全部溶于水,再向其中滴加过量的稀盐酸溶液,观察到
[提出问题2]:该样品是部分变质还是全部变质?
[实验方案2]:取该样品少量于烧杯里,加适量的水,搅拌,全部溶解后,再向其中加入
[提出问题3]:怎样除去样品中的杂质?
[实验方案3]:将样品全部溶于水,向其中加入适量的
【知识点】 碱的化学性质 常见离子的检验方法及现象 酸碱指示剂及其性质


步骤一:让铁球甲从斜面E点静止滚下,打到A处木块,推动木块;
步骤二:让铁球甲从斜面F点滚下,打到A处相同的木块,推动木块;
步骤三:换一铁球乙(m乙>m甲)从斜面上F点静止滚下,打到A处相同的木块,推动木块。
(1)铁球动能的大小是通过
(2)实际操作中,小军发现几次木块并未发生移动,对此你建议的改进方法
(3)为了让质量不同的甲、乙两球获得相同的初速度,有同学认为可以不用让两球都从E点滚下,而是设计了如图乙装置,只要每次让两球压缩弹簧到同样的形变程度后自然释放即可。不考虑各种能量损耗,该方法是否合理,请说明理由
【知识点】 动能的影响因素

(1)实验操作为:
a.往锥形瓶中放入适量的AlN样品;
b.打开分液漏斗的活塞往锥形瓶中加入过量的浓NaOH;
c.检验装置气密性;
d.测定收集到水的体积。
正确的操作顺序为
(2)广口瓶中的试剂X宜选用
A.稀硫酸 B.植物油 C.酒精 D.水
(3)若广口瓶内的液体没有装满(上方留有少量空间),则实验测得NH3体积将
(4)实验结束后,若观察到锥形瓶中还有固体,则样品中含有的杂质是
四、填空题 添加题型下试题
经过讨论大家一致认为不合理的猜想是
【实验探究】若猜想④成立,通过以下实验可确定固体B的成分,请将下表填写完整.
| 实验步骤 | 现 象 | 固体B的成分 |
| 有气泡产生 |
【知识点】 金属活动性顺序及其应用 金属的化学性质
(1)则X的化学式是
(2)尿素是目前使用量较大的一种
(3)尿素中碳元素和氮元素的质量比为
(4)现有100克质量分数为6%的尿素溶液,理论上可以吸收

(1)写出锂元素的符号
(2)锂离子电池供电过程中能量转化是
(3)智轨电车的胶轮轮胎是由合成材料和金属材料复合而成,其中使用的合成材料是合成橡胶,主要利用它的
A. 透气性好、耐磨
 B. 耐高温、高弹性
B. 耐高温、高弹性  C. 密度小、熔点低
C. 密度小、熔点低  D. 绝缘性好、耐低温
D. 绝缘性好、耐低温
【知识点】 合成橡胶 化学反应中能量的变化
五、解答题 添加题型下试题
| 实验 | 一 | 二 | 三 | 四 |
| 加入样品的质量/g | 5 | 10 | 15 | 20 |
| 生成CO2的质量/g | 0.88 | 1.76 | m | 2.2 |
(1)上表中m的数值是
(2)这种石灰石矿中碳酸钙的质量分数是
(3)稀盐酸中溶质的质量分数是?

(1)在实验过程中,AB段看到的明显实验现象是
(2)当滴入的Na2CO3溶液80克时,所得溶液中的溶质为
(3)求原溶液中HCl的质量分数为
(4)当滴入Na2CO3溶液至图中B点时,通过计算求所得不饱和溶液中溶质质量分数为多少
【知识点】 溶质质量分数的简单计算 酸的化学性质 盐的性质及用途 根据化学反应方程式的计算
①取100g混合溶液加入足量的AgNO3溶液,经过滤洗涤、干燥、称量得到179.375gAgCl固体;
②另取原混合溶液各100g与含有杂质的废铁屑反应(杂质不溶于水,也不参与反应),共做了五组实验,其实验数据如下表。
| 实验组别 | 一 | 二 | 三 | 四 | 五 |
| 混合溶液质量/g | 100 | 100 | 100 | 100 | 100 |
| 铁屑质量/g | 6 | 9 | 12 | 15 | 18 |
| 析出铜的质量/g | 3.2 | 4.8 | 6.4 | 8 | 8 |
请分析计算:
(1)第
(2)铁屑中铁的质量分数为多少?
(3)原混合溶液中FeCl2的质量分数为多少?
【知识点】 溶质质量分数的简单计算 盐的性质及用途 根据化学反应方程式的计算
I.取30g该铁矿粉在CO气流中充分加热,将反应后的气体用烧碱溶液充分吸收,烧碱溶液增重19.8g;
II.将上述加热后的固体取出后,再向固体逐滴加入稀硫酸,测得产生气体与滴入稀硫酸的质量关系如下图:

通过计算回答下列问题:
(1)过程ⅰ中生成气体的质量
(2)所用稀硫酸溶液的溶质质量分数为
(3)30g铁矿粉所含铁的氧化物中,氧元素的质量为
(4)通过计算可知该铁的氧化物的化学式为
【知识点】 金属的化学性质 化学式 有关化学式的计算和推断 根据化学反应方程式的计算
试卷分析
试卷题型(共 34题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 光合作用的条件和产物 化学变化和物理变化的判别 | |
| 2 | 0.85 | 常见实验操作 粗盐提纯实验 pH值的测量及方法 | |
| 3 | 0.85 | 常见物质的俗称 常见物质的分类 氧化物、酸、碱和盐的概念 | |
| 4 | 0.85 | 酸的物理性质及用途 酸的化学性质 碱的化学性质 盐的性质及用途 | |
| 5 | 0.85 | 能量及其存在的不同形式 | |
| 6 | 0.65 | 溶质质量分数的简单计算 中和反应及其应用 | |
| 7 | 0.4 | 酸的化学性质 盐的性质及用途 常见离子的检验方法及现象 常见物质的鉴定 | |
| 8 | 0.85 | 复分解反应及其应用 | |
| 9 | 0.65 | 碱的物理性质及用途 酸的物理性质及用途 盐的性质及用途 甲烷、乙炔等常见有机物的性质和用途 | |
| 10 | 0.65 | 常见气体的检验与除杂方法 盐的性质及用途 物质除杂或净化 | |
| 11 | 0.65 | 常见气体的检验与除杂方法 二氧化碳的检验和验满 物质的推断 质量守恒定律及其应用 | |
| 12 | 0.4 | 金属的化学性质 根据化学反应方程式的计算 | |
| 13 | 0.4 | 二氧化碳的化学性质 盐的性质及用途 物质的推断 复分解反应及其应用 | |
| 14 | 0.4 | 盐的性质及用途 离子或物质的共存问题 常见离子的检验方法及现象 常见物质的鉴定 | |
| 15 | 0.85 | 动能和势能的转化与守恒 | |
| 二、填空题 | |||
| 16 | 0.85 | 碱的物理性质及用途 酸的物理性质及用途 盐的性质及用途 化学式 | |
| 17 | 0.65 | 酸的化学性质 置换反应及其应用 复分解反应及其应用 | |
| 18 | 0.85 | 碱的物理性质及用途 | |
| 19 | 0.65 | 金属活动性顺序及其应用 金属的化学性质 | |
| 20 | 0.85 | 机械能 动能大小的比较 | |
| 21 | 0.65 | 酸的化学性质 中和反应及其应用 pH值的变化 溶液的酸碱性与pH值的关系 | |
| 22 | 0.65 | 金属活动性顺序及其应用 金属的化学性质 | |
| 23 | 0.4 | 金属的化学性质 酸的化学性质 盐的性质及用途 有关化学式的计算和推断 | |
| 27 | 0.65 | 金属活动性顺序及其应用 金属的化学性质 | |
| 28 | 0.65 | 盐与化肥 有关化学式的计算和推断 书写化学方程式、文字表达式 根据化学反应方程式的计算 | |
| 29 | 0.85 | 合成橡胶 化学反应中能量的变化 | |
| 三、探究题 | |||
| 24 | 0.4 | 碱的化学性质 常见离子的检验方法及现象 酸碱指示剂及其性质 | |
| 25 | 0.65 | 动能的影响因素 | |
| 26 | 0.4 | 常用气体的发生装置和收集装置与选取方法 常见气体的检验与除杂方法 碱的化学性质 盐的性质及用途 | |
| 四、解答题 | |||
| 30 | 0.4 | 溶质质量分数的简单计算 二氧化碳的实验室制法 根据化学反应方程式的计算 | |
| 31 | 0.94 | 浓硫酸的性质及浓硫酸的稀释 | |
| 32 | 0.4 | 溶质质量分数的简单计算 酸的化学性质 盐的性质及用途 根据化学反应方程式的计算 | |
| 33 | 0.4 | 溶质质量分数的简单计算 盐的性质及用途 根据化学反应方程式的计算 | |
| 34 | 0.4 | 金属的化学性质 化学式 有关化学式的计算和推断 根据化学反应方程式的计算 | |








