浙江省台州杜桥镇中学2022-2023学年九年级上学期月考科学试题
浙江
九年级
阶段练习
2024-05-06
8次
整体难度:
适中
考查范围:
常见的物质、物质的运动与相互作用、科学探究所需要的基本技能、物质的结构
一、选择题 添加题型下试题
| A.铁丝弯折 | B.钢铁熔化 | C.钢铁生锈 | D.铁球下落 |
【知识点】 化学变化和物理变化的判别
| A.牙膏(pH=9.0) |
| B.食醋(pH≈2.5) |
| C.肥皂(pH=10.0) |
| D.洗洁精(pH≈7.5) |
【知识点】 中和反应及其应用 溶液的酸碱性与pH值的关系
| A.溶液的pH大于7 | B.遇紫色石蕊试液变蓝色 |
| C.电离时生成的阴离子只有OH- | D.都能与酸反应 |
【知识点】 碱的化学性质
| A.生活中用作调味品的食盐 | B.“侯氏制碱法”制取的纯碱 |
| C.用于吸水干燥的生石灰 | D.作为建筑材料的大理石 |
【知识点】 盐的性质及用途
| A.HCl、ZnSO4、K2CO3、NaCl | B.KNO3、BaCl2、Na2SO4、NaOH |
| C.NaOH、K2CO3、NaCl、Na2SO4 | D.HCl、NaNO3、H2SO4、KCl |
【知识点】 盐的性质及用途 离子或物质的共存问题 酸碱指示剂及其性质
二、填空题 添加题型下试题
| A.分解反应 | B.化合反应 | C.置换反应 | D.复分解反应 |
三、选择题 添加题型下试题
| A.硝酸铵NH4NO3 |
| B.磷酸二氢铵NH4H2PO4 |
| C.尿素CO(NH2)2 |
| D.碳酸氢钾KHCO3 |
【知识点】 盐与化肥
| 物质的名称 | 俗名 | 化学式 | 类别 | |
| A. | 碳酸钠 | 烧碱 | Na2CO3 | 盐 |
| B. | 碳酸氢钠 | 小苏打 | NaHCO3 | 酸 |
| C. | 氢氧化钙 | 熟石灰 | CaO | 金属氧化物 |
| D. | 氢氧化钠 | 苛性碱 | NaOH | 碱 |
| A.A | B.B | C.C | D.D |

| A.Na2SO4 | B.NaCl |
| C.Na2CO3 | D.NaOH |
A.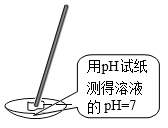 | B.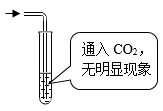 |
C. | D. |
【知识点】 中和反应及其应用
A.加热液体 | B.添加固体药品 |
C.滴加液体药品 | D.稀释浓硫酸 |
【知识点】 常见实验操作 浓硫酸的性质及浓硫酸的稀释
| A.浓盐酸 | B.NaOH溶液 | C.Ca(OH)2溶液 | D.浓硫酸 |
【知识点】 酸的化学性质 碱的化学性质 浓硫酸的性质及浓硫酸的稀释
| A.CO、H2、HCl | B.SO2、CO2、HCl | C.H2、O2、N2 | D.SO2、H2、CO |
【知识点】 碱的化学性质
下面对白色固体混合物组成的判断,正确的是( )
| A.一定同时含有NaCl、MgCl2、BaCl2、NaOH |
| B.一定含有MgCl2、BaCl2、NaOH,不含有NaCl |
| C.一定含有MgCl2、BaCl2、NaOH,可能含有NaCl |
| D.一定含有MgCl2、BaCl2,可能含有NaCl、NaOH |
【知识点】 盐的性质及用途 常见离子的检验方法及现象
四、填空题 添加题型下试题
A.水
B.氢氧化钠
C.盐酸
D.纯碱
【知识点】 盐的性质及用途
(1)少量存于胃液中帮助消化的是
(2)常用降低土壤酸性的是
(3)在日常生活中用做调味剂的是
(4)做馒头时用于除去面团发酵生成的酸的是

(2)已知X是金属单质,请写出稀硫酸与Y反应的一个化学方程式
【知识点】 酸的化学性质 书写化学方程式、文字表达式

(1)在滴加的过程中,烧杯中溶液的 pH 逐渐
(2)由图可知,稀盐酸与氢氧化钠溶液发生的反应是
【知识点】 中和反应及其应用 溶液的酸碱性与pH值的关系
(1)X的化学式为
(2)硝酸铵用做肥料时,要避免与

A.稀HCl B.酚酞试液 C.CaCl2 D.Ca(OH)2
(2)依据反应②,KOH能与下列物质反应的是
A.H2SO4 B.BaCl2 C.CuSO4 D.Na2CO3
(1)如图表示的是一些物质在常温下的近似pH,回答下列问题:

②测量苹果汁pH时,先用蒸馏水润湿pH试纸,会使pH偏
(2)焊接工业上常用稀盐酸清洗铁锈,写出用稀盐酸除铁锈的化学方程式为
【知识点】 酸的化学性质 溶液的酸碱性与pH值的关系
五、探究题 添加题型下试题

(2)实验结束后,同学们将废液倒入同一只废液缸中,最后发现废液浑浊并显红色。
【提出问题】废液中含有什么物质?
【假设猜想】通过分析上述实验,同学们猜想:废液中除酚酞和水外一定含有氯化钠。
老师问:废液中还可能有什么物质?
某同学脱口而出:废液中一定含有氢氧化钠,他的说法正确吗?同学们认为不准确,理由是:
(3)【实验验证】同学们对可能含有的物质进行进一步确定,取一定量的废液过滤,向滤液中加入几滴氯化钙溶液,发现马上产生了白色沉淀。根据该现象可以确定该废液中一定还含有
(4)【拓展提高】那么废液中是否含有氢氧化钠?
请你写出在原实验的基础上作出进一步判断的方法:
【知识点】 碱的化学性质 盐的性质及用途 常见离子的检验方法及现象 酸碱指示剂及其性质
六、填空题 添加题型下试题
(1)医生用胃舒平(主要成分Al(OH)3)来治疗胃酸过多的疾病,请用方程式表示原理:
(2)如图:①最先产生气泡的是
②B烧杯中先出现的现象是
(3)浓硫酸可以用做干燥剂是因为它具有

七、探究题 添加题型下试题

(2)稀硫酸加入到装有物质A的试管中并微微加热,溶液由无色变为蓝色,则物质A是
(3)为确定试管②中无色溶液的溶质成分,只要取适量该溶液,滴加
【知识点】 酸的化学性质
八、解答题 添加题型下试题

(2)该试剂瓶中硫酸溶液的质量为
(3)欲配制20%的稀硫酸200克,需取出该浓硫酸多少克?体积为多少毫升?
【知识点】 密度公式的应用 溶质质量分数的简单计算 氧化物、酸、碱和盐的概念
九、探究题 添加题型下试题

(2)据图分析在实验操作过程中应是往
(3)某同学借助无色酚酞试液观察反应进程,则当观察到的实验
【知识点】 中和反应及其应用 pH值的变化 溶液的酸碱性与pH值的关系
十、填空题 添加题型下试题
| 配料 | 氯化钠、碘酸钾(KIO3) |
| 保质期 | 18个月 |
| 食用方法 | 勿长时间炖炒 |
| 贮藏指南 | 避光、避热、密封、防潮 |
(2)由表中信息可知碘酸钾受热易分解,该性质属于
(3)KIO3中I元素的质量分数是多少
十一、解答题 添加题型下试题
(1)参加反应的二氧化碳气体的质量是
(2)反应后溶液中溶质的质量分数是多少
【知识点】 根据化学反应方程式的计算
XX钙片 主要成分:CaCO3 规格:每片2.0g 用量:一日一次,每次2片 含量:碳酸钙__g/片 |
(2)反应后产生气体的质量
(3)试通过计算求每片钙片中碳酸钙的含量。

【知识点】 二氧化碳的实验室制法 质量守恒定律及其应用 根据化学反应方程式的计算
| 第1次 | 第2次 | 第3次 | 第4次 | |
| 加入稀盐酸的质量/g | 20 | 20 | 20 | 20 |
| 烧杯中剩余物质的质量/g | 118.2 | 136.4 | 155.6 | 175.6 |
(2)草木灰浸出液中K2CO3的质量分数是多少?
(3)请写出草木灰浸出液中含有硫酸根离子的验证方法

试卷分析
试卷题型(共 32题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.94 | 化学变化和物理变化的判别 | |
| 2 | 0.94 | 中和反应及其应用 溶液的酸碱性与pH值的关系 | |
| 3 | 0.85 | 碱的化学性质 | |
| 4 | 0.94 | 盐的性质及用途 | |
| 5 | 0.65 | 盐的性质及用途 离子或物质的共存问题 酸碱指示剂及其性质 | |
| 7 | 0.85 | 盐与化肥 | |
| 8 | 0.85 | 碱的物理性质及用途 盐的性质及用途 常见物质的俗称 | |
| 9 | 0.65 | 酸的化学性质 复分解反应及其应用 | |
| 10 | 0.85 | 中和反应及其应用 | |
| 11 | 0.85 | 酸的化学性质 | |
| 12 | 0.85 | 常见实验操作 浓硫酸的性质及浓硫酸的稀释 | |
| 13 | 0.85 | 酸的化学性质 碱的化学性质 浓硫酸的性质及浓硫酸的稀释 | |
| 14 | 0.85 | 碱的化学性质 | |
| 15 | 0.65 | 盐的性质及用途 常见离子的检验方法及现象 | |
| 二、填空题 | |||
| 6 | 0.94 | 盐的性质及用途 复分解反应及其应用 | |
| 16 | 0.85 | 盐的性质及用途 | |
| 17 | 0.85 | 酸的化学性质 碱的化学性质 盐的性质及用途 | |
| 18 | 0.85 | 酸的化学性质 书写化学方程式、文字表达式 | |
| 19 | 0.85 | 中和反应及其应用 溶液的酸碱性与pH值的关系 | |
| 20 | 0.65 | 酸碱指示剂及其性质 溶液的酸碱性与pH值的关系 有关化学式的计算和推断 | |
| 21 | 0.85 | 盐与化肥 化学方程式的配平 | |
| 22 | 0.85 | 碱的化学性质 盐的性质及用途 | |
| 23 | 0.85 | 酸的化学性质 溶液的酸碱性与pH值的关系 | |
| 25 | 0.65 | 酸的化学性质 中和反应及其应用 浓硫酸的性质及浓硫酸的稀释 书写化学方程式、文字表达式 | |
| 29 | 0.85 | 化学性质与物理性质的差别及应用 有关化学式的计算和推断 常见物质的分类 | |
| 三、探究题 | |||
| 24 | 0.65 | 碱的化学性质 盐的性质及用途 常见离子的检验方法及现象 酸碱指示剂及其性质 | |
| 26 | 0.65 | 酸的化学性质 | |
| 28 | 0.65 | 中和反应及其应用 pH值的变化 溶液的酸碱性与pH值的关系 | |
| 四、解答题 | |||
| 27 | 0.65 | 密度公式的应用 溶质质量分数的简单计算 氧化物、酸、碱和盐的概念 | |
| 30 | 0.65 | 根据化学反应方程式的计算 | |
| 31 | 0.65 | 二氧化碳的实验室制法 质量守恒定律及其应用 根据化学反应方程式的计算 | |
| 32 | 0.65 | 溶质质量分数的简单计算 盐的性质及用途 酸碱指示剂及其性质 根据化学反应方程式的计算 | |



