浙江省诸暨市浣纱初中2019-2020学年九年级九月份阶段性测试科学试题
浙江
九年级
阶段练习
2019-10-24
243次
整体难度:
适中
考查范围:
常见的物质、物质的结构、科学探究所需要的基本技能、物质的运动与相互作用
一、选择题 添加题型下试题
A.柠檬pH(2∽3) | B.西红柿pH(4∽5) |
C.橙子pH(3∽4)  | D.西瓜pH(5∽6) |
【知识点】 溶液的酸碱性与pH值的关系
| A.溶液的质量减小 | B.溶液的浓度减小 | C.溶质的质量减小 | D.溶剂的质量增大 |
【知识点】 酸的物理性质及用途 浓硫酸的性质及浓硫酸的稀释
| 药品柜 | 甲 | 乙 | 丙 | 丁 |
| 药品 | CuO、MnO2等 | HCl、H2SO4等 | KOH、Ca(OH)2等 | NaCl、CuSO4等 |
A.甲 | B.乙 | C.丙 | D.丁 |
【知识点】 氧化物、酸、碱和盐的概念
加入的物质 | 石蕊试液 | Fe2O3粉末 | BaCl2溶液 |
现象 | 试液变红 | 固体逐渐溶解,溶液变黄 | 无明显现象 |
| A.稀盐酸 | B.稀硫酸 |
| C.NaOH溶液 | D.Na2CO3溶液 |
【知识点】 酸的化学性质
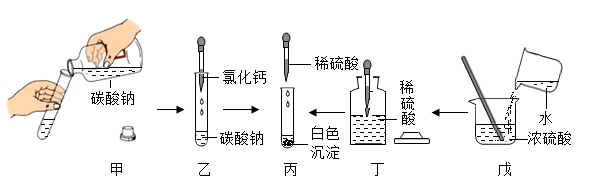
| A.甲中试剂瓶标签正对手心,是为了防止手被腐蚀 |
| B.乙中将滴管伸入试管内,是为了防止试剂滴落到试管外 |
| C.丁中试剂瓶盖倒放在桌面上,主要是为了避免瓶中试剂受污染 |
| D.戊中将水缓缓倒入浓硫酸并搅拌,是为了防止局部过热引起酸液飞溅 |
【知识点】 实验操作注意事项的探究 浓硫酸的性质及浓硫酸的稀释
| 选项 | 物质 | 杂质 | 操作 |
| A | CaO | CaCO3 | 加入过量的水,过滤 |
| B | 盐酸 | 硫酸 | 加入过量的BaCl2溶液,过滤 |
| C | NaNO3溶液 | NaCl溶液 | 加入过量的AgNO3溶液,过滤 |
| D | CaCl2溶液 | 稀盐酸 | 加入过量的CaCO3粉末,过滤 |
| A.A | B.B | C.C | D.D |
【知识点】 物质除杂或净化

A.①② | B.①②④ | C.②④ | D.①②③ |
二、填空题 添加题型下试题
(1)用于治疗胃酸过多症的是
(2)用作改良酸性土壤的是
(3)用作食品调味剂的是
(1)打开两瓶分别盛有浓硫酸和浓盐酸的试剂瓶,瓶口出现白雾的是盛有
(2)下列是探究酸性质的实验

在盛有少量氧化铜粉末的试管中加入足量稀盐酸,观察到的实验现象是

(1)请你在编号②处各填入一种物质。②是
(2)若编号④的物质是盐,请你写出符合编号④的一个化学方程式:
(1)氢氧化钠固体敞口放置容易变质,写出氢氧化钠变质的化学方程式
(2)课堂上老师做了其中一个实验,在试管中加入2~3mL氯化铁溶液,然后滴加1~2mL氢氧化钠溶液,观察到的实验现象是

(1)碱溶液能使酚酞溶液变
(2)图中的X代表一类物质,则X为
(3)碱溶液有相似化学性质的原因是都含有
【知识点】 碱的化学性质 酸碱指示剂及其性质 书写化学方程式、文字表达式
OH﹣ | NO3﹣ | Cl﹣ | SO42﹣ | CO32﹣ | |
H+ | ﹣ | 溶、挥 | 溶、挥 | 溶 | 溶、挥 |
Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
Ca2+ | 溶 | 溶 | 溶 | 微 | 不 |
Ba2+ | 溶 | 溶 | 溶 | 不 | 不 |
(1)酸、碱、盐之间发生的复分解反应,其实质是它们的溶液中离子之间相互结合生成沉淀或气体或水,否则反应就不能发生.则BaCl2溶液和NaNO3溶液混合后,
(2)写出一个有CaCO3生成的反应化学方程式
【知识点】 盐的性质及用途 书写化学方程式、文字表达式 复分解反应及其应用
三、探究题 添加题型下试题
I.取少量固体样品于烧杯中,先加足量水溶解,再加入足量的
 溶液,有白色沉淀产生;
溶液,有白色沉淀产生;II.继续向烧杯中滴加稀盐酸并不断搅拌,烧杯内固体质量随加入稀盐酸质量的变化如图所示.
请回答下列问题:
(
 )AB段观察到的现象是
)AB段观察到的现象是(
 )C点时,溶液中一定含有的溶质是
)C点时,溶液中一定含有的溶质是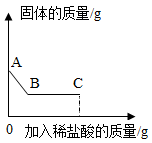
【知识点】 盐的性质及用途 常见离子的检验方法及现象 常见物质的鉴定
四、填空题 添加题型下试题
【知识点】 溶质质量分数的简单计算 盐的性质及用途 根据化学反应方程式的计算
五、探究题 添加题型下试题
把自制的紫甘蓝(紫色包心菜)如图(1)所示分别滴加到试管中,观察到的现象如表所示:

| 溶液 | 白醋 | 盐酸 | 食盐水 | 草木灰水 | 石灰水 |
| 加入紫甘蓝汁后的颜 | 红色 | 红色 | 紫色 | 蓝 | 蓝 |
(1)观察表中的紫甘蓝汁颜色变化情况,紫甘蓝汁
(2)用pH试纸测定图1中部分溶液的酸碱度:白醋pH
(3)图2是三位同学分别测定某溶液酸碱度的操作示意图,其中可能导致被测溶液的pH数值发生改变的错误操作是
【知识点】 酸碱指示剂及其性质 pH值的测量及方法 溶液的酸碱性与pH值的关系
回答下列问题。
(1)填写表中的空格。
| 实验过程 | 实验现象 | 实验结论 |
| 向盛有少量Fe2O3的试管中加入NaCl溶液,振荡 | 固体不溶解 |
(2)是否需要做“向Fe2O3中加入水”的对比实验?为什么?
(3)写出盐酸清除铁锈的化学方程式:
【提出问题】氢氧化钠溶液与稀盐酸混合后,所得溶液中溶质的成分是什么?
【作出猜想】
甲同学猜想:溶质有NaCl、HCl、NaOH
乙同学猜想:溶质只有NaCl
丙同学猜想:溶质有NaCl、HCl
你的猜想:溶质有
乙同学认为甲同学的猜想是错误的,理由是
【实验设计及验证】请你将下列实验报告填写完整:
| 实验操作 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中,加入碳酸钠溶液 | 丙同学的猜想正确 | |
| 有蓝色沉淀生成 | 你的猜想正确 |
【知识点】 中和反应及其应用 盐的性质及用途 常见离子的检验方法及现象

【提出问题】这瓶溶液是什么溶液?
【获得信息】酸、碱、盐的性质实验中用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠
【提出猜想】这瓶溶液是:猜想一:氯化钠溶液;猜想二:氢氧化钠溶液;猜想三:碳酸钠溶液。
【实验推断】
⑴小丽取样滴加无酚酞试液,溶液呈红色。
⑵小刚另取样滴加稀盐酸有
⑶小青认为小刚的结论不完全正确,理由是
小组同学讨论后一致认为还需要进行如下实验:
【继续探究】另取样加入过量的CaCl2溶液,观察到有白色沉淀产生,设计这一步骤的目的是
【实验结论】猜想
六、填空题 添加题型下试题

(1)硝酸铵属于
(2)把烧杯放在事先已洒上少量水的玻璃片上,然后向烧杯内加入一定量硝酸铵和氢氧化钡晶体,并用玻璃棒迅速搅拌后静置片刻,提起烧杯,发现玻璃片与烧杯底部粘在一起,玻璃片上的水结成了冰(如图)。由实验可知,氢氧化钡晶体与硝酸铵晶体反应时

【知识点】 盐与化肥 常见离子的检验方法及现象 化学反应中能量的变化
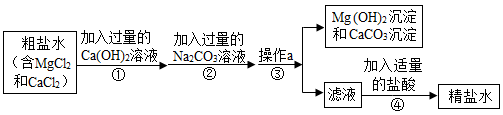
(1)步骤①反应的化学方程式为
(2)步骤③操作a的名称是
(3)若步骤①和步骤②的顺序颠倒,则最后所得的精盐水中还含有
【知识点】 过滤的原理、方法、操作及其应用 碱的化学性质 盐的性质及用途
七、解答题 添加题型下试题

【知识点】 溶解现象与溶解原理
步骤一:配制溶质质量分数为10%的氢氧化钠溶液。
步骤二:向20克待测稀盐酸中逐滴滴入上述氢氧化钠溶液,并使用pH计记录溶液的pH变化情况,绘制图像如下图。

(1)在步骤一中需要用到的玻璃仪器有
(2)在往稀盐酸中逐渐滴入氢氧化钠溶液的过程中,当溶液的pH达到2时,溶液中的溶质有
(3)已知发生反应的化学方程式为:NaOH + HCl=NaCl + H2O,请结合右图,计算该稀盐酸的溶质质量分数。
【知识点】 溶质质量分数的简单计算 中和反应及其应用 根据化学反应方程式的计算
| 反应时间t/s | t0 | t1 | t2 | t3 | t4 | t5 | t6 | t7 |
| 气体质量m/g | 0 | 0.88 | 1.76 | 2.64 | 3.52 | 4.4 | x | 4.4 |
(1)表中x的值为
(2)计算样品中氯化钠的质量
(3)计算完全反应后所得溶液中溶质的质量分数
【知识点】 溶质质量分数的简单计算 酸的化学性质 盐的性质及用途 根据化学反应方程式的计算

(1)P点时溶液中的溶质名称是
(2)反应生成沉淀的最大质量为多少克?
(3)求原BaCl2溶液的溶质质量分数?
【知识点】 溶质质量分数的简单计算 盐的性质及用途 根据化学反应方程式的计算
八、探究题 添加题型下试题

【提出问题1】某品牌牙膏中是否含有CaCO3?
【查阅资料】二氧化硅不与稀盐酸反应。
(1)【实验方案】取少量牙膏于试管中,加入适量的稀盐酸,出现气泡,将气体通入澄清石灰水,石灰水变浑浊,证明摩擦剂中含有
(2)【提出问题2】该牙膏中CaCO3的质量分数是多少?
【实验步骤】①按如图连接好装置后,发现一处明显的错误,改正为
②重新连接好装置,并再次检查装置的气密性;
③在B装置中加入牙膏样品8g
④关闭K1, 打开K2, 向牙膏样品中滴入10%的盐酸,至B中无气泡产生时,停止滴加盐酸;
⑤关闭K2, 打开K1缓缓地通入空气,至C中不再产生沉淀;
⑥将C装置中的固液混合物过滤、洗涤、烘干后称量其质量。
(3)实验数据如图(已知此品牌牙膏中的其他成分不和盐酸反应,装置内试剂均足量)

【实验分析及数据处理】
①若没有A装置,则测定结果将
②D装置的作用是
③据上面数据,计算该牙膏样品中碳酸钙的质量分数是
【知识点】 碱的化学性质 盐的性质及用途 根据化学反应方程式的计算
试卷分析
试卷题型(共 27题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 溶液的酸碱性与pH值的关系 | |
| 2 | 0.65 | 酸的物理性质及用途 浓硫酸的性质及浓硫酸的稀释 | |
| 3 | 0.94 | 氧化物、酸、碱和盐的概念 | |
| 4 | 0.65 | 酸的化学性质 碱的化学性质 盐的性质及用途 酸碱指示剂及其性质 | |
| 5 | 0.65 | 酸的化学性质 | |
| 6 | 0.85 | 实验操作注意事项的探究 浓硫酸的性质及浓硫酸的稀释 | |
| 7 | 0.65 | 物质除杂或净化 | |
| 8 | 0.4 | 中和反应及其应用 盐的性质及用途 | |
| 二、填空题 | |||
| 9 | 0.85 | 碱的物理性质及用途 盐的性质及用途 | |
| 10 | 0.85 | 酸的物理性质及用途 酸的化学性质 | |
| 11 | 0.85 | 酸的化学性质 盐的性质及用途 | |
| 12 | 0.85 | 碱的化学性质 盐的性质及用途 | |
| 13 | 0.65 | 碱的化学性质 酸碱指示剂及其性质 书写化学方程式、文字表达式 | |
| 14 | 0.65 | 盐的性质及用途 书写化学方程式、文字表达式 复分解反应及其应用 | |
| 16 | 0.4 | 溶质质量分数的简单计算 盐的性质及用途 根据化学反应方程式的计算 | |
| 21 | 0.65 | 盐与化肥 常见离子的检验方法及现象 化学反应中能量的变化 | |
| 22 | 0.65 | 过滤的原理、方法、操作及其应用 碱的化学性质 盐的性质及用途 | |
| 三、探究题 | |||
| 15 | 0.4 | 盐的性质及用途 常见离子的检验方法及现象 常见物质的鉴定 | |
| 17 | 0.85 | 酸碱指示剂及其性质 pH值的测量及方法 溶液的酸碱性与pH值的关系 | |
| 18 | 0.65 | 控制变量法 酸的化学性质 | |
| 19 | 0.65 | 中和反应及其应用 盐的性质及用途 常见离子的检验方法及现象 | |
| 20 | 0.4 | 酸的化学性质 碱的化学性质 盐的性质及用途 酸碱指示剂及其性质 | |
| 27 | 0.65 | 碱的化学性质 盐的性质及用途 根据化学反应方程式的计算 | |
| 四、解答题 | |||
| 23 | 0.85 | 溶解现象与溶解原理 | |
| 24 | 0.65 | 溶质质量分数的简单计算 中和反应及其应用 根据化学反应方程式的计算 | |
| 25 | 0.4 | 溶质质量分数的简单计算 酸的化学性质 盐的性质及用途 根据化学反应方程式的计算 | |
| 26 | 0.65 | 溶质质量分数的简单计算 盐的性质及用途 根据化学反应方程式的计算 | |







