浙江省台州市椒江区第五中学2019届九年级上学期第一次月考科学试题
浙江
九年级
阶段练习
2019-07-25
226次
整体难度:
适中
考查范围:
科学探究所需要的基本技能、常见的物质、物质的运动与相互作用、物质的结构、生命系统的构成层次、人类生存的地球、增进对科学探究的理解和提高探究的能力
一、选择题 添加题型下试题
A. 取固体药品 取固体药品 | B. 收集氧气 收集氧气 |
C. 稀释浓硫酸 稀释浓硫酸 | D. 检查气密性 检查气密性 |
| A.阿拉伯胶在反应中相当于催化剂 |
| B.喷涌而出的二氧化碳是一种氧化物 |
| C.喷涌现象发生时,既有化学变化又有物理变化 |
| D.把曼妥思薄荷糖放入雪碧中不能形成喷涌现象 |
【知识点】 影响化学反应速率的因素 催化剂在化学反应中的作用
| A.用小苏打作焙制糕点的发酵粉 | B.用硫磺熏制白木耳、粉丝等食品 |
| C.用甲醛溶液作食用水产品的防腐剂 | D.用含亚硝酸钠的工业用盐腌制食品 |
【知识点】 盐的性质及用途
| 选项 | 性质 | 用途 |
| A | 氢氧化钙呈碱性 | 改良酸性土壤 |
| B | 浓硫酸具有脱水性 | 干燥氧气 |
| C | 稀盐酸能与某些金属氧化物反应 | 除铁锈 |
| D | 氢氢化钠能与某此非金属氧化物反应 | 吸收二氧化硫 |
| A.A | B.B | C.C | D.D |

| A.V示数变小,A示数变大 |
| B.V示数变大,A示数变小 |
| C.V示数变小,A示数变小 |
| D.V示数变大,A示数变大 |

| A.天气预报瓶利用天气和大气压的关系进行预报的 |
| B.A管和B球液面相平时,显示内外气压一致 |
| C.A管液面明显下降时,往往转为阴雨天气 |
| D.B球内装较多红墨水,可以减少瓶内温度变化造成的干扰 |

A.Fe2O3+3CO 2Fe+3CO2 2Fe+3CO2 |
B.2KMnO4 K2MnO4+MnO2+O2↑ K2MnO4+MnO2+O2↑ |
| C.Zn+2HCl2=ZnCl2+H2↑ |
| D.NaOH+HCl=NaCl+H2O |
【知识点】 化合价规律和原则 氧化反应 还原反应 识别化学反应基本类型

| A.小球受力平衡 |
| B.小球的速度不变 |
| C.如果将细线剪断,小球将做匀速直线运动 |
| D.细线对小球的拉力为零 |
【知识点】 力的作用效果
①比较硬度,硬度小的是“愚人金”
②灼烧,表面变色的是“愚人金”
③浸没在稀硫酸中,表面有气泡产生的是“愚人金”
④浸没在硫酸锌溶液中,表面附着白色物质的是“愚人金”
| A.①③ | B.②④ | C.①④ | D.②③ |
【知识点】 金属活动性顺序及其应用 金属的化学性质 合金与合金的性质
| A.HCl、CuSO4 、KCl、Ma2SO4 | B.Na2CO3、Na2SO4、HCl、H2SO4 |
| C.K2CO3 、NaOH、HCl、BaCl2 | D.HCl、NaOH、CaCl2、KNO3 |
| A.该粉末中一定含有CaCO3、Na2SO4、BaC12 |
| B.该粉末中一定不含有KNO3、CuSO4 |
| C.该粉末中一定含有KNO3 |
| D.该粉末中一定含有Na2SO4、KNO3、BaC12 |

| A.甲表示向一定量硫酸铜和硫酸混合液中加入氢氧化钠溶液 |
| B.乙表示加热一定量氯酸钾和二氧化锰的混合物 |
| C.丙表示向盛有少量二氧化锰的烧杯中不断加入双氧水 |
| D.丁表示向一定量氢氧化钠溶液中加入稀盐酸 |
【知识点】 实验室制取氧气的反应原理 碱的化学性质 中和反应及其应用
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向收集满CO2的软塑料瓶中加入约 1/3体积的食盐水,旋紧瓶盖,振荡 | 塑料瓶变瘪 | CO2能与食盐反应 |
| B | 点燃从导管放出的某气体,在火焰上 方罩一个冷而干燥的烧杯 | 烧杯内壁有无色液滴产生 | 被点燃的气体一定是H2 |
| C | 某溶液中加入BaCl2溶液和稀硝酸 | 有白色沉淀产生 | 溶液中一定含有硫酸根离子 |
| D | 将白磷浸没在热水中,再向热水中的 白磷通氧气 | 通氧气前白磷不燃烧, 通氧气后白磷燃烧 | 氧气是可燃物燃烧的条件之一 |
| A.A | B.B | C.C | D.D |
【知识点】 二氧化碳的化学性质 常见离子的检验方法及现象 燃烧的条件
二、填空题 添加题型下试题
(1)西瓜和杨梅味甜多汁,这些汁液主要存在于果肉细胞的
A.细胞膜 B.细胞质 C.细胞核 D.液泡
(2)西瓜和杨梅的种子数目不同,是因为子房内
【知识点】 细胞的结构

(1)如图为微信登录界面。若按界面中人所在角度去观察地球,能看到南极洲。则从此人所在角度观察,地球自转的方向为
(2)6月12日这一天,南极点附近为
【知识点】 地球自转 地球自转的方向和周期 地球公转 昼夜长短变化

【知识点】 材料制造与环境保护 有关元素化合价的计算
(1)高层建筑的楼顶常装有用钢铁做的避雷针,其作用是将雷电引导到地下,这说明钢铁具有良好的
(2)小王家厨房里的菜刀生锈了,铁生锈需要有
【知识点】 金属的物理性质及用途 金属锈蚀的条件及其防护 酸的化学性质
三、探究题 添加题型下试题
方法一:用胶头滴管直接吸取足量汗液转移到烧杯中,再加入适量蒸馏水稀释;
方法二:用出汗的手在盛有自来水的容器中清洗,再将清洗后的自来水转移到烧杯中。
(1)你认为她应该选用的是方法
(2)用试管取适量提取液,滴入硝酸钡溶液,没有出现白色沉淀,说明汗液中
(3)用试管取适量提取液,滴入硝酸银溶液,发现出现白色沉淀,加入稀硝酸后沉淀不溶解。由此可推测该白色沉淀的化学式是
(4)将适量的提取液倒入蒸发皿中加热蒸发,出现类似食盐的小颗粒。你认为她能否仅凭上述三步实验得出“这些小颗粒就是氯化钠”?
【知识点】 盐的性质及用途 常见离子的检验方法及现象 物质的推断
四、填空题 添加题型下试题
(1)有新闻联播报道:我国在南海成功完成了“可燃冰”试验开采工作。可燃冰主要成分是甲烷,学名叫“天然气水合物”,是一种高效清洁、储量巨大的新能源。甲烷作燃料是因为它具有
(2)一定条件下氢气与溶解在水中的二氧化碳结合生成甲烷和水,这一化学反应被称作“产甲烷作用”。请写出“产甲烷作用”的化学方程式:
五、解答题 添加题型下试题

(1)打开止水夹后观察到的现象是
(2)反应后将集气瓶中混合物过滤,所得溶液中除Na2CO3外,则溶液中还存在的溶质有
【知识点】 碱的化学性质
六、探究题 添加题型下试题
I.取少量固体样品于烧杯中,先加足量水溶解,再加入足量的
 溶液,有白色沉淀产生;
溶液,有白色沉淀产生;II.继续向烧杯中滴加稀盐酸并不断搅拌,烧杯内固体质量随加入稀盐酸质量的变化如图所示.
请回答下列问题:
(
 )AB段观察到的现象是
)AB段观察到的现象是(
 )C点时,溶液中一定含有的溶质是
)C点时,溶液中一定含有的溶质是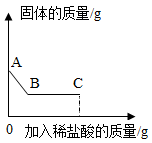
【知识点】 盐的性质及用途 常见离子的检验方法及现象 常见物质的鉴定
(1)请完成证明金属粉末中存在Fe和Cu的实验设计:
| 实验操作 | 实验现象 | 结论 |
| Ⅰ取少量的金属粉末于试管中,加入足量的 | 有气泡产生 | 仅除去铝 |
| Ⅱ将试管静置,弃去上层清液,加入足量的稀硫酸 | 证明含有铁 | |
| Ⅲ将试管静置,弃去上层清液,多次洗涤剩余固体 | 剩余固体呈紫红色 | 证明含有铜 |
(2)为探究该金属粉末中Al的质量分数,取20g该金属粉末,加入氢氧化钠溶液反应,剩余固体质量与所加氢氧化钠溶液的质量关系如图所示,则该金属粉末中Al的质量分数为

【知识点】 金属活动性顺序及其应用 金属的化学性质 酸的化学性质 碱的化学性质
【建立猜想】①两种酸溶液的pH不同。(注:pH相同,则单位体积溶液中H+数目相同)②两种酸溶液中的阴离子不同。
【实验过程】
| 实验 次数 | 试剂 | 实验条件 | 实验现象 |
| 1 | 0.2克CuO粉末+6毫升pH=0的盐酸 | 常温 | 黑色粉末很快溶解,溶液呈蓝绿色 |
| 2 | 0.2克CuO粉末+6毫升pH=0的硫酸 | 常温 | 无明显现象 |
| 3 | 0.2克CuO粉末+6毫升pH=0的硫酸+0.35克NaCl | 常温 | 黑色粉末很快溶解.溶液呈蓝绿色 |
| 4 | 0.2克CuO粉末+6毫升pH=0的硫酸+0.35克 | 常温 | 无明显现象 |
【实验结论】常温下,pH相同的盐酸和硫酸溶液于CuO反应现象出现差异的原因是由于
【知识点】 获取事实与证据 酸的化学性质 溶液的酸碱性与pH值的关系

【猜 想】Mg(OH)Cl分解后产物可能有Mg、MgCl2、MgO、HCl气体、H2O、Cl2。老师告诉他产物就是上述猜想中的其中几种,并提示Cl2是一种黄绿色有刺激性气味的气体。
【实验一】取少量的Mg(OH)Cl放入试管中,按如图所示装置进行实验,加热过程中观察到足量硝酸银溶液中有白色沉淀产生,一段时间后,沉淀不再产生,大试管口也没有液滴形成,管内有固体剩余,无其他现象。由此推知Mg(OH)Cl分解后产物中有
【实验二】取少量实验一剩余固体于试管中,加入足量稀盐酸,没有气泡产生。由此推知Mg(OH)Cl分解后产物中没有
【实验三】再取少量实验一剩余固体加入足量稀硝酸,固体全部溶解,再滴入AgNO3溶液,无沉淀产生。自此推知Mg(OH)Cl分解后产物中没有
【结论】Mg(OH)Cl受热分懈的化学反应方程式为
【知识点】 酸、碱、盐的鉴别
七、解答题 添加题型下试题

实验步骤如下:先分别称量蜡烛、装置Ⅱ、装置Ⅲ的质量,按图示连接好仪器装置,点燃蜡烛,同时从a导管口抽气,一段时间后熄灭蜡烛,再分别称量蜡烛、装置Ⅱ、装置Ⅲ的质量。实验数据如表:
| 蜡烛 | 装置Ⅱ | 装置Ⅲ | |
| 反应前的质量/g | 15.8 | 182.3 | 212.2 |
| 反应后的质量/g | 14.4 | 184.1 | 216.6 |
(1)由该实验数据计算,蜡烛中碳、氢元素的质量之比为
(2)装置Ⅱ 和装置Ⅲ 的顺序能否颠倒?

(1)装置C在实验中的作用是
(2)仅根据D装置中黑色粉末变红这一现象,能否证明混合气体中一定存在CO?请判断并说明理由
(3)小丁根据装置E中出现白色硫酸铜粉末变成蓝色的实验现象,得出该混合气体中有氢气存在的结论。你认为结论是否可靠?若可靠,请说明理由;若不可靠,请对图1实验装置提出改进意见。
(4)图1方案中B装置可用来吸收CO2但没有现象。为证明CO2和NaOH能发生反应,小丁又设计了图2所示的方案。则图2方案中所加试剂X应该是
【知识点】 常见气体的检验与除杂方法 二氧化碳的化学性质

(2)一个花青素分子中共有
(3)28.7克花青素中含有多少克碳元素?(请列式计算)
八、探究题 添加题型下试题
【查阅资料】蒸馏水不能使紫色石蕊试液变色。

【知识点】 二氧化碳的化学性质

【资料查阅】Na2CO3溶液与CuSO4溶液混合能产生蓝色沉淀。
【活动与探究】取一定量上述固体粉末,加足量水溶解。
(1)【现象与结论】经上述操作,得到蓝色澄清溶液,则原固体粉末中一定没有
(2)【探索与拓展】为进一步确定原固体粉末的组成,该实验小组同学先用托盘天平称取46.2g该粉末,溶于水配成174.6g溶液,再往其中加入溶质质量分数为8%的NaOH溶液,产生沉淀的质量与所加NaOH溶液质量的关系如图所示。据图回答:
①计算产生最大沉淀量时所加NaOH溶液的质量。
②通过计算确定46.2g固体粉末的组成。(回答出物质名称和其质量)
【知识点】 盐的性质及用途 根据化学反应方程式的计算
九、填空题 添加题型下试题
| 功能 | 迎宾、送餐等 |
| 质量 | 50kg |
| 移动速度 | 0.2~0.6m/s |
| 电池容量 | 12Ah |
| 功率 | 最大功率100W |
| 工作电压 | 24V |
| 最大送餐质量 | 15kg |
(2)机器人底盘的轮子与水平地面接触的总面积为0.01米2,求机器人水平运送3千克物体(含餐盘)时,对地面产生的压强。
(3)如果该机器人以最大功率在水平地面上以0.4米/秒的速度匀速前进10秒,求机器人行进过程中受到地面对它的阻力。
(提示:机器人行进过程中的牵引力F=功率P/速度V,即F=P/V)


【知识点】 增大压强的方法及其应用 功率计算公式的应用
十、解答题 添加题型下试题

(1)P点溶液中的溶质是
(2)m1为多少克?(列式计算)
(3)混合溶液与NaOH溶液恰好完全反应时,溶液中的溶质质量分数是多少?(保留小数点后一位)
【知识点】 酸的化学性质 碱的化学性质 盐的性质及用途 根据化学反应方程式的计算
十一、探究题 添加题型下试题

(1)甲同学实验中所发生的化学方程式为
【查阅资料】CaCl2、NaCl的溶液呈中性,Na2CO3溶液呈
【实验探究一】确定甲、乙同学上述实验后所得溶液中的溶质.
(2)取甲所得溶液少许,加入石蕊试液,溶液显红色,甲所得溶液中一定含有的溶质是
(3)取乙所得溶液少许,加入酚酞试液,溶液显红色,乙所得溶液中一定含有的溶质是
【实验探究二】
(4)甲、乙同学把上述实验所得溶液倒入同一废液缸中,观察到废液缸中产生少量气泡,最终有白色沉淀生成,该白色沉淀是
【讨论交流】丙同学提出:若将上述废缸中物质取出,过滤,所得滤液中含有哪些物质呢?经过讨论大家一致认为:一定含有NaCl,可能含有CaCl2、盐酸和Na2CO3中的部分物质.
【实验探究三】取少量滤液于试管中,滴加过量的稀硝酸,可观察到有大量气泡产生.
【归纳总结】该滤液中含有的溶质是氯化钠和
(5)【探索与拓展】有一份由Na2SO4、NaCl两种物质组成的固体样品.为确定其组成,上述小组同学将样品全部溶于蒸馏水中制成119.3g溶液,再往其中加入104gBaCl2溶液,两者恰好完全反应.过滤,得到23.3g白色沉淀和一定质量的滤液.经测定,该滤液中溶质质量分数为9%.试计算:(均需计算过程)所用BaCl2的溶液中溶质的质量分数.所用样品的质量.
【知识点】 溶质质量分数的简单计算 酸的化学性质 盐的性质及用途 酸碱指示剂及其性质
十二、填空题 添加题型下试题
(1)硫酸铜所含阴离子的符号是
(2)煅烧石灰石(主要成分CaCO3)可制得生石灰(CaO).若要制取11.2t氧化钙,根据化学方程式计算需要碳酸钙的质量是多少?
(3)波尔多液不能用铁质容器来配制的原因是
【知识点】 溶解现象与溶解原理 金属活动性顺序及其应用 离子 根据化学反应方程式的计算
试卷分析
试卷题型(共 35题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 常见实验操作 常用气体的发生装置和收集装置与选取方法 浓硫酸的性质及浓硫酸的稀释 | |
| 2 | 0.85 | 影响化学反应速率的因素 催化剂在化学反应中的作用 | |
| 3 | 0.65 | 盐的性质及用途 | |
| 4 | 0.65 | 碱的化学性质 中和反应及其应用 | |
| 5 | 0.65 | 常见物质的俗称 化学式 | |
| 6 | 0.85 | 电流表的读数方法 电压表的读数方法 电路的动态分析 | |
| 7 | 0.85 | 大气压强的存在 大气压与人类生活 | |
| 8 | 0.65 | 化合价规律和原则 氧化反应 还原反应 识别化学反应基本类型 | |
| 9 | 0.65 | 力的作用效果 | |
| 10 | 0.65 | 金属活动性顺序及其应用 金属的化学性质 合金与合金的性质 | |
| 11 | 0.4 | 酸、碱、盐的鉴别 复分解反应及其应用 | |
| 12 | 0.65 | 金属活动性顺序及其应用 金属的化学性质 | |
| 13 | 0.4 | 酸的化学性质 盐的性质及用途 常见物质的鉴定 | |
| 14 | 0.4 | 实验室制取氧气的反应原理 碱的化学性质 中和反应及其应用 | |
| 15 | 0.4 | 二氧化碳的化学性质 常见离子的检验方法及现象 燃烧的条件 | |
| 二、填空题 | |||
| 16 | 0.85 | 细胞的结构 | |
| 17 | 0.85 | 地球自转 地球自转的方向和周期 地球公转 昼夜长短变化 | |
| 18 | 0.65 | 材料制造与环境保护 有关元素化合价的计算 | |
| 19 | 0.65 | 金属的物理性质及用途 金属锈蚀的条件及其防护 酸的化学性质 | |
| 21 | 0.85 | 甲烷、乙炔等常见有机物的性质和用途 书写化学方程式、文字表达式 | |
| 32 | 0.65 | 增大压强的方法及其应用 功率计算公式的应用 | |
| 35 | 0.65 | 溶解现象与溶解原理 金属活动性顺序及其应用 离子 根据化学反应方程式的计算 | |
| 三、探究题 | |||
| 20 | 0.65 | 盐的性质及用途 常见离子的检验方法及现象 物质的推断 | |
| 23 | 0.4 | 盐的性质及用途 常见离子的检验方法及现象 常见物质的鉴定 | |
| 24 | 0.65 | 金属活动性顺序及其应用 金属的化学性质 酸的化学性质 碱的化学性质 | |
| 25 | 0.65 | 获取事实与证据 酸的化学性质 溶液的酸碱性与pH值的关系 | |
| 26 | 0.4 | 酸、碱、盐的鉴别 | |
| 30 | 0.4 | 二氧化碳的化学性质 | |
| 31 | 0.65 | 盐的性质及用途 根据化学反应方程式的计算 | |
| 34 | 0.4 | 溶质质量分数的简单计算 酸的化学性质 盐的性质及用途 酸碱指示剂及其性质 | |
| 四、解答题 | |||
| 22 | 0.65 | 碱的化学性质 | |
| 27 | 0.65 | 浓硫酸的性质及浓硫酸的稀释 有关化学式的计算和推断 质量守恒定律及其应用 | |
| 28 | 0.65 | 常见气体的检验与除杂方法 二氧化碳的化学性质 | |
| 29 | 0.65 | 酸碱指示剂及其性质 有关化学式的计算和推断 化学符号及其周围数字的意义 | |
| 33 | 0.15 | 酸的化学性质 碱的化学性质 盐的性质及用途 根据化学反应方程式的计算 | |




