有一包白色固体样品,可能含碳酸钠、硫酸钠、氯化钠、氢氧化钠中的一种或几种.小科同学为探究其成分做了以下实验:
I.取少量固体样品于烧杯中,先加足量水溶解,再加入足量的 溶液,有白色沉淀产生;
溶液,有白色沉淀产生;
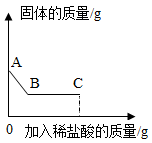
II.继续向烧杯中滴加稀盐酸并不断搅拌,烧杯内固体质量随加入稀盐酸质量的变化如图所示.
请回答下列问题:
( )AB段观察到的现象是
)AB段观察到的现象是____________________ .
( )C点时,溶液中一定含有的溶质是
)C点时,溶液中一定含有的溶质是____________________ .
I.取少量固体样品于烧杯中,先加足量水溶解,再加入足量的
 溶液,有白色沉淀产生;
溶液,有白色沉淀产生;II.继续向烧杯中滴加稀盐酸并不断搅拌,烧杯内固体质量随加入稀盐酸质量的变化如图所示.
请回答下列问题:
(
 )AB段观察到的现象是
)AB段观察到的现象是(
 )C点时,溶液中一定含有的溶质是
)C点时,溶液中一定含有的溶质是
更新时间:2018-11-11 00:40:18
|
相似题推荐
探究题
|
较难
(0.4)
【推荐1】定性和定量结合既是化学的重要思想,也是研究物质组成的重要方法。某研究性学习小组为检测实验室用H2还原CuO所得红色固体Cu中是否含有Cu2O(红色),进行了认真的探究。请你一起踏上探究之路,回答下列问题。
【查阅资料】
①无水CuSO4遇水变蓝;
②高温灼烧CuO生成Cu2O和O2;
③Cu2O与稀H2SO4反应:Cu2O+H2SO4=Cu+CuSO4+H2O。
【设计实验方案】
方案1 取该红色固体加入适量稀H2SO4,实验现象___________ ,结论为红色固体中含有Cu2O。
方案2装置如图所示,拟通过干燥管中CuSO4变蓝来判断红色固体是否含有Cu2O。

(1)为确保探究的科学、合理、安全。实验中还应采取的措施有___________ ;填序号)
①加热前先排尽装置中的空气;
②在氢气发生器与硬质玻璃管之间加一个干燥装置;
③在盛有CuSO4的干燥管后再连接一个装有浓H2SO4的洗气瓶。
(2)由方案2实验后得出结论:红色固体中含有Cu2O。写出红色固体Cu2O与H2反应的化学方程式___________
方案3 称得干燥坩埚(常用于固体加热的容器)的质量为ag,取红色固体置于坩埚中称得总质量为bg,在空气中高温灼烧至质量恒定,称得最后坩埚与固体总质量为cg。
(1)该实验方案最少得进行___________ 次称量;
(2)若确认红色固体中含有Cu2O,则c与a,b应符合的数学关系式为___________ 。
【查阅资料】
①无水CuSO4遇水变蓝;
②高温灼烧CuO生成Cu2O和O2;
③Cu2O与稀H2SO4反应:Cu2O+H2SO4=Cu+CuSO4+H2O。
【设计实验方案】
方案1 取该红色固体加入适量稀H2SO4,实验现象
方案2装置如图所示,拟通过干燥管中CuSO4变蓝来判断红色固体是否含有Cu2O。

(1)为确保探究的科学、合理、安全。实验中还应采取的措施有
①加热前先排尽装置中的空气;
②在氢气发生器与硬质玻璃管之间加一个干燥装置;
③在盛有CuSO4的干燥管后再连接一个装有浓H2SO4的洗气瓶。
(2)由方案2实验后得出结论:红色固体中含有Cu2O。写出红色固体Cu2O与H2反应的化学方程式
方案3 称得干燥坩埚(常用于固体加热的容器)的质量为ag,取红色固体置于坩埚中称得总质量为bg,在空气中高温灼烧至质量恒定,称得最后坩埚与固体总质量为cg。
(1)该实验方案最少得进行
(2)若确认红色固体中含有Cu2O,则c与a,b应符合的数学关系式为
您最近一年使用:0次
探究题
|
较难
(0.4)
【推荐2】化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究:查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体生成。
I、摩擦剂中氢氧化铝的定性检验取适量牙膏样品,加水成分搅拌、过滤。(已知:氢氧化铝 能溶解在氢氧化钠溶液中,生成NaAlO2和水)
II、牙膏样品中碳酸钙的定量测定利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。

依据实验过程回答下列问题:
(1)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:___________ 。
(2)C中反应生成BaCO3的化学方程式是___________ 。
(3)下列各项措施中,不能提高测定准确度的是___________ (填标号)。
A.在加入盐酸之前,应排净装置内的CO2气体
B. 滴加盐酸不宜过快
C. 在A-B之间增添盛有浓硫酸的洗气装置
D.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(4)实验中准确称取8.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g。则样品中碳酸钙的质量分数为___________ 。
(5)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是___________ 。
I、摩擦剂中氢氧化铝的定性检验取适量牙膏样品,加水成分搅拌、过滤。(已知:氢氧化铝 能溶解在氢氧化钠溶液中,生成NaAlO2和水)
II、牙膏样品中碳酸钙的定量测定利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。

依据实验过程回答下列问题:
(1)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:
(2)C中反应生成BaCO3的化学方程式是
(3)下列各项措施中,不能提高测定准确度的是
A.在加入盐酸之前,应排净装置内的CO2气体
B. 滴加盐酸不宜过快
C. 在A-B之间增添盛有浓硫酸的洗气装置
D.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(4)实验中准确称取8.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g。则样品中碳酸钙的质量分数为
(5)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是
您最近一年使用:0次
探究题
|
较难
(0.4)
名校
【推荐3】某初中化学兴趣小组的同学们利用所学的知识和一些实验用品,围绕着实验室中的一瓶氢氧化钠溶液,展开了下列实验探究活动:
【提出问题1】瓶中氢氧化钠溶液是否变质?若变质是否完全变质?
【实验与结论】小组的同学们设计并进行了如图所示的实验:

步骤一:向溶液A中滴加过量的__________ (填化学式)溶液,溶液中产生白色沉淀,得出这瓶氢氧化钠溶液已变质。
步骤二:向过滤后得到的滤液B中通入CO2气体,观察到液面下导管口有气泡冒出,溶液中__________ 。
(填实验现象),进而得出这瓶氢氧化钠溶液部分变质。
【提出问题2】探究氢氧化钠的变质程度(氢氧化钠的变质程度= )
)
【深入探究】两位同学分别从瓶中取等质量的溶液进行了相应的实验(实验过程中不考虑氢氧化钠再与空气中的任何成分发生反应)。并将实验步骤及相关数据记录如下:
【分析与结论】通过分析发现,根据两位同学的数据,就可以计算出氢氧化钠的变质程度__________ (用百分比表示)。
【提出问题1】瓶中氢氧化钠溶液是否变质?若变质是否完全变质?
【实验与结论】小组的同学们设计并进行了如图所示的实验:

步骤一:向溶液A中滴加过量的
步骤二:向过滤后得到的滤液B中通入CO2气体,观察到液面下导管口有气泡冒出,溶液中
(填实验现象),进而得出这瓶氢氧化钠溶液部分变质。
【提出问题2】探究氢氧化钠的变质程度(氢氧化钠的变质程度=
 )
)【深入探究】两位同学分别从瓶中取等质量的溶液进行了相应的实验(实验过程中不考虑氢氧化钠再与空气中的任何成分发生反应)。并将实验步骤及相关数据记录如下:
| 甲同学 | 乙同学 | |
| 实验步骤及相关数据 | 将所取溶液蒸干,称量所得固体,质量为4.26g | 向所取溶液中加入足量的Ba(OH)2溶液,充分反应后过滤,将滤渣洗涤、干燥、称量为1.97g |
您最近一年使用:0次
探究题
|
较难
(0.4)
【推荐1】一包白色固体混合物,可能由硫酸铜、碳酸钠、硫酸钠、氯化钠中的一种或几种混合而成,为确定其组成进行如图所示的实验:

试推断:
(1)混合物中一定没有的物质是________ (写出化学式)
(2)当“现象A”出现_____ 时,则证明原混合物中既有碳酸钠又有硫酸钠 。

试推断:
(1)混合物中一定没有的物质是
(2)当“现象A”出现
您最近一年使用:0次
探究题
|
较难
(0.4)
【推荐2】一包白色固体粉末,可能由氯化钠、氢氧化钠、碳酸钠、硫酸钠、氢氧化钙中的一种或几种组成,为了探究这包粉末的组成,进行以下实验:(提示:碳酸钠溶液具有弱碱性)
①取少量样品,加水溶解,无现象。加入足量的稀盐酸,有气泡产生。
②另取少量样品,加水溶解,滴加无色酚酞试液,溶液变红色。
③取第②步红色溶液,进行了如下实验。

(1)白色沉淀M是________ 。(填名称)
(2)加入的试剂X是________ 。(填化学式)
(3)通过上述实验确定该白色粉末中一定含有________ 。(填化学式)
①取少量样品,加水溶解,无现象。加入足量的稀盐酸,有气泡产生。
②另取少量样品,加水溶解,滴加无色酚酞试液,溶液变红色。
③取第②步红色溶液,进行了如下实验。

(1)白色沉淀M是
(2)加入的试剂X是
(3)通过上述实验确定该白色粉末中一定含有
您最近一年使用:0次
探究题
|
较难
(0.4)
【推荐1】课本中有一问:为什么汗水有咸味?学习小组同学为此开展探究.
[提出问题]汗水中产生咸味的物质是什么?
[假设与猜想]根据生活经验推测,汗水中产生咸味的物质可能是_________ .
[制订计划]为了证明咸味物质是猜想中的物质,一是要证明汗水溶液中含有阴离子___ (填写离子符号),
二是要证明汗水溶液中有阳离子_______ (填写离子符号).
[进行实验]
证明阴离子的实验:向汗水溶液中滴加____ 溶液,再加入少量稀硝酸,振荡,仍有白色沉淀产生.
[分析与交流]上述实验中,证明阴离子存在的化学反应方程式为:_______________ ,该反的基本反应类型是______ .
[提出问题]汗水中产生咸味的物质是什么?
[假设与猜想]根据生活经验推测,汗水中产生咸味的物质可能是
[制订计划]为了证明咸味物质是猜想中的物质,一是要证明汗水溶液中含有阴离子
二是要证明汗水溶液中有阳离子
[进行实验]
证明阴离子的实验:向汗水溶液中滴加
[分析与交流]上述实验中,证明阴离子存在的化学反应方程式为:
您最近一年使用:0次
探究题
|
较难
(0.4)
【推荐2】某化学兴趣小组在进行酸碱中和反应的实验探究时,向烧杯中的氢氧化钠溶液滴加稀盐酸一会儿后,发现忘记添加酸碱指示剂。某同学从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到试管中溶液不变色。于是针对此溶液的成分,同学们进行了科学探究。
(1)猜想与假设:
猜想一:反应后氢氧化钠过量,溶液呈碱性;
猜想二:氢氧化钠与盐酸恰好完全中和,溶液呈中性;
猜想三:__________________________________ 。
同学们经过讨论后觉得猜想一不正确,其理由是:_______________________________ 。
(2)设计并进行实验:
①化学兴趣小组的同学为了验证自己的猜想,设计了实验方案一:
②请你设计另一个实验方案(与实验方案一不同),验证猜想三成立,并填写下表:
(1)猜想与假设:
猜想一:反应后氢氧化钠过量,溶液呈碱性;
猜想二:氢氧化钠与盐酸恰好完全中和,溶液呈中性;
猜想三:
同学们经过讨论后觉得猜想一不正确,其理由是:
(2)设计并进行实验:
①化学兴趣小组的同学为了验证自己的猜想,设计了实验方案一:
实验步骤 | 实验现象 | 实验结论 |
用洁净、干燥的玻璃棒蘸取少量反应后的溶液滴在干燥的pH试纸上,观察颜色变化并与标准比色卡对比。 | pH (填“>”、“=”或“<”)7 | 猜想二不成立 猜想三成立 |
②请你设计另一个实验方案(与实验方案一不同),验证猜想三成立,并填写下表:
实验步骤 | 实验现象 | 实验结论 |
猜想三成立 |
您最近一年使用:0次
探究题
|
较难
(0.4)
【推荐3】有一包白色粉末,可能是由硫酸铜、氯化钠、碳酸钠、硫酸钠中的一种或几种组成,为检验其中的成分,小科经实验得到下表,请完成相关内容。
(3)小明认为小科的实验方案有问题,不能得出白色粉末中一定有氯化钠,你建议小科如何改进实验?_________________
| 实验步骤及现象 | 结论 |
| ①将少许白色粉末溶于水得到无色溶液A | 白色粉末中一定没有(1) |
| ②在A中加入足量氯化钡溶液,生成白色沉淀B,过滤得滤液C; 在白色沉淀B中加入足量稀硝酸,(2) (填实验现象) | 白色粉末中一定有碳酸钠和硫酸钠 |
| ③在滤液C中加入硝酸银溶液,出现白色沉淀,再滴加稀硝酸,沉淀不溶解 | 白色粉末中一定有氯化钠 |
(3)小明认为小科的实验方案有问题,不能得出白色粉末中一定有氯化钠,你建议小科如何改进实验?
您最近一年使用:0次




