2013-2014学年浙江省宁波七中九年级第一学期第一次月考科学试卷
浙江
九年级
阶段练习
2016-02-29
286次
整体难度:
适中
考查范围:
常见的物质、物质的运动与相互作用、科学探究所需要的基本技能、物质的结构、生物的新陈代谢
一、选择题 添加题型下试题
| A.将水缓缓倒入盛有浓硫酸的烧杯中,边倒边搅拌 |
| B.将浓硫酸缓缓倒入盛有水的量筒中,边倒边搅拌 |
| C.将浓硫酸和水同时倒入一试剂瓶中,充分振荡 |
| D.将浓硫酸缓缓倒入盛有水的烧杯中,边倒边搅拌 |
【知识点】 浓硫酸的性质及浓硫酸的稀释
A. | B. | C. | D. |
【知识点】 金属活动性顺序及其应用 金属的化学性质
| A.一定含有硫酸根离子 |
| B.一定含有银离子 |
| C.只有硫酸根离子,没有银离子 |
| D.可能含有硫酸根离子或银离子 |
【知识点】 盐的性质及用途 常见离子的检验方法及现象
 。该化学反应属于( )
。该化学反应属于( )| A.分解反应 | B.化合反应 | C.置换反应 | D.复分解反应 |
【知识点】 识别化学反应基本类型
A. |
B. |
C. |
D. |
| A.保存三甲基一氯硅时应密封防水 |
| B.扑灭三甲基一氯硅引发的着火,应使用二氧化碳、干粉灭火剂,并用弱碱性水处理 |
| C.三甲基一氯硅水溶液呈中性 |
| D.三甲基一氯硅由碳、氢、硅、氯四种元素组成 |
【知识点】 有机物的特性
| A.金属元素有正化合价,因此非金属元素一定没有正化合价 |
| B.碱都含有氢元素,所以含有氢元素的化合物一定是碱 |
| C.中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应 |
| D.氧化物只含有两种元素,所以氧化物中一定有一种元素不是氧元素 |
【知识点】 中和反应及其应用 氧化物、酸、碱和盐的概念 化合价规律和原则
 SiO2+Ti。该反应中的还原剂是( )
SiO2+Ti。该反应中的还原剂是( )| A.Si | B.TiO2 | C.SiO2 | D.Ti |
【知识点】 书写化学方程式、文字表达式 氧化反应 还原反应

| A.化学方程式中乙、丁的分子个数比为1:1 |
| B.甲和丁中同种元素化合价不相等 |
| C.该反应中共有三种元素 |
| D.乙和丙中所含元素种类相同 |
【知识点】 构成物质的微粒 质量守恒定律及其应用
| A.用钢丝球洗刷铝锅脏物 |
| B.用洗洁精洗去餐具上的油污,是因为它具有乳化作用 |
| C.铵态氮肥与熟石灰混合使用可以明显提高肥效 |
| D.为减少“白色污染”,应将废弃塑料制品随地焚烧 |
【知识点】 乳浊液的概念及其与溶液的区别 金属锈蚀的条件及其防护 盐的性质及用途
| A.活性炭 | B.淀粉溶液 | C.无水硫酸铜 | D.酚酞溶液 |
【知识点】 酸碱指示剂及其性质
A.在 的溶液中: 的溶液中: 、 、 、 、 |
B.在 的溶液中: 的溶液中: 、 、 、 、 |
C.在 的溶液中: 的溶液中: 、 、 、 、 |
D.在 的溶液中: 的溶液中: 、 、 、 、 |
【知识点】 离子或物质的共存问题
A. 向pH=3的溶液中加水 向pH=3的溶液中加水 |
B. 一定质量的稀盐酸与锌粒反应 一定质量的稀盐酸与锌粒反应 |
C. 向H2SO4和CuSO4混合溶液中加NaOH溶液 向H2SO4和CuSO4混合溶液中加NaOH溶液 |
D. 煅烧一定质量的石灰石 煅烧一定质量的石灰石 |
【知识点】 酸的化学性质 碱的化学性质 盐的性质及用途 溶液的酸碱性与pH值的关系
| A.完全反应得到无色溶液,样品中一定没有CaCO3 |
| B.NaCl不与盐酸反应,样品中一定没有NaCl |
| C.所加稀盐酸中溶质的质量分数为7.3% |
| D.Na2CO3和MgCO3都能和盐酸反应生成气体,样品中一定有Na2CO3和MgCO3 |
| A.通常情况下,HN3的水溶液pH<7 |
| B.HN3能与NaOH反应生成NaN3 |
| C.NH4N3属于盐类 |
| D.NaN3受到撞击时会发生爆炸生成氮气,是因为NaN3中含有N2分子 |
A.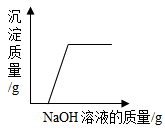 在稀盐酸中加入氯化铜,然后向其中逐滴加入NaOH溶液 在稀盐酸中加入氯化铜,然后向其中逐滴加入NaOH溶液 |
B. 在NaOH溶液中加入CaCO3,然后向其中逐滴加入稀盐酸 在NaOH溶液中加入CaCO3,然后向其中逐滴加入稀盐酸 |
C. 在NaOH溶液中加入CuO,然后向其中逐滴加入稀硫酸 在NaOH溶液中加入CuO,然后向其中逐滴加入稀硫酸 |
D. 在NaOH溶液中加入Ba(NO3)2,然后向其中逐滴加入稀硫酸 在NaOH溶液中加入Ba(NO3)2,然后向其中逐滴加入稀硫酸 |
| A.碳酸钠 | B.氢氧化钙 | C.碳酸镁 | D.氧化铁 |
【知识点】 天平的使用 盐的性质及用途 质量守恒定律及其应用 根据化学反应方程式的计算
二、填空题 添加题型下试题
(1)氢氧化钠溶液易变质的原因是 (写化学方程式)。
(2)取少量已部分变质的氢氧化钠溶液于试管中,滴入足量稀盐酸后可观察到 的现象。
【知识点】 碱的化学性质

(1)金属单质B的化学式是
(2)金属铁与蓝色溶液D反应的化学方程式为
【知识点】 金属的化学性质
(1)氢氟酸的pH 7(选填“>”、“=”或“<”);
(2)剧毒性和腐蚀性属于氢氟酸的 性质(选填“物理”或“化学”)
(3)写出氢氟酸与熟石灰反应的化学方程式 。
【知识点】 酸的化学性质 pH值的变化 溶液的酸碱性与pH值的关系
(1)找证据:收集、分析各种证据是认识物质的基本方法。如汗液有咸味,因此有同学认为汗液中有氯化钠。为了验证猜想,他收集了一定量的汗液,然后向其中滴加一种化学试剂,看到有白色沉淀生成,这种化学试剂是 。
(2)推理:食盐和工业用盐(主要成分为亚硝酸钠,化学式NaNO2)都有咸味,但亚硝酸钠对人体是有剧毒的。比较食盐和亚硝酸钠的化学式,可推断亚硝酸钠组成成分中的 是有剧毒的。(用离子符号表示)
【知识点】 物质的推断

(1)根据以上信息可知,上表中X=
(2)按照下列要求,请从不同的角度比较磷酸和硫酸:
①相同分子数时,物质的质量:磷酸
②溶液的质量及溶质的质量分数均相同时溶液的pH:磷酸溶液

回答下列问题。
(1)加入过量A(Fe粉)反应后,再进行操作a,此操作为
(2)工厂废液中加入过量A反应的化学方程式为
(3)溶液甲中的金属离子是
(4)步骤①②③中所发生的化学反应,其中属于置换反应的是
(5)铁红是炼铁的主要原料,写出用CO和铁红炼铁的化学方程式
【知识点】 过滤的原理、方法、操作及其应用 金属的化学性质 金属的冶炼 置换反应及其应用
光合作用最简表达式为:

(1)10千克小球藻在光照条件下,1小时可产生 克葡萄糖。
(2)过去人们一直对于光合作用产物O2的来源感到疑惑。若宇航员利用中子数不同的两种氧原子18O和16O标记水和二氧化碳分子中的氧原子,进行了如图实验。请你判断光合作用产生的O2来自 。

| A.CO2 |
| B.H2O |
| C.部分来自CO2,部分来自H2O |
| D.无法判断 |
【知识点】 光合作用的条件和产物 有关化学式的计算和推断 质量守恒定律及其应用
三、探究题 添加题型下试题
【提出问题】黑色颗粒和白色物质是什么?
【进行猜想】甲认为黑色颗粒是
乙同学还认为白色物质是氢氧化钠。
甲同学立刻认为乙同学的猜想是错误的,其理由是
【查阅资料】氧化钠为白色粉末,溶于水生成氢氧化钠:Na2O + H2O = 2NaOH
【实验探究】甲同学对白色物质进行实验探究。
| 实验方案 | 实 验 操 作 | 实验现象 | 结 论 |
| 方案1 | 取样品少量于试管中,加入适量水,振荡,样品 全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质为Na2O |
| 方案2 | ①取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 | 出现白色沉淀 | 白色物质是 |
| ②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
【反思评价】丙同学认为方案1得到的结论不正确,理由是
【得出结论】钠在二氧化碳中燃烧的化学方程式为
【知识点】 盐的性质及用途
四、填空题 添加题型下试题

(1)实验中,证明混合气体中有水蒸气的现象是白色固体变为蓝色;若B中澄清石灰水出现浑浊现象,则证明混合气体中有二氧化碳,证明混合气体中有一氧化碳的现象是
(2)若混合气体中含有CO,在F处尚缺少的实验仪器的名称是
(3)如果将上述装置中的A,B交换.则不能检验混合气体中是否含有
【知识点】 常见气体的检验与除杂方法 金属的冶炼
五、探究题 添加题型下试题
(1)金属镁是一种较活泼金属,在二氧化碳气体中也能燃烧。燃烧的化学方程式为
 ,此反应类型属于( )
,此反应类型属于( ) A 分解反应
B 化合反应
C 置换反应
D 复分解反应
(2)镁铝合金广泛用于火箭、导弹和飞机制造业等。某兴趣小组为探究镁铝合金的组成,取7.8 g镁铝合金样品,投入到足量的稀硫酸溶液中,共收集得到氢气0.8克,则该合金中,镁和铝的质量比为 。
(3)老师每次做有关镁的实验时都会强调:镁是一种银白色有金属光泽的金属。但拿出的镁条总是有一层灰黑色的“外衣”,这层灰黑色的外衣是什么物质呢?
猜想:小明认为可能是MgO;小亮认为可能是Mg2(OH)2CO3;小龙认为可能是Mg(OH)2。小龙认为小明的猜想是错误的,其理由是 。

实验探究:小亮按上图所示装置进行实验,发现试管口有液滴出现,澄清石灰水变浑浊,同时受热的试管内产生了白色固体。
实验分析:实验后,小亮认为小龙的猜测也是错误的,其理由是 。
查阅资料得出结论:Mg(OH)2和Mg2(OH)2CO3都可以加热分解,产物均为氧化物,据此请你写出Mg2(OH)2CO3加热分解的化学方程式 。
【知识点】 酸的化学性质 碱的化学性质 盐的性质及用途 根据化学反应方程式的计算
六、填空题 添加题型下试题

(1)葡萄糖的化学式为C6H12O6,它是由 种元素组成的,其碳、氢元素的质量比C:H= 。
(2)现要配制10kg这种葡萄糖注射液,需要葡萄糖 kg。
七、解答题 添加题型下试题
| 反应时间(秒) | 0 | 25 | 50 | 75 | 100 | 125 | 150 | 175 | 200 |
| 滴入稀盐酸体积(毫升) | 0 | 4 | 8 | 12 | 16 | 20 | 24 | 28 | 32 |
| pH | 13.2 | 13.0 | 12.7 | 12.4 | 12.1 | 7.0 | 2.0 | 1.6 | 1.3 |
| 温度(℃) | 36.9 | 37.5 | 38.0 | 38.5 | 38.8 | 39.2 | 39.0 | 38.8 | 38.6 |
(1)观察上表发现,当反应时间在
(2)分析上表数据发现,在逐渐滴加稀盐酸的过程中,溶液的温度先升高后降低,请分析原因:
(3)结合上表中滴入稀盐酸体积与pH的变化数据,试计算氢氧化钠稀溶液中溶质的质量。
【知识点】 中和反应及其应用 根据化学反应方程式的计算

根据所得数据计算:
(1)500g该废水中硫酸铜的质量。
(2)该废水中硫酸的溶质质量分数。
 NaNO3+H2O+NH3↑)。把产生的所有NH3用足量的硫酸溶液吸收,同时测量2分钟内硫酸溶液增加的质量,结果如下表所示:
NaNO3+H2O+NH3↑)。把产生的所有NH3用足量的硫酸溶液吸收,同时测量2分钟内硫酸溶液增加的质量,结果如下表所示:| 时间/s | 0 | 20 | 30 | 40 | 60 | 80 | 100 | 120 |
| 增加的质量/g | 0 | 0.7 | m | 1.2 | 1.5 | 1.6 | 1.7 | 1.7 |
试回答下列问题:
(1)请在下面的坐标纸上,以反应时间为横坐标,以产生的NH3质量为纵坐标,画出能够表明产生气体的质量随时间变化的关系曲线;

(2)表中m约为
(3)硝酸铵样品的纯度是多少?
(4)试计算反应后所得硝酸钠溶液的溶质质量分数(不考虑反应过程中水损失的质量)。
【知识点】 酸的化学性质 盐的性质及用途 根据化学反应方程式的计算
试卷分析
试卷题型(共 34题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 浓硫酸的性质及浓硫酸的稀释 | |
| 2 | 0.65 | 酸的化学性质 酸、碱、盐的鉴别 | |
| 3 | 0.65 | 金属活动性顺序及其应用 金属的化学性质 | |
| 4 | 0.65 | 盐的性质及用途 常见离子的检验方法及现象 | |
| 5 | 0.85 | 识别化学反应基本类型 | |
| 6 | 0.65 | 金属活动性顺序及其应用 复分解反应及其应用 金属、金属氧化物、碱之间的转化 | |
| 7 | 0.64 | 有机物的特性 | |
| 8 | 0.64 | 常见实验操作 | |
| 9 | 0.65 | 中和反应及其应用 氧化物、酸、碱和盐的概念 化合价规律和原则 | |
| 10 | 0.94 | 书写化学方程式、文字表达式 氧化反应 还原反应 | |
| 11 | 0.65 | 构成物质的微粒 质量守恒定律及其应用 | |
| 12 | 0.65 | 乳浊液的概念及其与溶液的区别 金属锈蚀的条件及其防护 盐的性质及用途 | |
| 13 | 0.85 | 酸碱指示剂及其性质 | |
| 14 | 0.65 | 离子或物质的共存问题 | |
| 15 | 0.65 | 酸的化学性质 碱的化学性质 盐的性质及用途 溶液的酸碱性与pH值的关系 | |
| 16 | 0.4 | 酸的化学性质 盐的性质及用途 | |
| 17 | 0.4 | 中和反应及其应用 溶液的酸碱性与pH值的关系 氧化物、酸、碱和盐的概念 | |
| 18 | 0.65 | 中和反应及其应用 盐的性质及用途 | |
| 19 | 0.65 | 碱的化学性质 | |
| 20 | 0.4 | 天平的使用 盐的性质及用途 质量守恒定律及其应用 根据化学反应方程式的计算 | |
| 二、填空题 | |||
| 21 | 0.65 | 碱的化学性质 | |
| 22 | 0.85 | 金属的化学性质 | |
| 23 | 0.94 | 酸的化学性质 pH值的变化 溶液的酸碱性与pH值的关系 | |
| 24 | 0.85 | 物质的推断 | |
| 25 | 0.65 | 溶质质量分数的简单计算 溶液的酸碱性与pH值的关系 有关化学式的计算和推断 | |
| 26 | 0.4 | 过滤的原理、方法、操作及其应用 金属的化学性质 金属的冶炼 置换反应及其应用 | |
| 27 | 0.4 | 光合作用的条件和产物 有关化学式的计算和推断 质量守恒定律及其应用 | |
| 29 | 0.65 | 常见气体的检验与除杂方法 金属的冶炼 | |
| 31 | 0.85 | 一定溶质质量分数的溶液的配制 化学式 有关化学式的计算和推断 标签上标示的物质成分及其含义 | |
| 三、探究题 | |||
| 28 | 0.4 | 盐的性质及用途 | |
| 30 | 0.4 | 酸的化学性质 碱的化学性质 盐的性质及用途 根据化学反应方程式的计算 | |
| 四、解答题 | |||
| 32 | 0.65 | 中和反应及其应用 根据化学反应方程式的计算 | |
| 33 | 0.94 | 酸的化学性质 碱的化学性质 酸、碱、盐的鉴别 | |
| 34 | 0.4 | 酸的化学性质 盐的性质及用途 根据化学反应方程式的计算 | |











